Clear Sky Science · he
העלייה ב-CST1 המתווכת על ידי NFATC2 מקדמת גדילה ומטסטזות של כולנגיוקרצינומה
מדוע הסיפור על סרטן כבד זה חשוב
כולנגיוקרצינומה תוך‑כבדית היא סכנה קטלנית שמתחילה בצינורות המרה הקטנים בתוך הכבד. לעתים קרובות היא מתגלה בשלב מאוחר, מתפשטת במהירות ומגיבה בצורה לקויה לטיפולים סטנדרטיים. מחקר זה חושף שרשרת מולקולרית נסתרת שעוזרת לתאי הגידול להתחמק מהזדקנות, לגדול ללא הרף ולהתפשט לאיברים מרוחקים. על‑ידי חשיפת השרשרת הזו, העבודה מצביעה על דרכים חדשות שיכולות לעכב או לעצור את סרטן זה שקשה לטפל בו.
מבט קרוב על סרטן כבד שקט אך קטלני
כולנגיוקרצינומה מהווה רק חלק קטן ממקרי הסרטן של הכבד, אך גורמת לחלק לא פרופורציונלי ממקרי המוות בשל סרטן ברחבי העולם. סיבה אחת לכך היא שהתסמינים המוקדמים מטושטשים או חסרים, ולכן רבים מהמטופלים מאובחנים רק לאחר שהמחלה התקדמה. המחברים התחילו בחיפוש בבסיסי נתונים ציבוריים גדולים של ביטוי גנים, יחד עם דגימות גידול מבית החולים שלהם, כדי לזהות גנים שהם באופן עקבי פעילים יותר בגידולי צינורות מרה מאשר ברקמה נורמלית ושגם מנבאים הישרדות ירודה. מתוך מאות גנים משתנים בלט גן אחד: CST1, שמקודד חלבון מופרש קטן בשם ציסטאטין SN. מטופלים שלגידוליהם היו רמות גבוהות של CST1 חיו תקופות משמעותית קצרות יותר, מה שסימן את CST1 כסמן אזהרה וכמניע פוטנציאלי של המחלה.
כיצד חלבון בודד מחזק גדילה והתפשטות
כדי לבדוק את תפקידו של CST1, החוקרים השתמשו בקווי תאים של סרטן צינורות מרה שבהם יכלו להעלות או להנמיך את רמות CST1. כאשר הכריחו תאים לייצר יותר CST1, התאים התרבו מהר יותר, זזו ביתר קלות דרך מחסומים נקבוביים והצליחו לחדור ביתר יכולת דרך ג׳ל שמחקה את הרקמה הסובבת. כאשר הפחיתו CST1, קצב הגדילה של התאים האט, התאים נעצרו בשלב מוקדם במחזור התא והיכולת שלהם לנוע ולחדור ירדה. בעכברים, גידולים שנוצרו להפרשה מופרזת של CST1 יצרו קשריות גדולות יותר בכבד וגרעו יותר גרורות בריאות, בעוד שגידולים עם CST1 מדוכא צמחו לאט יותר והתפשטו פחות. בסך הכל, הניסויים הללו מראים ש-CST1 אינו רק סימן היקפי, אלא מקדם פעיל של גדילה ופיזור הגידול.
כיבוי תהליך ההזדקנות התאית כדי להימלט מבלמים טבעיים
לתאים נורמליים יש מערכת בטיחות פנימית הנקראת סניסנס: כשמצטבר אצלם מספיק נזק, הם נכנסים למצב מנוחה קבוע ועוצרים להתחלק. זה פועל כמחסום מול סרטן. הצוות מצא שהפחתת CST1 בתאי הסרטן הופכת את מערכת הבטיחות הזו חזרה לפעילה. תאים עם CST1 מופחת הראו סימנים קלאסיים של סניסנס, כולל שינויים בצורה, פעילות מוגברת של אנזים קשור לסניסנס ושינויים בגורמי דלקת שהם מפרישים. באופן מפתיע, על אף ש-CST1 שינה גם את אופן הטיפול של התאים במולקולות קטנות המשמשות לבניית DNA, ניסיונות להציל את הגדילה על ידי אספקת אבני בניין נוספים נכשלו. זה מרמז שכוחו העיקרי של CST1 איננו בהזנת סינתזת ה‑DNA, אלא בעזרה לתאי הגידול לעקוף את תוכנית הסניסנס שהיה עוצר אותם.
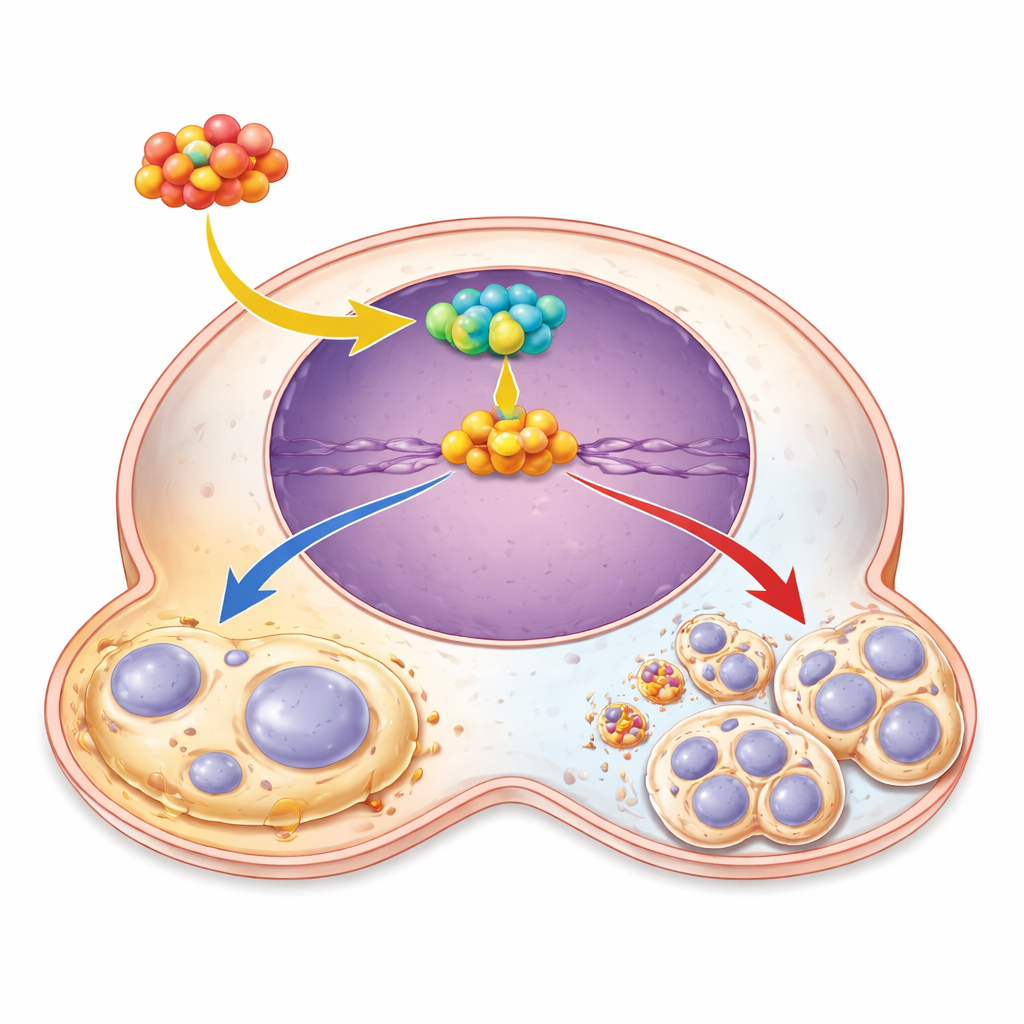
רצף אונקוגני: מ‑NFATC2 דרך CST1 אל SOX4
בהעמקה נוספת, החוקרים הרכיבו רצף מולקולרי בעל שלושה שלבים בתוך תאי הסרטן. בראש עומד NFATC2, פקטור שעתוק שנקשר ל‑DNA ומפעיל גנים מסוימים. הם הראו ש‑NFATC2 נקשר ישירות לאזור הבקרה של גן CST1 ומגביר את פעילותו. כשרמות NFATC2 היו גבוהות, CST1 עלה; כשדיכאו את NFATC2, רמות CST1 ירדו והתנהגויות מקדמות‑גידול נחלשו. במורד הזרם של CST1 זיהו שחקן מרכזי נוסף, פקטור השעתוק SOX4, שנקשר בעבר לעיכוב סניסנס בסרטנים אחרים. CST1 הגביר את רמות SOX4, וכאשר דיכאו CST1, הוספת SOX4 נוספת הספיקה לשחזר את גדילת התאים ולהפחית את אותות הסניסנס. זה מציב את SOX4 כביצועי העיקרי של השפעות ה‑anti‑aging והקידום‑גדילה של CST1.
מה המשמעות לטיפולים עתידיים
על‑ידי מיפוי הרצף NFATC2–CST1–SOX4, המחקר חושף כיצד תאי סרטן צינורות מרה מנטרלים את בלמי ההזדקנות הפנימיים שלהם, מה שמאפשר גדילה והתפשטות בלתי מבוקרות. עבור הקורא הרחב, המסר הוא שהגידולים האלה משתלטים על רשת קטנה של חלבונים כדי לשמור על התאים צעירים ומתחלקים תמיד. הפרעה לשרשרת זו בכל נקודה — חסימת שליטת NFATC2 על CST1, הפחתת CST1 עצמו או חסימת SOX4 — עשויה לשחזר את הנטייה הטבעית של התא להאט ולעצור. אמנם נדרשת עבודה נוספת לפני שהתובנות האלה יתורגמו לתרופות חדשות, אך CST1 בעיקרו מצטייר כמטרה מבטיחה לטיפולים וכסמן שעשוי לסייע בזיהוי מטופלים בסיכון גבוה יותר.
ציטוט: Zhao, W., Zhao, J., Li, K. et al. NFATC2-mediated CST1 upregulation drives cholangiocarcinoma growth and metastasis. Cell Death Discov. 12, 187 (2026). https://doi.org/10.1038/s41420-026-03036-8
מילות מפתח: כולנגיוקרצינומה, CST1, הזדקנות תאיית, מטסטזת סרטן, מסלול NFATC2 SOX4