Clear Sky Science · pl
Adaptacyjna wobec domeny głęboka sieć kontrastowa do klasyfikacji raka pęcherza moczowego napędzanej przez obrazowanie rezonansu magnetycznego
Dlaczego mądrzejsze badania obrazowe mają znaczenie
Rak pęcherza jest powszechny i może zagrażać życiu, ale nie wszystkie guzy pęcherza zachowują się tak samo. Niektóre pozostają na powierzchni ściany pęcherza, podczas gdy inne wnikają w mięsień i wymagają znacznie bardziej agresywnego leczenia. Lekarze korzystają z rezonansu magnetycznego (MRI), aby ocenić, jak głęboko urósł guz, jednak obrazy te bywają trudne do interpretacji i różnią się między szpitalami. W tym badaniu przedstawiono nowy system sztucznej inteligencji (AI) zaprojektowany, by odczytywać skany MRI pęcherza bardziej konsekwentnie i dokładnie, niezależnie od miejsca pozyskania obrazów.
Dwa rodzaje guzów, dwie bardzo różne ścieżki
Dla pacjentów kluczowe jest ustalenie, czy ich guz ogranicza się do wewnętrznej wyściółki pęcherza (bez naciekania mięśnia), czy też przeniknął warstwę mięśniową (naciekanie mięśnia). Odpowiedź determinuje wszystko — od rodzaju operacji po plany chemioterapii i radioterapii. Obecnie lekarze opierają decyzje na połączeniu endoskopii, pobrania próbki tkanki i badań obrazowych, ale skany MRI mogą pokazywać guzy o nieostrych granicach, nietypowych kształtach i niewielkich rozmiarach, co utrudnia ocenę. Dodatkowo aparaty od różnych producentów i z różnych szpitali generują obrazy o nieco odmiennym wyglądzie, co może zmylić standardowe modele komputerowe.
Budowa AI, która dobrze „podróżuje”
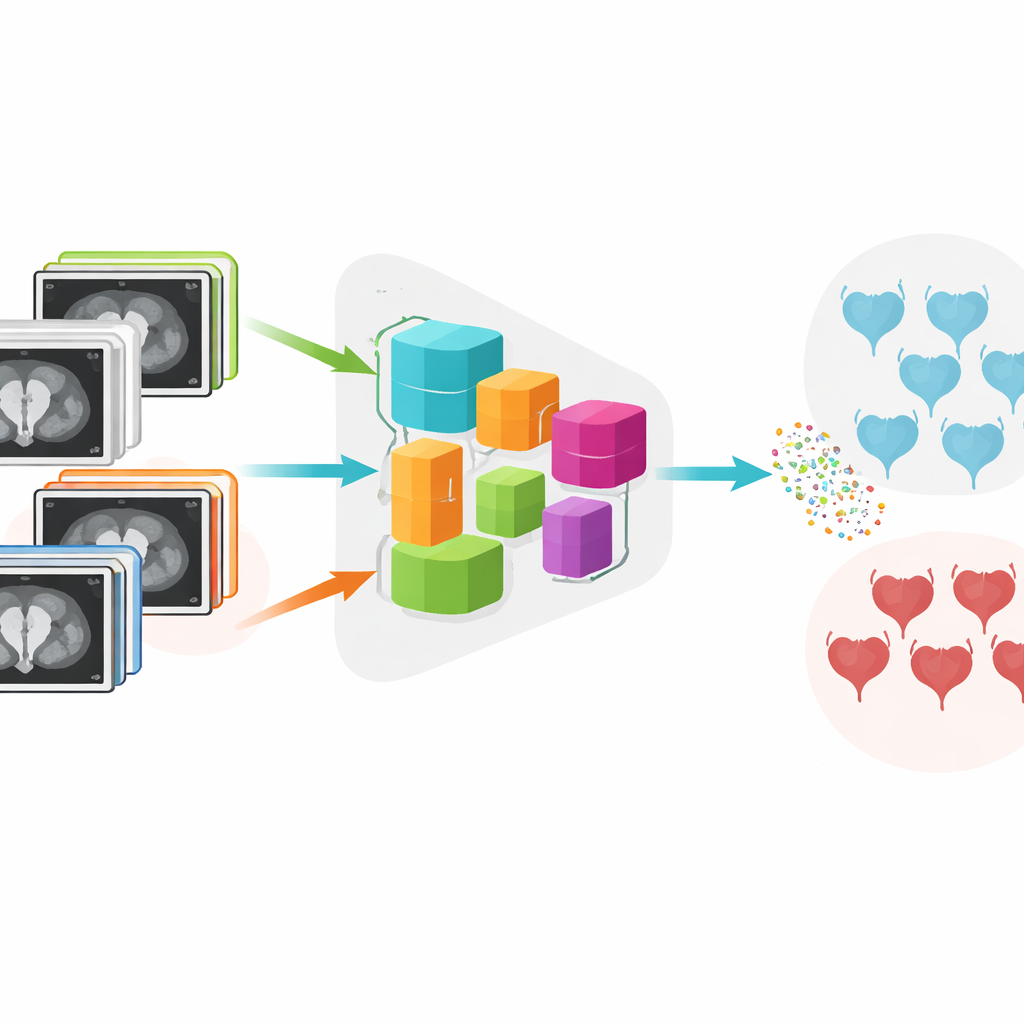
Autorzy opracowali system nazwany DADCNet, który próbuje pokonać te przeszkody. Trenowali go na skanach MRI od 279 pacjentów z rakiem pęcherza leczonych w czterech różnych ośrodkach medycznych, każdy używał innych marek i ustawień aparatów. Zamiast uczyć się tylko z jednego szpitala i potem testować w innym, sieć otrzymuje obrazy zarówno z „rodzimych” ośrodków, na których się uczy, jak i z „nowych” ośrodków, z którymi zetknie się później. W modelu etap ekstrakcji cech przekształca surowe obrazy w wzorce liczbowe, a specjalny moduł «adaptacji domeny» skłania te wzorce do ujednolicenia między szpitalami. Dzięki temu AI skupia się na medycznej treści obrazu zamiast na specyficznych cechach aparatu.
Nauczanie systemu rozróżniania
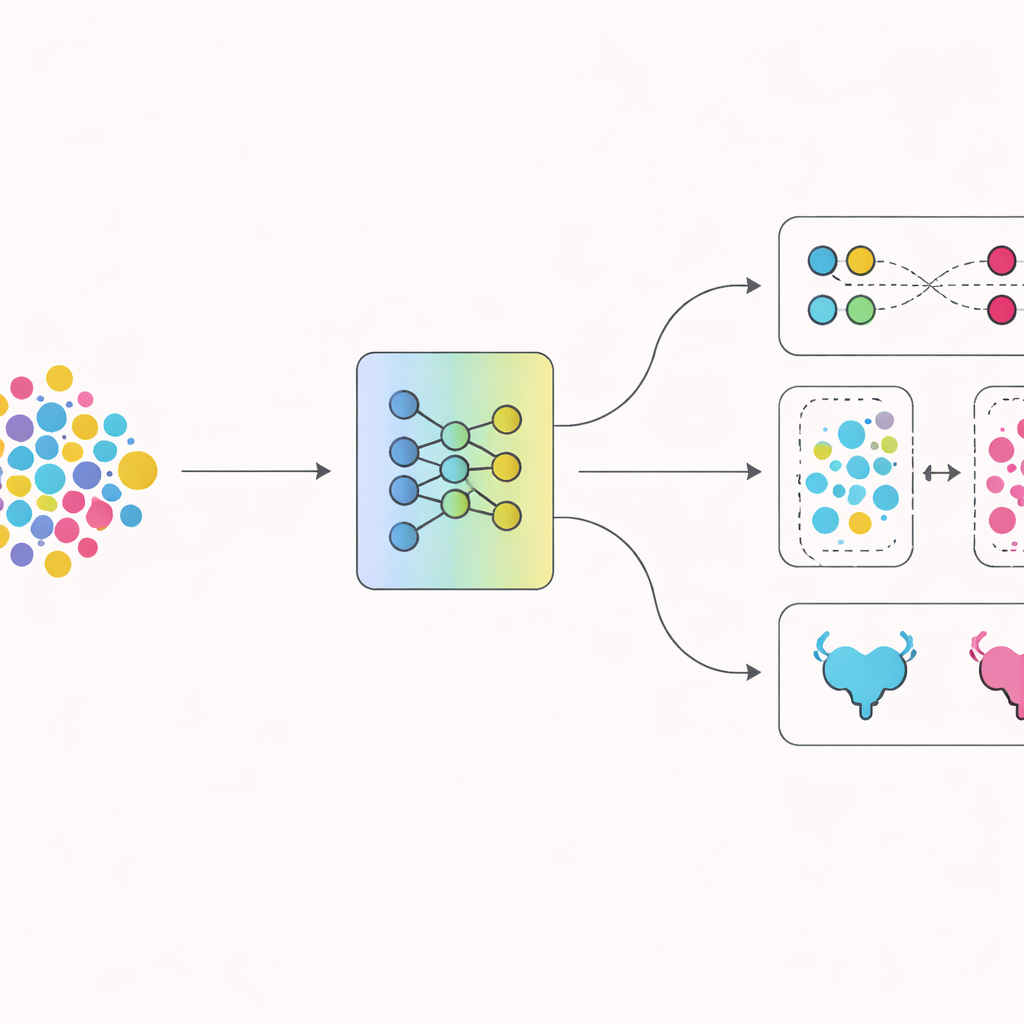
Drugą innowacją jest sposób, w jaki sieć jest trenowana, aby rozdzielać dwa typy choroby. Poza zwykłym nagradzaniem poprawnych odpowiedzi, autorzy wykorzystują technikę zachęcającą obrazy tego samego rodzaju guza do ciasnego grupowania w wewnętrznej przestrzeni modelu, jednocześnie odpychając obrazy różnych typów guzów. Z czasem to trening oparty na kontraście pomaga modelowi wyznaczyć czyściejszą granicę między rakiem nie naczynającym mięśnia a rakiem naciekającym mięsień. Narzędzia wizualizacyjne potwierdzają, że reprezentacje wewnętrzne obu grup, które początkowo były splątane, stopniowo rozdzielają się na odrębne klastry w miarę postępów treningu.
Sprawdzanie nowego podejścia w praktyce
Naukowcy porównali swój system z kilkoma dobrze znanymi modelami głębokiego uczenia powszechnie stosowanymi w obrazowaniu medycznym. W powtarzanych testach na różnych podziałach danych DADCNet osiągnął wyższą dokładność i lepszą równowagę między wykrywaniem guzów naciekających mięsień a unikaniem fałszywych alarmów. Gdy wyłączono elementy projektu — albo adaptację między ośrodkami, albo trening oparty na kontraście — wydajność spadała i stawała się mniej stabilna, co podkreśla znaczenie obu komponentów. Dodatkowe eksperymenty naśladujące rzeczywiste użycie, gdzie AI trenowano na danych z niektórych szpitali i testowano na zupełnie innym, pokazały, że DADCNet radzi sobie z takimi zmianami lepiej niż inne modele.
Wskazywanie, na co AI „patrzy”
Aby dać lekarzom pewność, zespół sprawdził, które regiony każdego skanu MRI sieć wykorzystuje przy formułowaniu prognoz. Mapy cieplne ujawniły, że model koncentruje się głównie na samym guzie i pobliskiej warstwie mięśniowej — tych samych obszarach, które radiolodzy badają, decydując, czy nowotwór przeniknął mięsień. Ta zgodność między uwagą człowieka a maszyny, wraz z wyraźnym rozdziałem typów guzów w wewnętrznej przestrzeni modelu, sugeruje, że system nie tylko zapamiętuje powierzchowne wzorce, lecz uczy się medycznie istotnych wskazówek.
Co to oznacza dla pacjentów
Mówiąc prosto, praca ta pokazuje, że starannie zaprojektowana AI może odczytywać skany MRI pęcherza z wysoką dokładnością, nawet gdy skany pochodzą z różnych szpitali i urządzeń. Ucząc się ignorować techniczne różnice między ośrodkami i uwydatniać kontrast między wczesną a zaawansowaną chorobą, DADCNet może wspierać lekarzy w podejmowaniu pewniejszych, bardziej spójnych decyzji dotyczących agresywności leczenia raka pęcherza. Chociaż potrzebne są większe badania i szersze testy, podejście to wskazuje drogę ku przyszłym narzędziom obrazowym, które dobrze «podróżują» między szpitalami i pomagają zapewnić pacjentom właściwy poziom opieki oparty na bardziej wiarygodnej ocenie skanów.
Cytowanie: Huang, J., Hu, H., Sun, M. et al. A domain-adaptive deep contrastive network for magnetic resonance imaging-driven bladder cancer classification. npj Digit. Med. 9, 305 (2026). https://doi.org/10.1038/s41746-026-02499-4
Słowa kluczowe: rak pęcherza MRI, rak pęcherza naciekający mięsień, AI w obrazowaniu medycznym, adaptacja domeny, uczenie kontrastowe