Clear Sky Science · fr
Un réseau contrastif profond adapté au domaine pour la classification du cancer de la vessie par imagerie par résonance magnétique
Pourquoi des scans plus intelligents comptent
Le cancer de la vessie est fréquent et peut mettre la vie en danger, mais toutes les tumeurs vésicales ne se comportent pas de la même façon. Certaines restent à la surface de la paroi vésicale, tandis que d’autres pénètrent dans le muscle et nécessitent un traitement beaucoup plus agressif. Les médecins utilisent l’imagerie par résonance magnétique (IRM) pour évaluer la profondeur de croissance d’une tumeur, mais ces images peuvent être difficiles à interpréter et varient d’un hôpital à l’autre. Cette étude présente un nouveau système d’intelligence artificielle (IA) conçu pour lire les scans IRM de la vessie de manière plus cohérente et précise, indépendamment du lieu de collecte des images.
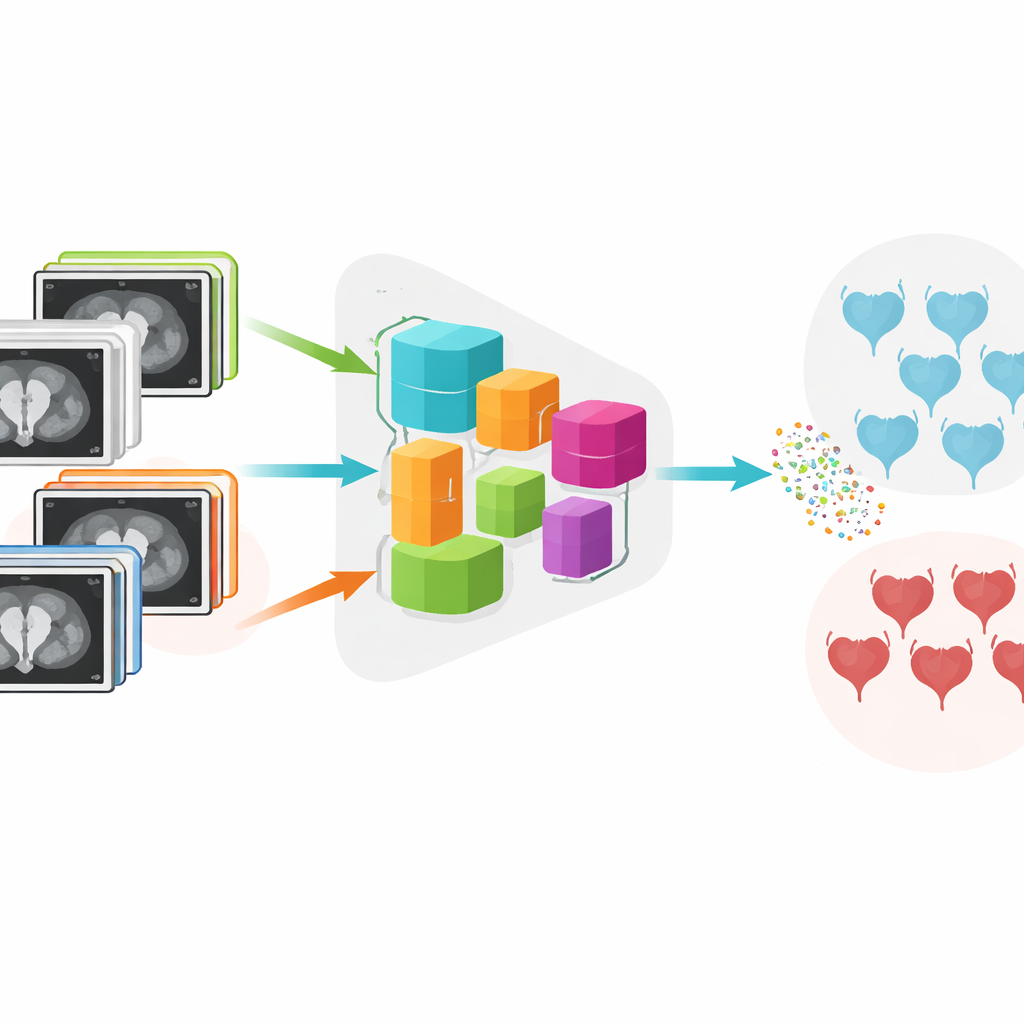
Deux types de tumeurs, deux trajectoires très différentes
Pour les patients, la question clé est de savoir si la tumeur est limitée à la muqueuse de la vessie (non envahissante le muscle) ou si elle a envahi la couche musculaire (envahissante le muscle). La réponse guide tout, du type de chirurgie aux protocoles de chimiothérapie et de radiothérapie. Aujourd’hui, les médecins s’appuient sur un mélange d’endoscopie, de prélèvements et d’imagerie pour décider, mais les scans IRM peuvent montrer des tumeurs aux contours flous, aux formes étranges et de petite taille, rendant l’évaluation difficile. De plus, les appareils de différents fabricants et hôpitaux produisent des images aux apparences légèrement différentes, ce qui peut embrouiller les modèles informatiques classiques.
Construire une IA qui voyage bien
Les auteurs ont développé un système appelé DADCNet qui tente de surmonter ces obstacles. Ils l’ont entraîné sur des scans IRM de 279 patients atteints d’un cancer de la vessie traités dans quatre centres médicaux différents, chacun utilisant des marques et des réglages d’appareils distincts. Plutôt que d’apprendre uniquement à partir d’un hôpital puis d’être testé sur un autre, le réseau reçoit des images à la fois des centres « d’origine » dont il apprend et des centres « nouveaux » qu’il rencontrera ensuite. À l’intérieur du modèle, une étape d’extraction de caractéristiques transforme les images brutes en motifs numériques, tandis qu’un module spécial d’« adaptation de domaine » pousse ces motifs à se ressembler entre les hôpitaux. Cela aide l’IA à se concentrer sur le contenu médical de l’image plutôt que sur les particularités de l’appareil.
Apprendre au système à voir des différences nettes
La deuxième innovation réside dans la manière dont le réseau est entraîné à séparer les deux types de maladie. Au-delà de simplement récompenser les bonnes réponses, les auteurs utilisent une technique qui encourage les images d’un même type de tumeur à se regrouper étroitement dans l’espace interne du modèle, tout en écartant les images des types de tumeur différents. Au fil du temps, cet entraînement fondé sur le contraste aide le modèle à tracer une frontière plus nette entre les cancers non envahissants le muscle et ceux envahissant le muscle. Des outils de visualisation confirment que les représentations internes des deux groupes, initialement mêlées, se séparent progressivement en grappes distinctes au cours de l’entraînement.
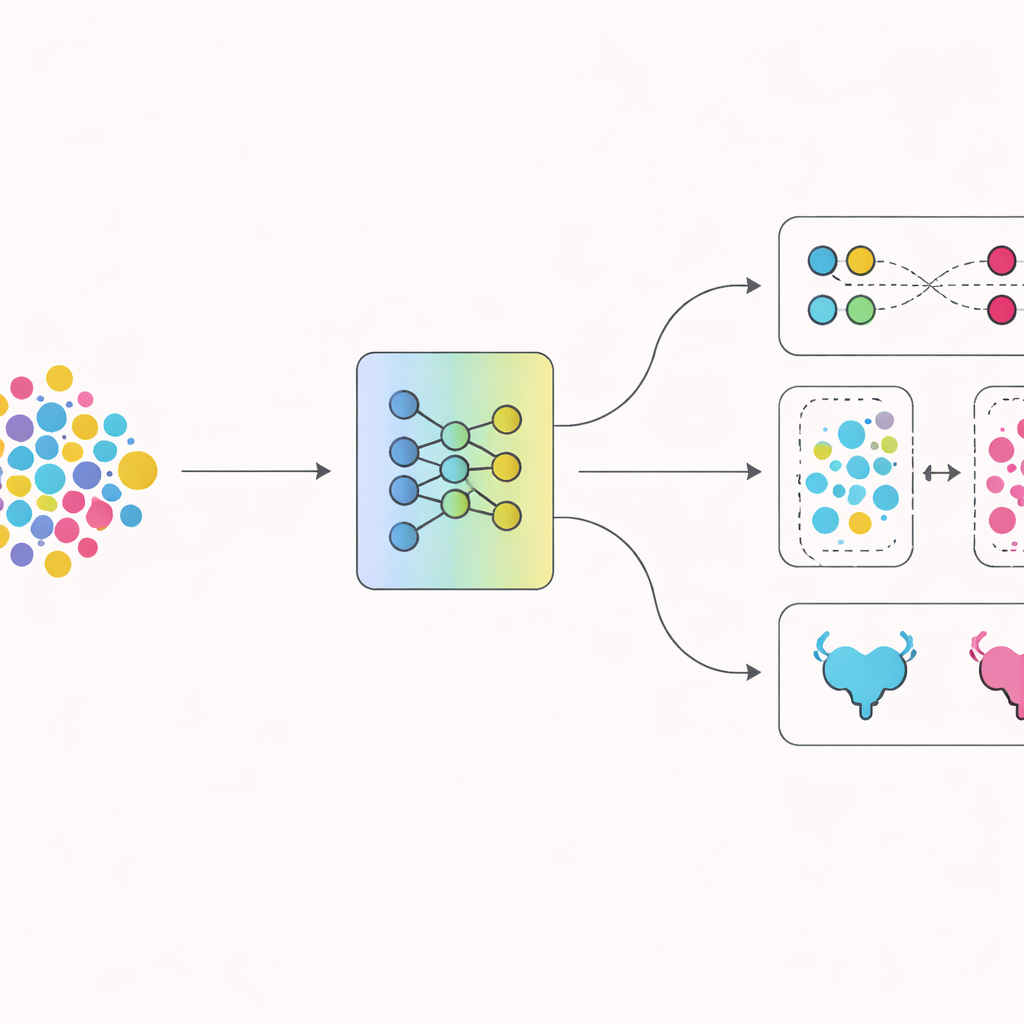
Mettre la nouvelle approche à l’épreuve
Les chercheurs ont comparé leur système à plusieurs modèles d’apprentissage profond bien connus et largement utilisés en imagerie médicale. À partir de tests répétés sur différentes divisions des données, DADCNet a atteint une plus grande précision et un meilleur équilibre entre la détection correcte des tumeurs envahissant le muscle et l’évitement des fausses alertes. Lorsque des composants du dispositif étaient désactivés — soit l’adaptation inter-centres, soit l’entraînement par contraste — les performances chutaient et devenaient moins stables, soulignant que les deux éléments étaient importants. Des expériences supplémentaires simulant une utilisation réelle, où l’IA est entraînée sur certains hôpitaux puis testée sur un hôpital complètement différent, ont montré que DADCNet gérait ces variations de manière plus robuste que d’autres modèles.
Voir où l’IA « regarde »
Pour rassurer les cliniciens, l’équipe a examiné quelles régions de chaque scan IRM le réseau utilise pour formuler ses prédictions. Des cartes thermiques ont révélé que le modèle se concentre principalement sur la tumeur elle-même et sur la couche musculaire adjacente — les mêmes zones que les radiologues inspectent pour décider si le cancer a envahi le muscle. Cet alignement entre l’attention humaine et celle de la machine, associé à la nette séparation des types de tumeurs dans l’espace interne du modèle, suggère que le système ne se contente pas de mémoriser des motifs superficiels mais apprend des indices d’intérêt médical.
Ce que cela signifie pour les patients
Concrètement, ce travail montre qu’une IA soigneusement conçue peut lire les scans IRM de la vessie avec une grande précision, même lorsque ces scans proviennent d’hôpitaux et d’appareils différents. En apprenant à ignorer les différences techniques entre les centres et à accentuer le contraste entre maladie précoce et maladie avancée, DADCNet pourrait aider les médecins à prendre des décisions plus sûres et plus cohérentes sur le degré d’agressivité du traitement du cancer de la vessie. Bien que des études plus larges et des tests plus étendus soient encore nécessaires, cette approche ouvre la voie à des outils d’imagerie qui se déplacent bien d’un hôpital à l’autre et contribuent à garantir que les patients reçoivent le niveau de soin approprié basé sur une lecture plus fiable de leurs scans.
Citation: Huang, J., Hu, H., Sun, M. et al. A domain-adaptive deep contrastive network for magnetic resonance imaging-driven bladder cancer classification. npj Digit. Med. 9, 305 (2026). https://doi.org/10.1038/s41746-026-02499-4
Mots-clés: IRM cancer de la vessie, cancer de la vessie envahissant le muscle, IA en imagerie médicale, adaptation de domaine, apprentissage contrastif