Clear Sky Science · nl
Een domeinaanpasbaar diep contrastnetwerk voor MRI-gestuurde classificatie van blaaskanker
Waarom slimere scans ertoe doen
Blaaskanker komt vaak voor en kan levensbedreigend zijn, maar niet alle blaastumoren gedragen zich op dezelfde manier. Sommige blijven aan de oppervlakte van de blaaswand, terwijl andere in de spier ingroeien en veel ingrijpender behandeling vereisen. Artsen gebruiken magnetische resonantiebeeldvorming (MRI) om te beoordelen hoe diep een tumor is gegroeid, maar deze beelden zijn moeilijk te interpreteren en variëren van ziekenhuis tot ziekenhuis. Deze studie introduceert een nieuw systeem voor kunstmatige intelligentie (AI) dat bedoeld is om blaasmri-scans consistenter en nauwkeuriger te lezen, ongeacht waar de beelden zijn gemaakt.
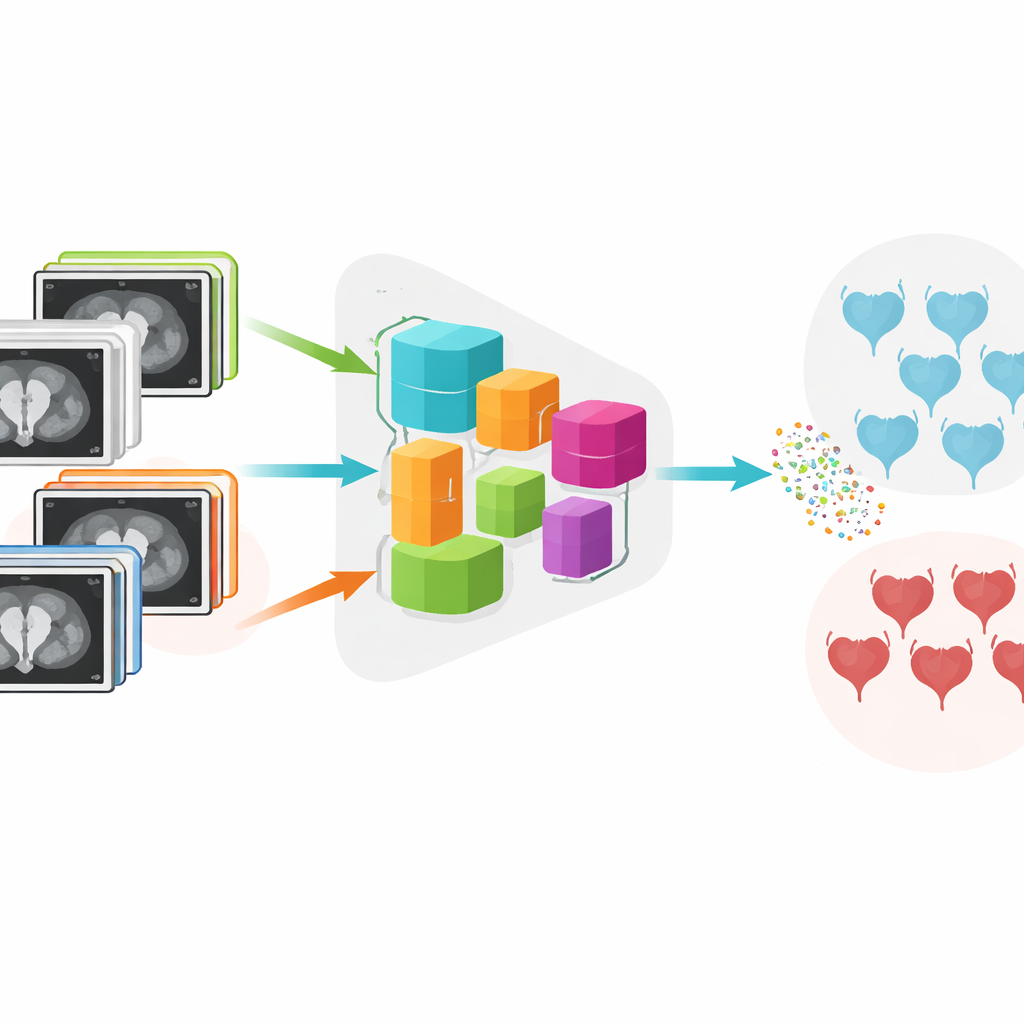
Twee soorten tumoren, twee heel verschillende trajecten
Voor patiënten is de kernvraag of de tumor beperkt blijft tot het binnenste slijmvlies van de blaas (niet-spierinvasief) of de spierlaag heeft doorgedrongen (spierinvasief). Het antwoord bepaalt vrijwel alles, van het type operatie tot chemotherapie- en bestralingsplannen. Tegenwoordig baseren artsen hun oordeel op een combinatie van endoscopie, weefselonderzoek en beeldvorming, maar MRI-scans kunnen tumoren met vage randen, onregelmatige vormen en kleine afmetingen tonen, wat de interpretatie bemoeilijkt. Daarbovenop produceren scanners van verschillende fabrikanten en ziekenhuizen beelden met licht afwijkende kenmerken, wat standaard computermodellen kan verwarren.
Een AI bouwen die goed reist
De auteurs ontwikkelden een systeem genaamd DADCNet dat probeert deze obstakels te overwinnen. Ze trainden het op MRI-scans van 279 blaaskankerpatiënten die in vier verschillende medische centra werden behandeld, elk met andere scannermerken en instellingen. In plaats van alleen te leren van één ziekenhuis en vervolgens op een ander te testen, krijgt het netwerk beelden van zowel de "thuis"-centra waarop het leert als de "nieuwe" centra die het later zal tegenkomen. In het model zet een fase voor feature-extractie de ruwe beelden om in numerieke patronen, terwijl een speciaal "domeinaanpassings"-module die patronen gelijkstroomt over ziekenhuizen. Dit helpt de AI zich te concentreren op de medische inhoud van het beeld in plaats van op eigenschappen van de scanner.
Het systeem leren duidelijke verschillen te zien
Een tweede innovatie ligt in hoe het netwerk wordt getraind om de twee ziektevormen te scheiden. Naast het eenvoudig belonen van correcte antwoorden gebruiken de auteurs een techniek die aanmoedigt dat beelden van hetzelfde type tumor dicht bij elkaar clusteren in de interne ruimte van het model, terwijl beelden van verschillende tumortypes uit elkaar worden geduwd. Na verloop van tijd helpt dit contrastgerichte trainen het model een scherpere grens te vormen tussen niet-spierinvasieve en spierinvasieve kankers. Visualisatietools bevestigen dat de interne representaties van de twee groepen, die aanvankelijk door elkaar liggen, zich tijdens de training geleidelijk in aparte clusters scheiden.
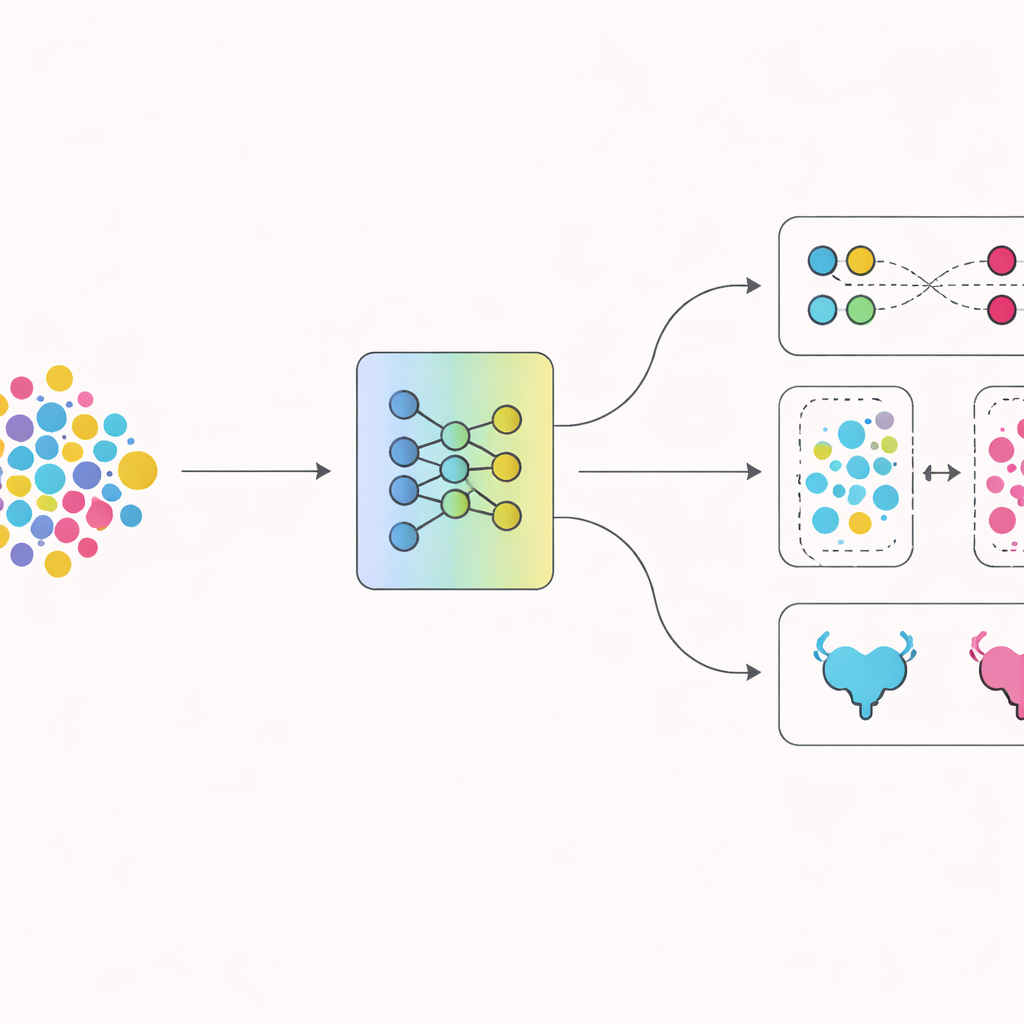
De nieuwe aanpak op de proef stellen
De onderzoekers vergeleken hun systeem met verschillende bekende deep-learningmodellen die veel worden gebruikt voor medische beeldvorming. Met herhaalde tests op verschillende verdelingen van de data behaalde DADCNet hogere nauwkeurigheid en een betere balans tussen het correct signaleren van spierinvasieve tumoren en het vermijden van valse alarmen. Wanneer delen van het ontwerp werden uitgeschakeld — ofwel de cross-center aanpassing ofwel de contrastgebaseerde training — daalde de prestatie en werd deze minder stabiel, wat aantoont dat beide onderdelen van belang zijn. Aanvullende experimenten die het echte gebruik nabootsen, waarbij de AI op sommige ziekenhuizen wordt getraind en op een totaal ander ziekenhuis wordt getest, toonden dat DADCNet deze verschuivingen beter aankan dan andere modellen.
Zien waar de AI "kijkt"
Om clinici gerust te stellen onderzocht het team welke regio's van elke MRI-scan het netwerk gebruikt bij zijn voorspellingen. Heatmaps toonden aan dat het model zich voornamelijk richt op de tumor zelf en de nabijgelegen spierlaag — dezelfde regio's die radiologen inspecteren om te beslissen of de kanker de spier is binnengedrongen. Deze afstemming tussen menselijke en machinale aandacht, samen met de duidelijke scheiding van tumortypes in de interne ruimte van het model, suggereert dat het systeem niet alleen oppervlakkige patronen memoriseert maar medische, betekenisvolle aanwijzingen leert.
Wat dit voor patiënten betekent
In eenvoudige bewoordingen laat dit werk zien dat zorgvuldige AI ontwerpen blaasmri-scans met hoge nauwkeurigheid kan lezen, zelfs wanneer die scans van verschillende ziekenhuizen en apparaten afkomstig zijn. Door te leren technische verschillen tussen centra te negeren en het contrast tussen vroeg en gevorderd ziektebeeld te verscherpen, kan DADCNet artsen ondersteunen bij het nemen van zelfverzekerdere, consistentere beslissingen over hoe agressief blaaskanker behandeld moet worden. Hoewel grotere studies en bredere tests nog nodig zijn, wijst deze aanpak op toekomstige beeldvormende hulpmiddelen die gemakkelijk van ziekenhuis naar ziekenhuis meegaan en helpen verzekeren dat patiënten het juiste zorgniveau krijgen op basis van een betrouwbaardere lezing van hun scans.
Bronvermelding: Huang, J., Hu, H., Sun, M. et al. A domain-adaptive deep contrastive network for magnetic resonance imaging-driven bladder cancer classification. npj Digit. Med. 9, 305 (2026). https://doi.org/10.1038/s41746-026-02499-4
Trefwoorden: blaaskanker MRI, spierinvasieve blaaskanker, AI voor medische beeldvorming, domeinaanpassing, contrastief leren