Clear Sky Science · pl
Badanie modelu nomogramu opartego na radiomice TK i cechach klinicznych dla klasyfikacji histologicznej guzów ślinianki przyusznej
Dlaczego to ma znaczenie dla pacjentów i lekarzy
Kiedy przy żuchwie pojawia się guz, zarówno pacjenci, jak i lekarze pilnie chcą wiedzieć: czy jest niegroźny czy niebezpieczny i jakie leczenie naprawdę jest potrzebne? W przypadku guzów ślinianki przyusznej, największej gruczołu ślinowego, odpowiedź zwykle pojawia się dopiero po operacji lub inwazyjnym badaniu igłowym. Badanie to sprawdza, czy informacje już ukryte w rutynowych skanach TK, połączone z prostymi danymi pacjenta, mogą z wyprzedzeniem rozróżniać te guzy na kluczowe typy, pomagając dostosować zabieg i unikać niepotrzebnego ryzyka.
Problem guzów gruczołowych o podobnym wyglądzie
Guzy ślinianki przyusznej są stosunkowo rzadkie, ale klinicznie istotne. Większość jest łagodna, szczególnie trzy częste typy: gruczolak wielopostaciowy, guz Warthina i gruczolak podstawnokomórkowy. Mniejszy odsetek to nowotwory złośliwe, wymagające bardziej agresywnej operacji i czasem radioterapii. Niestety wiele z tych guzów wygląda podobnie na standardowych badaniach obrazowych i często nie daje charakterystycznych objawów. Lekarze polegają na biopsji aspiracyjnej cienkoigłowej oraz własnej ocenie TK lub MRI, lecz biopsje bywają nieprzyjemne, czasem dają wyniki niejednoznaczne i niosą niewielkie ryzyko. To tworzy silną potrzebę lepszych, nieinwazyjnych narzędzi, które potrafią rozróżnić typy guzów przed zabiegiem.
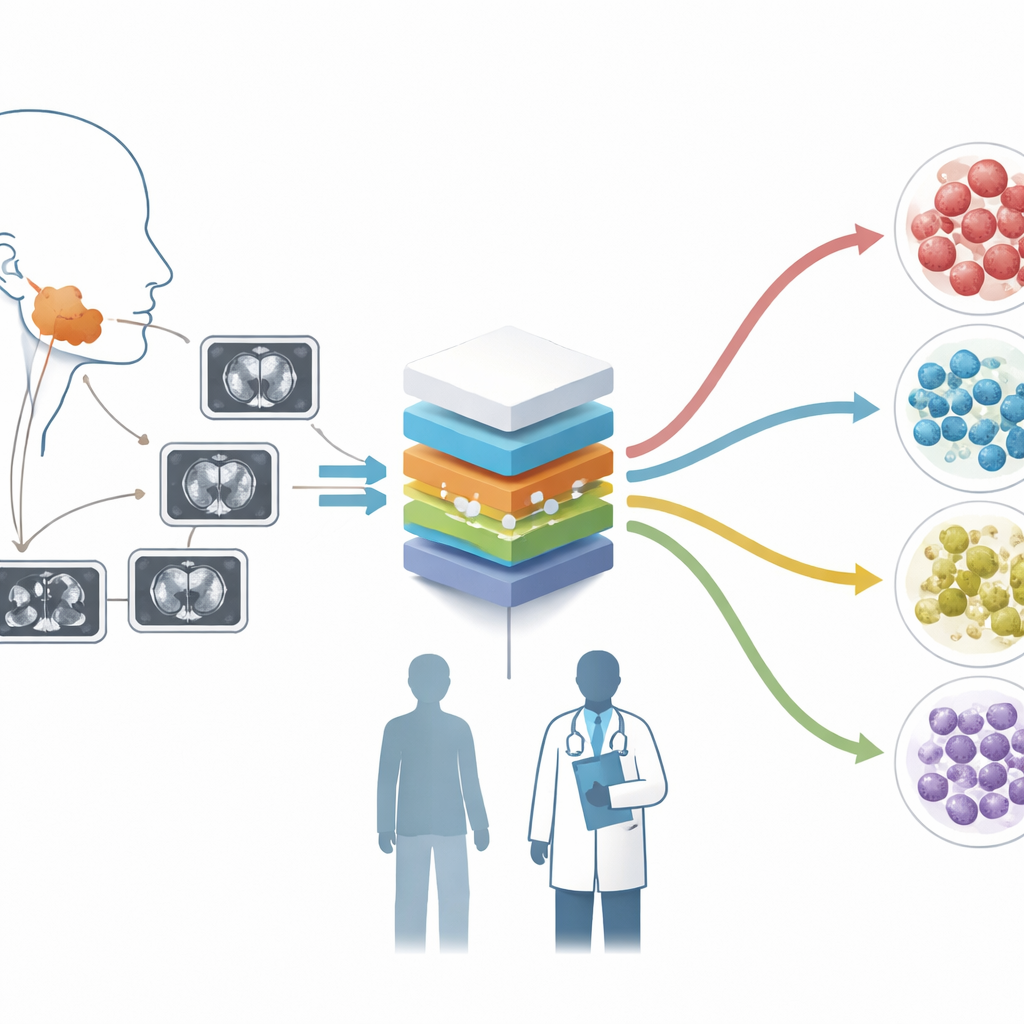
Przekształcanie badań TK w bogate mapy danych
Naukowcy zastosowali technikę zwaną radiomiką, która traktuje każdy skan TK jako bogate źródło danych, a nie tylko obraz. Z wzmocnionych obrazów TK 427 pacjentów z dwóch szpitali skrupulatnie odrysowali każdy guz i wprowadzili obrazy do specjalistycznego oprogramowania, które wydobywa ponad tysiąc cech numerycznych. Cechy te opisują wzory jasności, tekstury i kształtu, których oko ludzkie nie potrafi łatwo zmierzyć. Aby zapewnić wiarygodność danych pomiędzy różnymi skanerami, zespół przeskalował i znormalizował obrazy oraz zastosował statystyczną metodę ComBat do ujednolicenia cech pochodzących z różnych urządzeń.
Budowa inteligentnych modeli w trzech krokach decyzyjnych
Zamiast próbować klasyfikować wszystkie typy guzów jednocześnie, zespół rozłożył problem na trzy proste decyzje, które odzwierciedlają sposób myślenia klinicysty. Najpierw: łagodny czy złośliwy? Po drugie, wśród guzów łagodnych: czy to gruczolak wielopostaciowy w porównaniu z dwoma pozostałymi typami łącznie? Po trzecie, jeśli to jeden z tych dwóch, czy jest to guz Warthina czy gruczolak podstawnokomórkowy? Dla każdego kroku użyto metod uczenia maszynowego—regresji logistycznej, maszyn wektorów nośnych i drzew wzmacnianych gradientowo—aby znaleźć najbardziej informacyjne cechy radiomiczne i zbudować model predykcyjny. Modele oceniano pod kątem zdolności do rozdzielania grup, mierząc wydajność za pomocą pola pod krzywą ROC, standardowej miary dla testów diagnostycznych.
Łączenie wzorców obrazu z codziennymi wskazówkami klinicznymi
Choć radiomika uchwyciła subtelne szczegóły obrazu, autorzy docenili także wartość podstawowych informacji klinicznych. Ocenili cechy takie jak objawy, granice guza, powiększenie węzłów chłonnych, wiek, rozmiar guza i obszary torbielowate widoczne w TK. Za pomocą analizy statystycznej zidentyfikowali, które z tych czynników naprawdę przyczyniają się do rozróżnienia grup guzów. Następnie połączyli te predyktory kliniczne z „sygnaturą” radiomiczną w jedne narzędzie graficzne zwane nomogramem. Nomogram przekształca złożone wyniki modelu w łatwy w użyciu system punktowy, który może oszacować prawdopodobieństwo każdego typu guza dla konkretnego pacjenta.
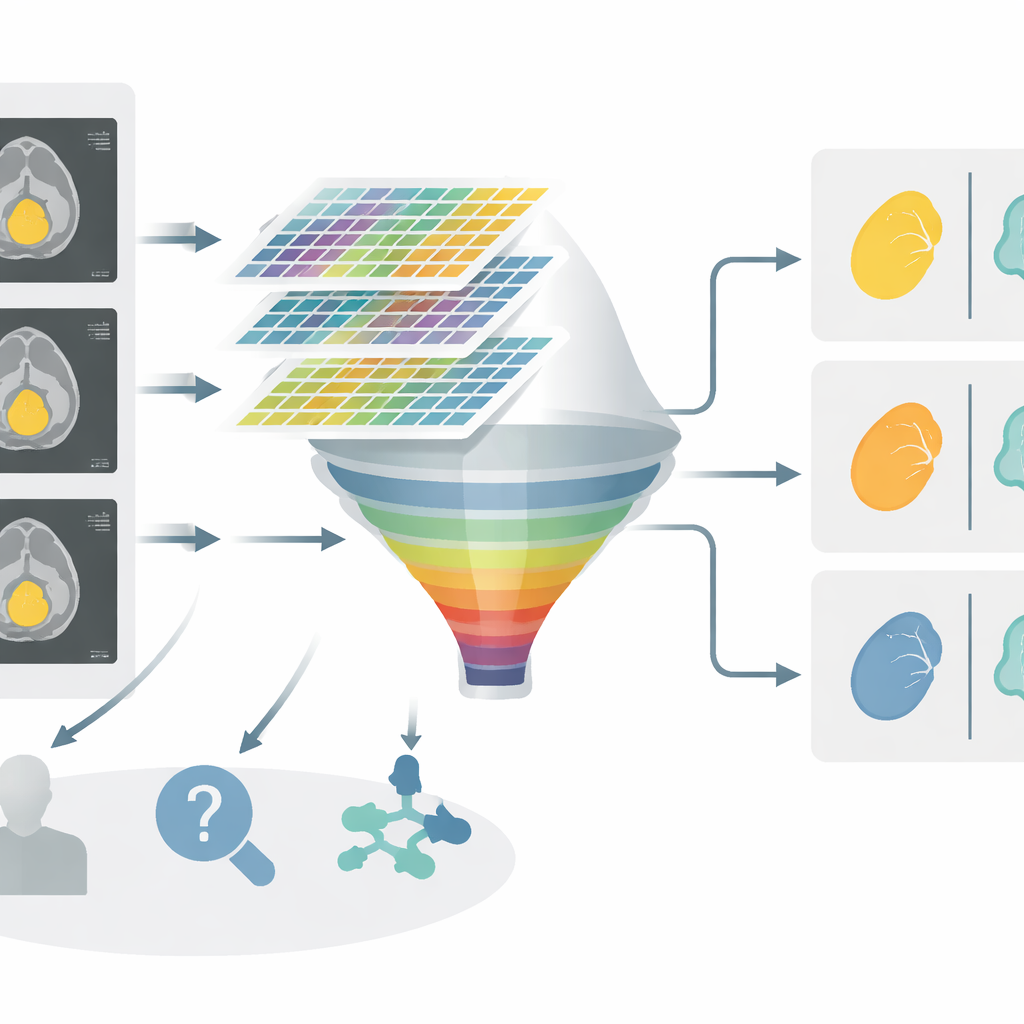
Co osiągnęło nowe narzędzie
We wszystkich trzech krokach decyzyjnych złożony nomogram przewyższał modele oparte wyłącznie na cechach klinicznych lub wyłącznie na radiomice. Na przykład przy rozróżnieniu guzów łagodnych i złośliwych zintegrowany model wykazał lepszą ogólną trafność i wyższy wynik diagnostyczny niż same czynniki kliniczne. Podobne ulepszenia zaobserwowano w dwóch porównaniach łagodny kontra łagodny, gdzie subtelne różnice są szczególnie trudne do zauważenia gołym okiem. Analiza krzywej decyzyjnej, która waży korzyści trafnej klasyfikacji przeciwko szkodom wynikającym z błędu, zasugerowała, że nomogram może oferować większy netto pożytek kliniczny w szerokim zakresie praktycznych progów decyzyjnych.
Co to oznacza na przyszłość
Mówiąc wprost, badanie pokazuje, że staranna analiza obrazów TK, połączona z rutynowo zbieranymi danymi pacjenta, może pomóc lekarzom pewniej klasyfikować guzy ślinianki przyusznej do znaczących kategorii przed operacją. Narzędzie nie zastępuje biopsji ani fachowej oceny, ale może ukierunkować decyzje dotyczące stopnia rozległości zabiegu i wskazać pacjentów, którzy mogą bezpiecznie uniknąć nadmiernie agresywnego leczenia. Przy większych, wieloośrodkowych badaniach i włączeniu innych rodzajów obrazowania, takie nomogramy oparte na radiomice mogą stać się praktyczną częścią codziennej opieki, wprowadzając bardziej spersonalizowaną i mniej inwazyjną diagnostykę dla osób z guzami gruczołów ślinowych.
Cytowanie: Shen, Q., Liu, Y., Xu, F. et al. The study of nomogram model based on CT radiomics and clinical features for histological classification of parotid gland tumors. Sci Rep 16, 11665 (2026). https://doi.org/10.1038/s41598-026-46970-4
Słowa kluczowe: guzy ślinianki przyusznej, radiomika TK, diagnoza przy użyciu uczenia maszynowego, klasyfikacja guzów, obrazowanie nieinwazyjne