Clear Sky Science · nl
De studie van een nomogrammodel gebaseerd op CT-radiomics en klinische kenmerken voor histologische classificatie van tumoren van de oorspeekselklier
Waarom dit belangrijk is voor patiënten en artsen
Wanneer er een zwelling nabij de kaak verschijnt, willen zowel patiënten als artsen snel weten: is het onschuldig of gevaarlijk, en welke behandeling is echt nodig? Bij tumoren van de oorspeekselklier, de grootste speekselklier, komt het antwoord meestal pas na een operatie of een invasieve naaldbiopsie. Deze studie onderzoekt of informatie die al verborgen ligt in routinematige CT-scans, gecombineerd met eenvoudige patiëntgegevens, deze tumoren van tevoren in belangrijke types kan indelen, zodat operaties beter kunnen worden afgestemd en onnodige risico’s vermeden worden.
Het probleem van gelijkende klierzwellingen
Tumoren van de oorspeekselklier zijn relatief zeldzaam maar klinisch relevant. De meeste zijn goedaardig, vooral drie veelvoorkomende typen: pleomorfe adenoom, Warthin-tumor en basaalceladenoom. Een kleiner deel is kwaadaardig en vereist agressievere chirurgie en soms bestraling. Helaas lijken veel van deze tumoren op standaardbeeldvorming erg op elkaar en hebben ze vaak geen onderscheidende symptomen. Artsen vertrouwen op fijnnaaldbiopsieën en hun eigen beoordeling van CT- of MRI-scans, maar biopsieën kunnen ongemakkelijk zijn, soms geen definitief resultaat geven en kleine risico’s hebben. Dit vergroot de noodzaak voor betere, niet-invasieve hulpmiddelen die tumortypen vóór de operatie kunnen onderscheiden.
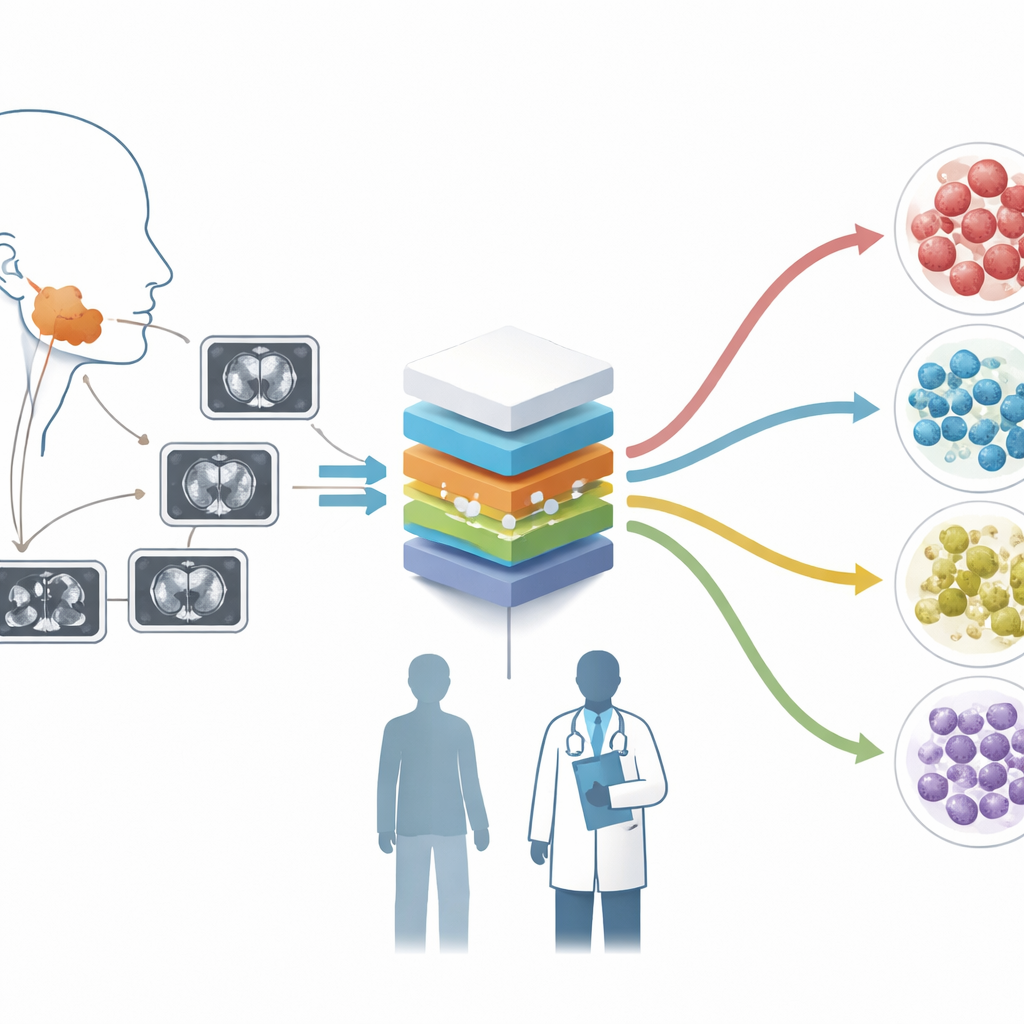
CT-scans omzetten in rijke datakaarten
De onderzoekers gebruikten een techniek die radiomics heet, waarmee elke CT-scan wordt behandeld als een rijke gegevensbron in plaats van alleen een afbeelding. Uit versterkte CT-beelden van 427 patiënten in twee ziekenhuizen hebben zij zorgvuldig elke tumor afgebakend en de beelden ingevoerd in gespecialiseerde software die meer dan duizend numerieke kenmerken extraheert. Deze kenmerken beschrijven patronen van helderheid, textuur en vorm die met het blote oog moeilijk te kwantificeren zijn. Om de data betrouwbaar te maken over verschillende scanners heen, hebben de onderzoekers de beelden herverschaald en genormaliseerd en een statistische methode genaamd ComBat gebruikt om kenmerken van meerdere apparatuur te harmoniseren.
Slimme modellen bouwen in drie beslissingsstappen
In plaats van te proberen alle tumortypen in één keer te classificeren, verdeelde het team het probleem in drie eenvoudige beslissingen die lijken op het denkproces van een clinicus. Eerst: goedaardig of kwaadaardig? Ten tweede, onder goedaardige tumoren: is het een pleomorf adenoom versus de twee andere typen samen? Ten derde, als het één van die twee is: is het een Warthin-tumor of een basaalceladenoom? Voor elke stap gebruikte men methoden van machinaal leren—logistische regressie, support vector machines en gradient-boosted trees—om de meest informatieve radiomicskenmerken te vinden en een voorspellend model te bouwen. Ze evalueerden deze modellen op hoe goed ze de groepen scheidden, gemeten met de area under the ROC-curve, een standaardmaat voor diagnostische testen.
Beeldpatronen mengen met alledaagse klinische aanwijzingen
Hoewel radiomics subtiele beelddetails vastlegde, erkenden de auteurs ook de waarde van eenvoudige klinische informatie. Ze beoordeelden kenmerken zoals symptomen, tumorrand, lymfekliervergroting, leeftijd, tumorgrootte en cyste-achtige gebieden op CT. Met statistische analyse identificeerden ze welke van deze factoren werkelijk bijdroegen aan het onderscheiden van de tumorgroepen. Vervolgens combineerden ze deze klinische voorspellers met de radiomics-«handtekening» in één grafisch hulpmiddel, een nomogram. Dit nomogram zet complexe modeluitkomsten om in een eenvoudig te gebruiken puntensysteem dat de kans op elk tumortype voor een individuele patiënt kan inschatten.
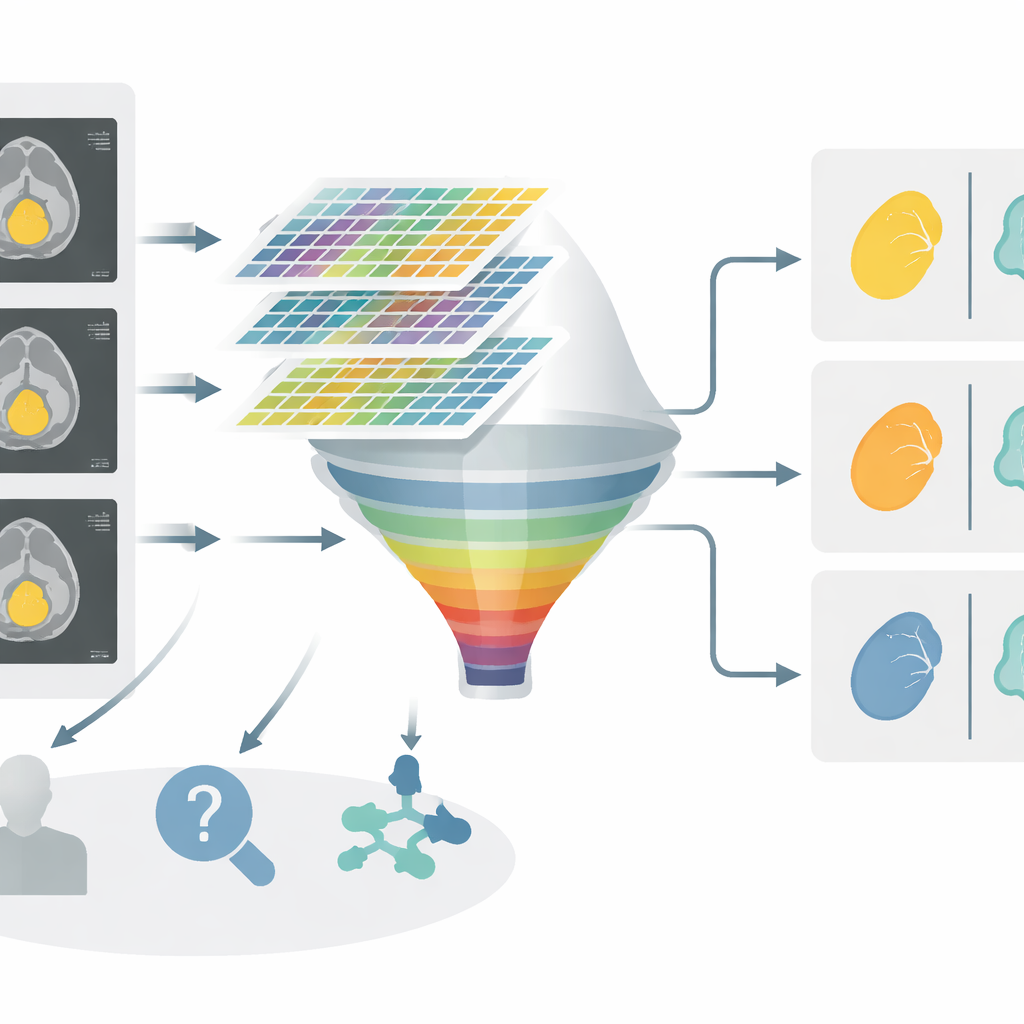
Wat het nieuwe hulpmiddel bereikte
Over alle drie de beslissingsstappen presteerde het gecombineerde nomogram beter dan modellen die alleen klinische kenmerken of alleen radiomics gebruikten. Bijvoorbeeld bij het scheiden van goedaardige en kwaadaardige tumoren toonde het geïntegreerde model een betere algehele nauwkeurigheid en een hogere diagnostische score dan alleen klinische factoren. Vergelijkbare verbeteringen deden zich voor in de twee goedaardig-tegen-goedaardig vergelijkingen, waarin subtiele verschillen met het blote oog bijzonder moeilijk te zien zijn. Decision-curve-analyse, die de voordelen van juiste classificatie afweegt tegen de nadelen van fouten, suggereerde dat het nomogram over een breed scala aan klinische beslissingsdrempels meer netto klinisch voordeel kan bieden.
Wat dit betekent voor de toekomst
Kort gezegd laat de studie zien dat zorgvuldige analyse van CT-beelden, gecombineerd met routinematig verzamelde patiëntgegevens, artsen kan helpen parotistumoren vóór de operatie betrouwbaarder in betekenisvolle categorieën in te delen. Het hulpmiddel vervangt geen biopsie of deskundig oordeel, maar het kan de besluitvorming over hoe ingrijpend een operatie moet zijn sturen en aangeven welke patiënten mogelijk veilig een te agressieve behandeling kunnen vermijden. Met grotere, multicenter-studies en de opname van andere beeldvormende modaliteiten kunnen dergelijke radiomics-gebaseerde nomogrammen een praktisch onderdeel van de dagelijkse zorg worden, en zo meer gepersonaliseerde en minder invasieve diagnostiek bieden aan mensen met speekselkliertumoren.
Bronvermelding: Shen, Q., Liu, Y., Xu, F. et al. The study of nomogram model based on CT radiomics and clinical features for histological classification of parotid gland tumors. Sci Rep 16, 11665 (2026). https://doi.org/10.1038/s41598-026-46970-4
Trefwoorden: tumoren van de oorspeekselklier, CT-radiomics, machinaal leren diagnose, tumorklassificatie, niet-invasieve beeldvorming