Clear Sky Science · pl
Charakteryzacja, fenotypowanie komórek układu odpornościowego i analiza różnicowej ekspresji genów przerzutów do mózgu oraz pierwotnych próbek raka piersi
Dlaczego rozsiew raka piersi do mózgu ma znaczenie
W miarę poprawy metod leczenia raka piersi wiele kobiet żyje dłużej — ale dodatkowy czas ujawnia poważny problem. Coraz więcej pacjentek rozwija guzy w mózgu, zwane przerzutami do mózgu, które są trudne w leczeniu i często prowadzą do ciężkich objawów. W tym badaniu postawiono proste, lecz kluczowe pytanie: na ile te guzy mózgowe różnią się od pierwotnych guzów piersi, z których pochodzą, szczególnie pod względem interakcji z układem odpornościowym? Odpowiedzi mogą wpłynąć na przyszłe terapie jednej z najbardziej obawianych komplikacji raka piersi. 
Badanie skojarzone — para próbek od tej samej pacjentki
Naukowcy przeanalizowali próbki guzów od dziesięciu kobiet, u których usunięto zarówno pierwotny guz piersi, jak i przerzut do mózgu. Takie podejście skojarzone pozwoliło porównać, dla każdej pacjentki, jak nowotwór zmienił się w czasie i po leczeniu. Zastosowano kilka technik laboratoryjnych: tradycyjne barwienia do oceny kluczowych białek decydujących o terapii; pomiary komórek odpornościowych wewnątrz i wokół guza; oraz nowoczesne sekwencjonowanie RNA, by odczytać, które geny są włączone lub wyłączone. Razem te metody dały wielowarstwowy obraz zarówno komórek nowotworowych, jak i otaczającej ich „sąsiedztwa” immunologicznego.
Przemiany tożsamości komórek guza
Jednym z głównych odkryć było to, że tożsamość raka, rozumiana klinicznie, może ulec zmianie po dotarciu do mózgu. U czterech z dziesięciu pacjentek przerzut mózgowy nie odpowiadał już pierwotnemu guzowi piersi w istotnych markerach, takich jak receptor estrogenowy czy HER2. W niektórych przypadkach guzy utraciły wrażliwość na hormony; w innych zmiany obejmowały zyskanie HER2 — modyfikację, która może otworzyć lub zamknąć opcje leczenia celowanego. Przy klasyfikacji opartej na profilu genowym, bardziej globalnym sposobie kategoryzacji raków piersi, również zaobserwowano przesunięcia podtypów między rakiem piersi a przerzutem w mózgu. Te zmiany podkreślają, że poleganie wyłącznie na cechach pierwotnego guza przy podejmowaniu decyzji terapeutycznych może pominąć kluczowe informacje po rozsiewie choroby.
Immunologiczne krajobrazy, które stają się chłodniejsze
Najbardziej uderzający kontrast pojawił się w mikrośrodowisku immunologicznym. Na podstawie danych RNA zespół oszacował, jakie typy komórek odpornościowych występowały w każdej próbce. Guzy pierwotne piersi częściej zawierały więcej komórek B, komórek plazmatycznych oraz limfocytów CD8 („zabójczych” T) — komórek zwykle związanych ze zdolnością organizmu do rozpoznawania i atakowania nowotworu. W przerzutach do mózgu te pomocne komórki były znacznie rzadsze. Zamiast nich zaobserwowano względny wzrost komórek powiązanych ze stłumionym lub „ropokojowym” stanem immunologicznym, takich jak makrofagi typu M2 i niektóre subpopulacje pomocniczych limfocytów T. Ten wzorzec sugeruje, że gdy komórki raka piersi osiedlają się w mózgu, wchodzą w środowisko — lub je współtworzą — które osłabia atak immunologiczny. 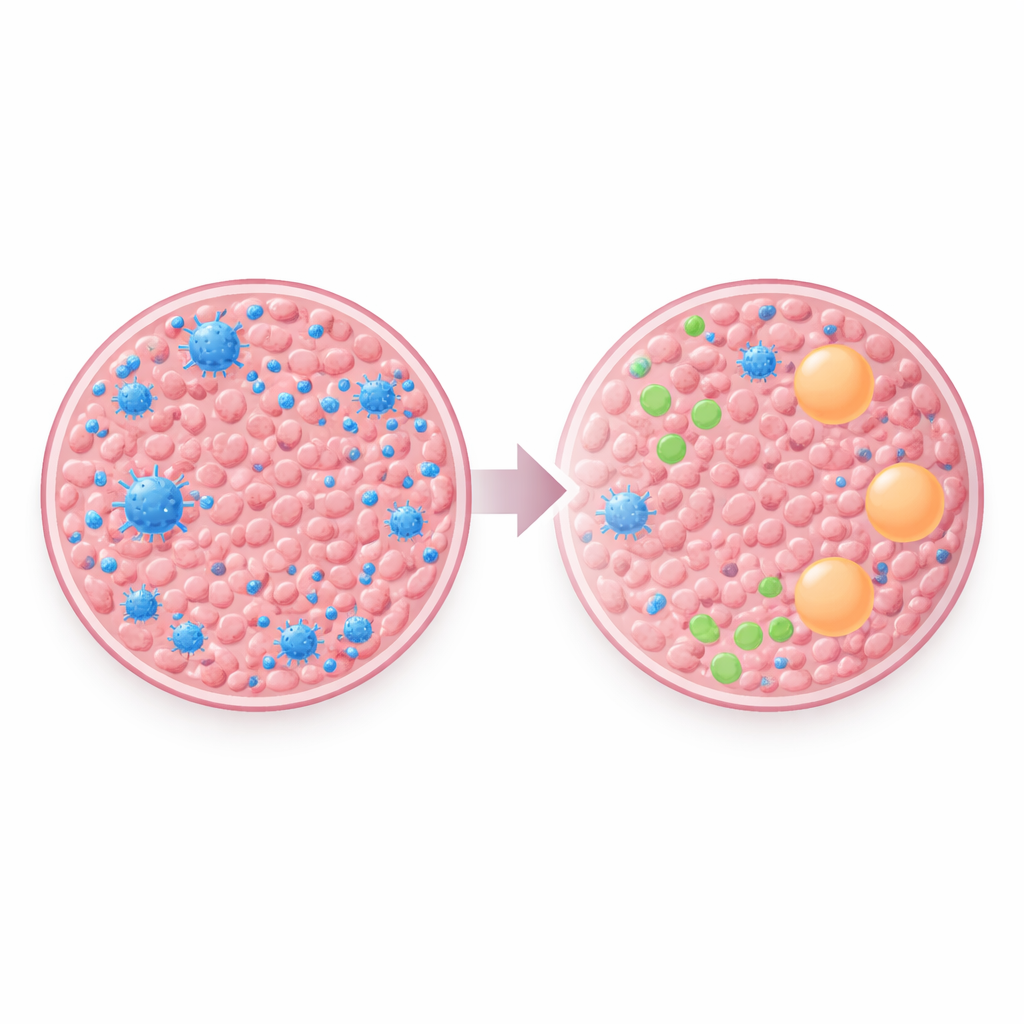
Zmiany w zużyciu energii i sygnalizacji
Wzorce aktywności genów opowiedziały kolejną historię. W pierwotnych guzach piersi najaktywniejsze grupy genów wiązały się z sygnałami immunologicznymi i zapalnymi, co korespondowało z bogatszą obecnością komórek walczących z nowotworem. W przerzutach do mózgu natomiast bardziej widoczne były geny związane z produkcją energii komórkowej — na przykład kierujące szlakami mitochondrialnymi. Choć badanie nie badało bezpośrednio metabolizmu, to przesunięcie sugeruje, że przerzuty mózgowe mogą przebudować sposób pozyskiwania energii, być może dostosowując się do unikalnego środowiska mózgu lub wspierając wzrost pod presją immunologiczną.
Co to oznacza dla przyszłych terapii
Dla laika wyniki te pomagają wyjaśnić, dlaczego obecne immunoterapie, takie jak leki „puszczające hamulce” układu odpornościowego, nie przyniosły jak dotąd spektakularnych efektów w raku piersi z przerzutami do mózgu. Guzy tam obecne wydają się funkcjonować w bardziej immunologicznie „cichym”, a nawet aktywnie immunosupresyjnym, niszowym środowisku z mniejszą liczbą komórek, od których zależą te terapie. Ponieważ badanie objęło jedynie dziesięć pacjentek i miało głównie obserwacyjny charakter, wnioski są wstępne. Mimo to silnie sugerują, że przerzuty raka piersi w mózgu nie są prostymi kopiami guzów pierwotnych: różnią się w kluczowych markerach, w sposobie komunikacji z układem odpornościowym i prawdopodobnie w sposobie zasilania. Zrozumienie i celowanie w ten zmieniony krajobraz będzie niezbędne do projektowania przyszłych terapii naprawdę chroniących mózg.
Cytowanie: Gassner, F.J., Rinnerthaler, G., Castagnaviz, V. et al. Characterization, immune cell phenotyping and differential gene expression analysis of brain metastases and primary breast cancer samples. Sci Rep 16, 10721 (2026). https://doi.org/10.1038/s41598-026-45607-w
Słowa kluczowe: przerzuty raka piersi do mózgu, mikrośrodowisko guza, uchylanie się od odpowiedzi immunologicznej, oporność na immunoterapię, sekwencjonowanie RNA