Clear Sky Science · pl
Zielona mikrosynteza heterozłącza CuO/ZnO przy użyciu Aspergillus terreus oraz jego aktywność przeciwbakteryjna i przeciw-wirulentnościowa wobec wielolekoopornego Escherichia coli
Dlaczego uporczywe zakażenia dotyczą nas wszystkich
Wiele powszechnych zakażeń, które kiedyś ustępowały po krótkim leczeniu antybiotykami, staje się coraz trudniejszych, a niekiedy niemożliwych do wyleczenia. Głównym sprawcą jest wielolekooporny Escherichia coli, rodzaj bakterii jelitowej, która może powodować bolesne zakażenia ran, dróg moczowych i krwi. W tym badaniu zbadano nietypowego sojusznika w walce z takimi superbakteriami: niegroźny grzyb glebowy, który pomaga wytwarzać maleńkie cząstki metalu zdolne nie tylko zabijać odporne szczepy E. coli, ale też osłabiać ich zdolność do wywoływania choroby.
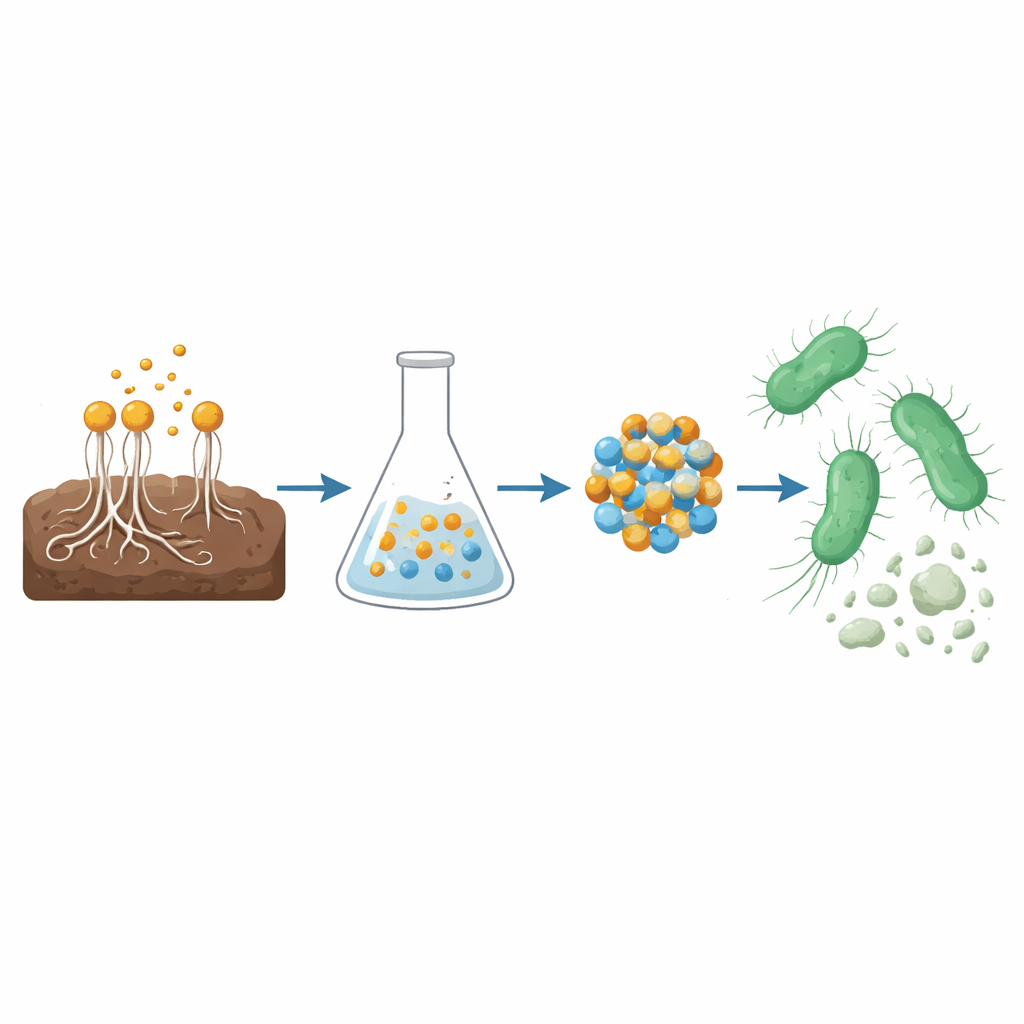
Grzyb działający jak mikrofabryka
Naukowcy zaczęli od gleby rolnej, poszukując grzyba, który mógłby pełnić rolę naturalnego warsztatu nanotechnologicznego. Wyizolowali i zidentyfikowali szczep Aspergillus terreus, grzyba strzępkowego znanego z wydzielania koktajlu związków organicznych, takich jak kwasy fenolowe i flawonoidy. Przy użyciu zaawansowanych analiz chemicznych potwierdzili, że bulion grzybowy zawiera związki takie jak kwas galusowy, kwas ferulowy i apigeninę. Substancje te mogą oddawać elektrony i przylegać do powierzchni metali, co czyni je idealnymi do przekształcania rozpuszczonych soli metali w stabilne, nanoskopijne cząstki bez użycia ostrych chemikaliów czy wysokoenergetycznych procesów przemysłowych.
Budowa dwumetalowej tarczy przeciw bakteriom
Zamiast jednego metalu zespół badawczy połączył miedź i cynk, tworząc nanokompozyt CuO/ZnO. W praktyce zmieszali filtrat grzybowy z roztworami octanów miedzi i cynku. Naturalne molekuły z grzyba przyłączały się do jonów miedzi i cynku, redukowały je i kierowały formowaniem niezwykle małych kryształków obu tlenków metali. Po ogrzewaniu w celu usunięcia pozostałości materiału organicznego powstał heterozłączeniowy nanokompozyt — przeplatające się cząstki tlenku miedzi i tlenku cynku o średnicy około 45 nanometrów, tysiące razy cieńsze niż ludzki włos. Mikroskopia i spektroskopia potwierdziły obecność obu tlenków, ich dobrą formę i ciasne połączenie, strukturę znaną z tego, że zwiększa generowanie wysoko reaktywnych rodników zawierających tlen.
Konfrontacja z rzeczywistym superbakterium
Aby sprawdzić, czy te zielono powstałe cząstki poradzą sobie z realnym zagrożeniem medycznym, naukowcy wyizolowali szczep E. coli z zakażeń ran w irackich szpitalach i wykazali, że oporny jest na wszystkie testowane antybiotyki. Sam filtrat grzybowy nie hamował wzrostu bakterii. W przeciwieństwie do niego nanokompozyt CuO/ZnO powodował wyraźne strefy zahamowania wzrostu na płytkach hodowlanych i blokował namnażanie bakterii przy stosunkowo niskich stężeniach w testach płynnych. Z upływem czasu cząstki zmniejszały liczbę żywych bakterii o kilka rzędów wielkości, szczególnie przy wyższych dawkach, co wskazuje na rzeczywiste zabijanie, a nie tylko spowolnienie wzrostu. Efekty te przypisuje się kilku współdziałającym mechanizmom: cząstki przywierają do powierzchni bakterii, uszkadzają jej osłonę, uwalniają jony miedzi i cynku zakłócające kluczowe enzymy oraz wspomagają powstawanie reaktywnych form tlenu, które uszkadzają lipidy, białka i DNA.
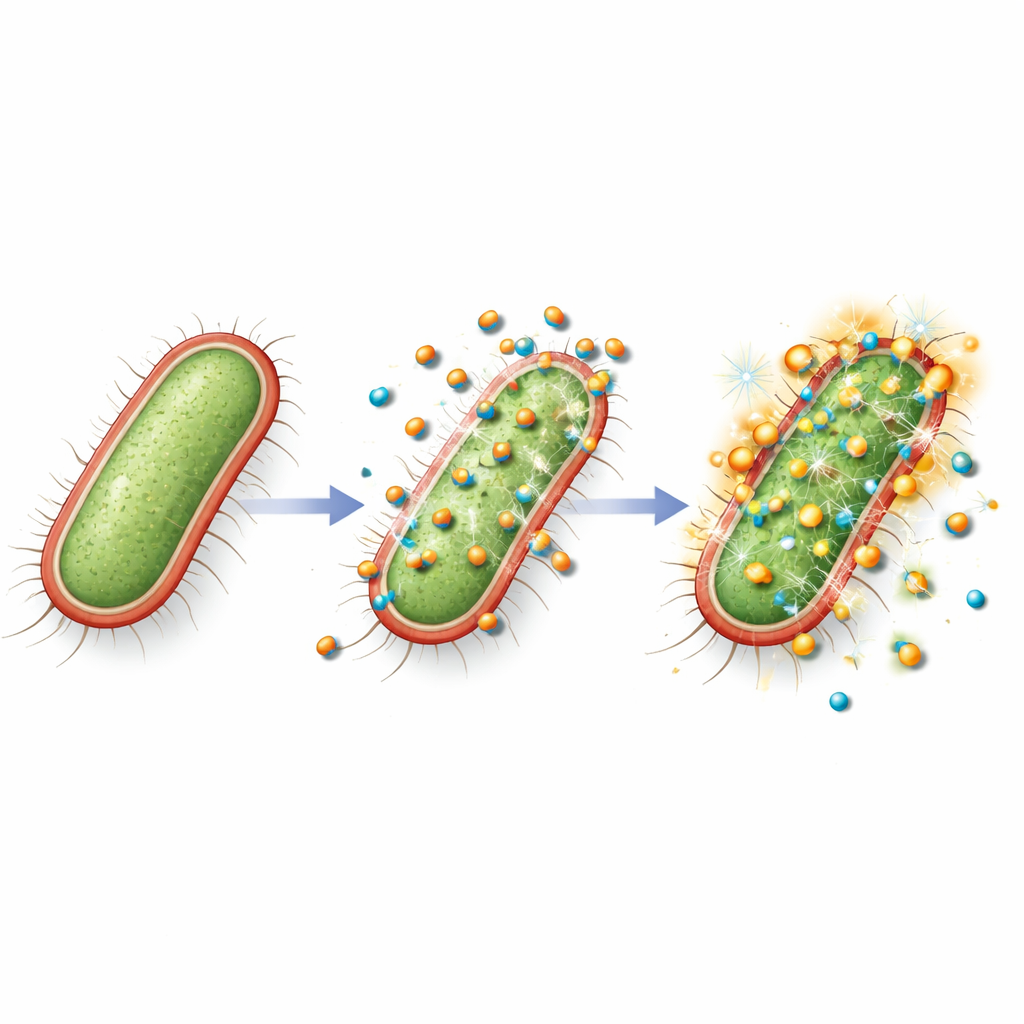
Wyłączanie narzędzi zakażenia
Co zaskakujące, nanokompozyt robił więcej niż tylko zabijać bakterie. Gdy badacze wystawili wielolekooporne E. coli na dawkę zbyt niską, by całkowicie zahamować wzrost, zmierzyli aktywność kluczowych genów pomagających bakteriom przyczepiać się do tkanek, komunikować z sąsiadami i wytwarzać toksyny. Pod tym subletalnym leczeniem geny odpowiedzialne za struktury przyczepne i produkcję toksyn wykazywały wielokrotne obniżenie aktywności, a centralny gen komunikacyjny używany w quorum sensing również został silnie stłumiony. Oznacza to, że bakterie, które przeżyły ekspozycję, były prawdopodobnie mniej zdolne do tworzenia biofilmów, koordynowania ataków i uszkadzania komórek gospodarza — skutecznie je rozbrajając, nawet jeśli nie zostały całkowicie wyeliminowane.
Co ta praca oznacza dla przyszłych terapii
Podsumowując, badanie pokazuje, że prosty grzyb glebowy można wykorzystać do wytworzenia mieszaniny nanocząstek miedzi i cynku, która działa na wielolekooporne E. coli na dwa sposoby: bezpośrednio atakuje komórki i jednocześnie wycisza genetyczne programy czyniące je niebezpiecznymi. Ponieważ proces unika toksycznych reagentów i używa tanich metali, można go skalować bardziej zrównoważenie niż wiele obecnych nanomateriałów. Zanim jednak trafi do klinik, naukowcy muszą potwierdzić bezpieczeństwo u zwierząt i ludzi oraz sprawdzić skuteczność w rzeczywistych ranach lub na urządzeniach medycznych. Mimo to nanokompozyt zbudowany przez grzyb wskazuje drogę ku nowej klasie terapii, które nie tylko zabijają superbakterie, lecz także pozbawiają je najgroźniejszych narzędzi.
Cytowanie: Obaid, A.N., Abdelghany, T.M., Soliman, A.M. et al. Green mycosynthesis of a CuO/ZnO heterojunction nanocomposite using Aspergillus terreus and its antibacterial and anti-virulence activity against multidrug-resistant Escherichia coli. Sci Rep 16, 12350 (2026). https://doi.org/10.1038/s41598-026-44775-z
Słowa kluczowe: wielolekooporne E. coli, zielona nanotechnologia, nanocząstki tlenków metali, powłoki antybakteryjne, hamowanie quorum sensing