Clear Sky Science · de
Grüne Mykosynthese eines CuO/ZnO-Heterojunktions-Nanokomposits mit Aspergillus terreus und dessen antibakterielle und anti‑Virulenz‑Aktivität gegen multiresistente Escherichia coli
Warum hartnäckige Infektionen uns alle betreffen
Viele gängige Infektionen, die früher mit einer kurzen Antibiotikakur rasch ausheilten, werden zunehmend schwerer und manchmal gar nicht mehr zu behandeln. Ein wesentlicher Schuldiger ist multiresistente Escherichia coli, ein Darmbakterium, das schmerzhafte Wund-, Harnwegs‑ und Blutbahninfektionen verursachen kann. Diese Studie untersucht einen ungewöhnlichen Verbündeten im Kampf gegen solche Supererreger: einen harmlosen Bodenpilz, der hilft, winzige Metallpartikel zu erzeugen, die nicht nur resistente E. coli abtöten können, sondern auch deren Krankheitspotential schwächen.
Ein Pilz, der wie eine winzige Fabrik wirkt
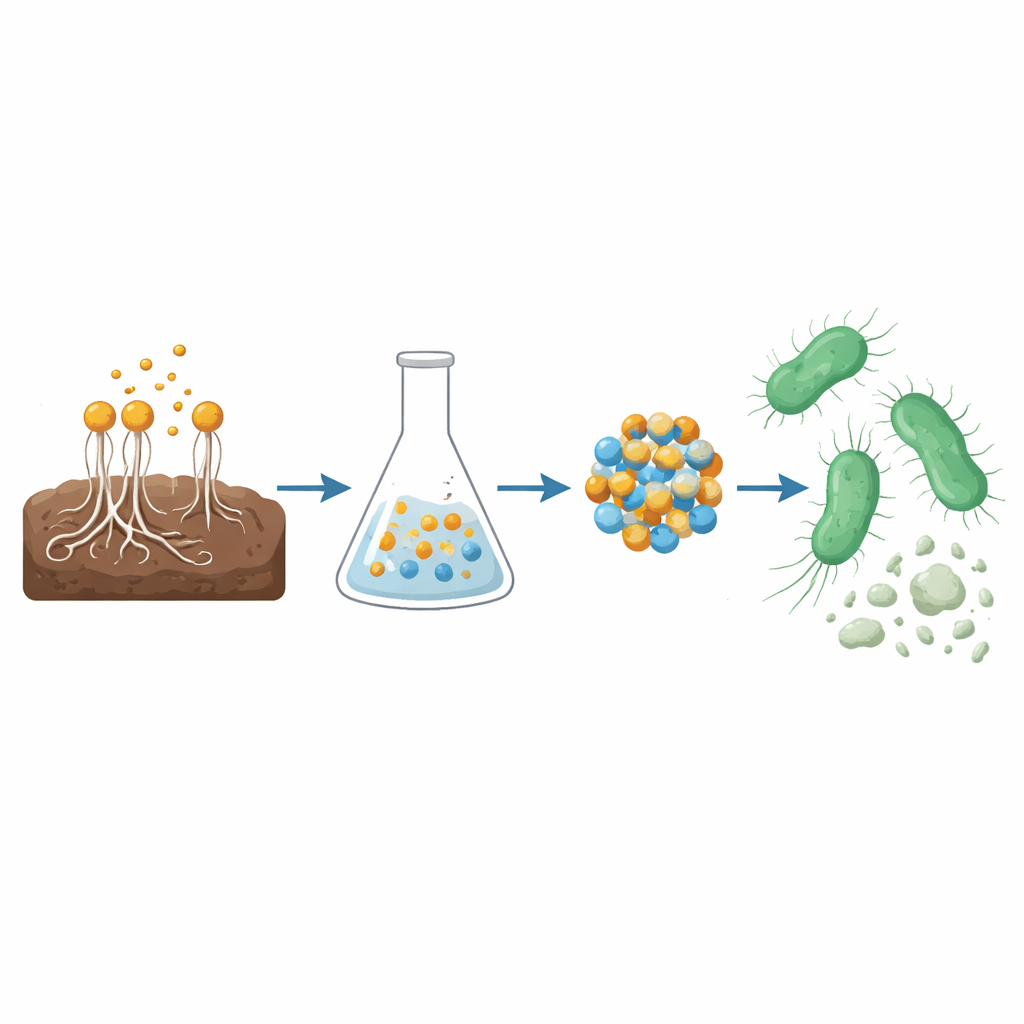
Die Forschenden begannen im Ackerboden und suchten nach einem Pilz, der als natürliche Nanotechnologie‑Werkstatt fungieren könnte. Sie isolierten und identifizierten einen Stamm von Aspergillus terreus, einen fadenförmigen Pilz, der ein Gemisch organischer Moleküle wie phenolische Säuren und Flavonoide ausschüttet. Mittels fortgeschrittener chemischer Analysen bestätigten sie, dass die Pilzbrühe Verbindungen wie Gallussäure, Ferulasäure und Apigenin enthielt. Diese Substanzen können Elektronen abgeben und an Metalloberflächen adsorbieren, wodurch sie ideal sind, gelöste Metallsalze ohne aggressive Chemikalien oder energieintensive Industrieprozesse in stabile, nanoskalige Partikel umzuwandeln.
Ein zweimetalliger Schutzschild gegen Bakterien
Statt ein einzelnes Metall zu verwenden, kombinierten die Forscher Kupfer und Zink zu einem CuO/ZnO‑Nanokomposit. Praktisch mischten sie den Pilzfiltrat mit Kupfer‑ und Zinkacetatlösungen. Die natürlichen Moleküle aus dem Pilz banden Kupfer‑ und Zinkionen, reduzierten sie und steuerten die Bildung extrem kleiner Kristalle der beiden Metalloxide. Nach Erhitzen zur Entfernung von Restorganik entstand ein Heterojunktions‑Nanokomposit—verschachtelte Kupferoxid‑ und Zinkoxidpartikel von etwa 45 Nanometern Durchmesser, tausende Male dünner als ein menschliches Haar. Mikroskopie und Spektroskopie bestätigten, dass beide Oxide vorhanden, gut ausgebildet und eng verbunden waren—eine Struktur, von der bekannt ist, dass sie die Erzeugung hochreaktiver Sauerstoffspezies fördert.
Im Einsatz gegen einen realen Supererreger
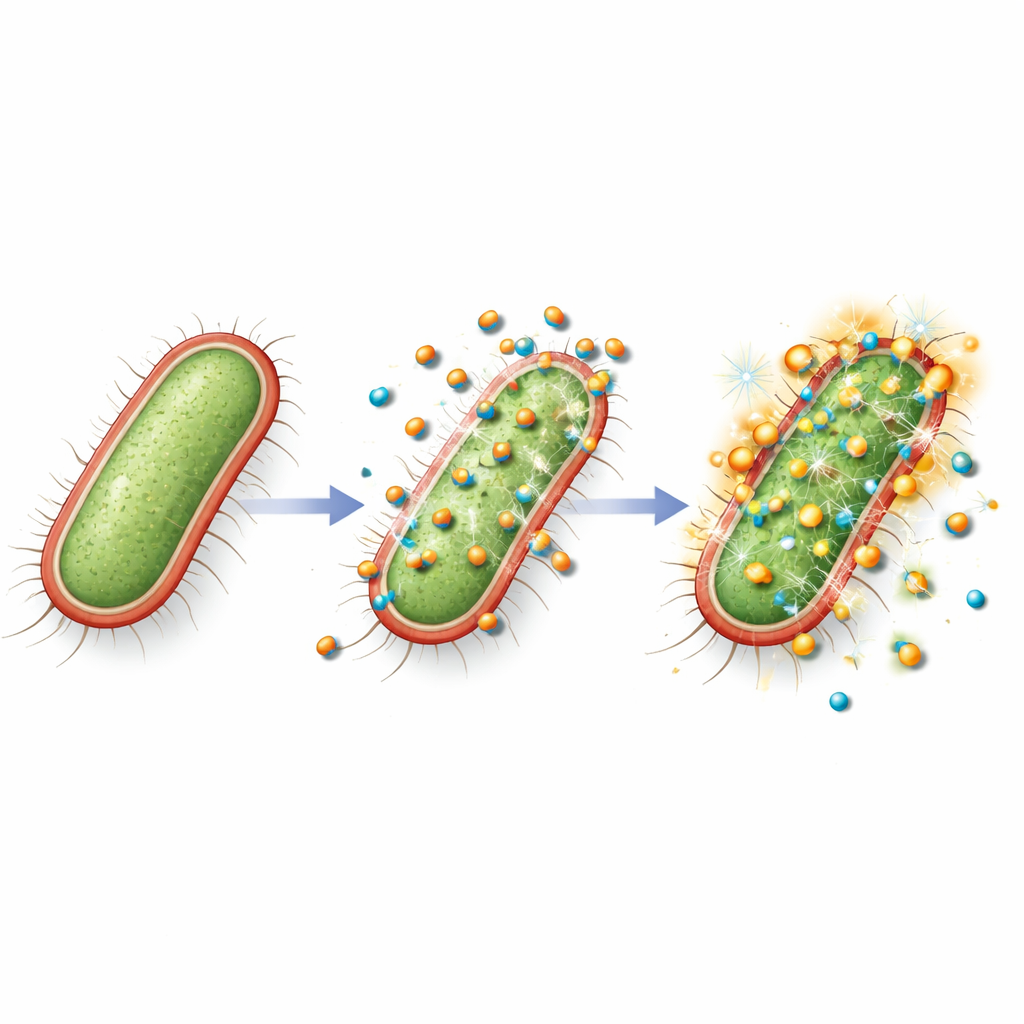
Um zu prüfen, ob diese grün hergestellten Partikel echte medizinische Bedrohungen bewältigen können, isolierten die Wissenschaftler einen E. coli‑Stamm aus Wundinfektionen irakischer Krankenhäuser und zeigten, dass er gegen alle getesteten Antibiotika resistent war. Das Pilzbrühen‑Extrakt allein verhinderte das Bakterienwachstum nicht. Im Gegensatz dazu erzeugte das CuO/ZnO‑Nanokomposit auf Kulturplatten klare Hemmhöfe und blockierte die bakterielle Vermehrung bei relativ niedrigen Konzentrationen in Brühtests. Im Verlauf reduzierten die Partikel die lebensfähigen Bakterienzahlen um mehrere Größenordnungen, besonders bei höheren Dosen, was auf echtes Abtöten statt nur verlangsamtes Wachstum hinweist. Diese Effekte werden wahrscheinlich durch mehrere kombinierte Wirkungen vermittelt: Die Partikel haften an der Bakterienoberfläche, stören die schützende Hülle, setzen Kupfer‑ und Zinkionen frei, die lebenswichtige Enzyme stören, und fördern die Bildung reaktiver Sauerstoffspezies, die Lipide, Proteine und DNA schädigen.
Die Werkzeuge der Infektion zum Schweigen bringen
Bemerkenswerterweise bewirkte das Nanokomposit mehr als nur Bakterienabtötung. Setzten die Forschenden multiresistente E. coli einer Dosis aus, die zu niedrig war, um das Wachstum vollständig zu stoppen, maßen sie die Aktivität zentraler Gene, die dem Bakterium helfen, an Gewebe zu haften, mit Nachbarn zu kommunizieren und Toxine zu produzieren. Unter dieser sublethalen Behandlung sank die Aktivität der Gene, die für Oberflächenhaftstrukturen und Toxinproduktion verantwortlich sind, um mehrere Facheinheiten, und ein zentrales Kommunikationsgen des Quorum‑Sensing wurde ebenfalls stark unterdrückt. Das bedeutet, dass die überlebenden Bakterien wahrscheinlich weniger fähig waren, Biofilme zu bilden, Angriffe zu koordinieren und Wirtszellen zu schädigen—sie wurden praktisch entwaffnet, auch wenn sie nicht vollständig eliminiert wurden.
Was diese Arbeit für zukünftige Therapien bedeutet
Insgesamt zeigt die Studie, dass ein einfacher Bodenpilz genutzt werden kann, um eine Kupfer‑Zink‑Nanopartikelmischung herzustellen, die gegen multiresistente E. coli auf zwei Arten wirkt: Sie greift die Zellen direkt an und dämpft zugleich die genetischen Programme, die sie gefährlich machen. Da der Prozess giftige Reagenzien vermeidet und preiswerte Metalle verwendet, könnte er nachhaltiger skaliert werden als viele derzeitige Nanomaterialien. Bevor eine klinische Anwendung möglich ist, müssen Wissenschaftler jedoch noch die Sicherheit in Tiermodellen und beim Menschen bestätigen und prüfen, wie gut das Material in echten Wunden oder an Medizinprodukten wirkt. Dennoch weist dieses pilzgefertigte Nanokomposit auf eine neue Klasse von Behandlungen hin, die Supererreger nicht nur töten, sondern ihnen zugleich ihre schädlichsten Werkzeuge nehmen.
Zitation: Obaid, A.N., Abdelghany, T.M., Soliman, A.M. et al. Green mycosynthesis of a CuO/ZnO heterojunction nanocomposite using Aspergillus terreus and its antibacterial and anti-virulence activity against multidrug-resistant Escherichia coli. Sci Rep 16, 12350 (2026). https://doi.org/10.1038/s41598-026-44775-z
Schlüsselwörter: multiresistente E. coli, grüne Nanotechnologie, Metalloxid‑Nanopartikel, antibakterielle Beschichtungen, Hemmung der Quorum‑Sensing