Clear Sky Science · es
Microsíntesis verde de un nanocompuesto heterounión CuO/ZnO usando Aspergillus terreus y su actividad antibacteriana y anti-virulencia frente a Escherichia coli multirresistente
Por qué las infecciones persistentes nos afectan a todos
Muchas infecciones comunes que antes se resolvían con un breve ciclo de antibióticos son cada vez más difíciles y, en ocasiones, imposibles de tratar. Un gran responsable es Escherichia coli multirresistente, un tipo de bacteria intestinal que puede provocar infecciones dolorosas en heridas, del tracto urinario y del torrente sanguíneo. Este estudio explora un aliado inusual en la lucha contra esos supermicrobios: un hongo de suelo inocuo que ayuda a fabricar diminutas partículas metálicas capaces no solo de matar E. coli resistente, sino también de debilitar su capacidad para causar enfermedad.
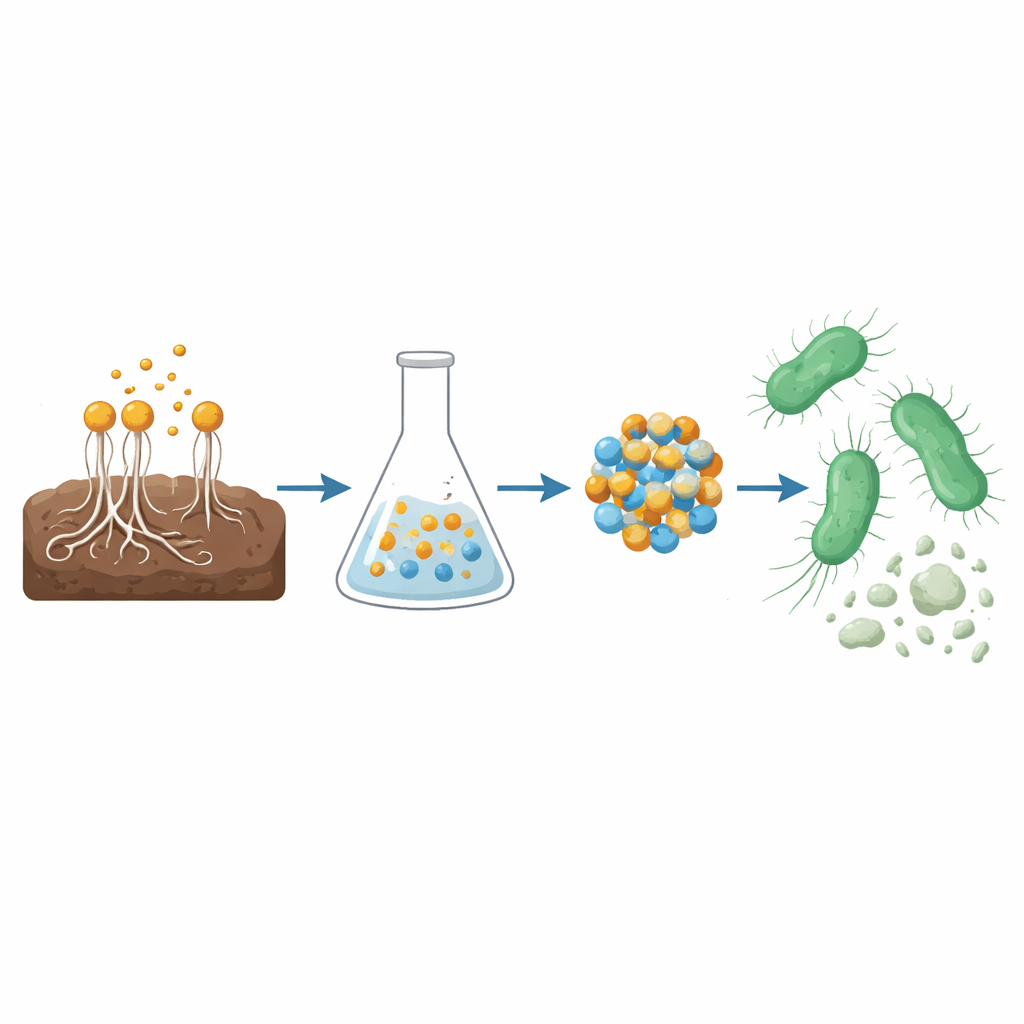
Un hongo que funciona como una pequeña fábrica
Los investigadores empezaron en suelo agrícola, buscando un hongo que pudiera actuar como un taller natural de nanotecnología. Aislaron e identificaron una cepa de Aspergillus terreus, un hongo filamentoso conocido por secretar una mezcla de moléculas orgánicas como ácidos fenólicos y flavonoides. Mediante análisis químicos avanzados, confirmaron que el caldo fúngico contenía compuestos como ácido gálico, ácido ferúlico y apigenina. Estas sustancias pueden donar electrones y adherirse a superficies metálicas, por lo que son ideales para transformar sales metálicas disueltas en partículas estables de tamaño nanométrico sin recurrir a productos químicos agresivos ni a procesos industriales de alta energía.
Construyendo un escudo bimetálico contra bacterias
En lugar de usar un solo metal, el equipo combinó cobre y zinc para formar un nanocompuesto CuO/ZnO. En términos prácticos, mezclaron el filtrado fúngico con soluciones de acetato de cobre y de zinc. Las moléculas naturales del hongo se unieron a los iones de cobre y zinc, los redujeron y guiaron la formación de cristales extremadamente pequeños de ambos óxidos metálicos. Tras un calentamiento para eliminar restos de material orgánico, el resultado fue un nanocompuesto heterounión: partículas entrelazadas de óxido de cobre y óxido de zinc de aproximadamente 45 nanómetros de diámetro, miles de veces más finas que un cabello humano. La microscopía y la espectroscopía confirmaron que ambos óxidos estaban presentes, bien formados y fuertemente conectados, una estructura conocida por potenciar la generación de especies reactivas ricas en oxígeno.
Enfrentando a un supermicrobio real
Para comprobar si estas partículas producidas de forma verde podían enfrentarse a amenazas médicas reales, los científicos aislaron una cepa de E. coli de infecciones de heridas en hospitales iraquíes y demostraron que resistía todos los antibióticos probados. El caldo fúngico por sí solo no detuvo el crecimiento bacteriano. En contraste, el nanocompuesto CuO/ZnO produjo claros halos de inhibición en placas de cultivo y bloqueó la multiplicación bacteriana a concentraciones relativamente bajas en pruebas en caldo. Con el tiempo, las partículas redujeron el recuento de bacterias viables en varios órdenes de magnitud, sobre todo a dosis más altas, lo que indica una acción bactericida real más que una mera ralentización del crecimiento. Se piensa que estos efectos surgen de varias acciones combinadas: las partículas se adhieren a la superficie bacteriana, alteran su envoltura protectora, liberan iones de cobre y zinc que interfieren con enzimas vitales y favorecen la formación de especies reactivas de oxígeno que dañan lípidos, proteínas y ADN.
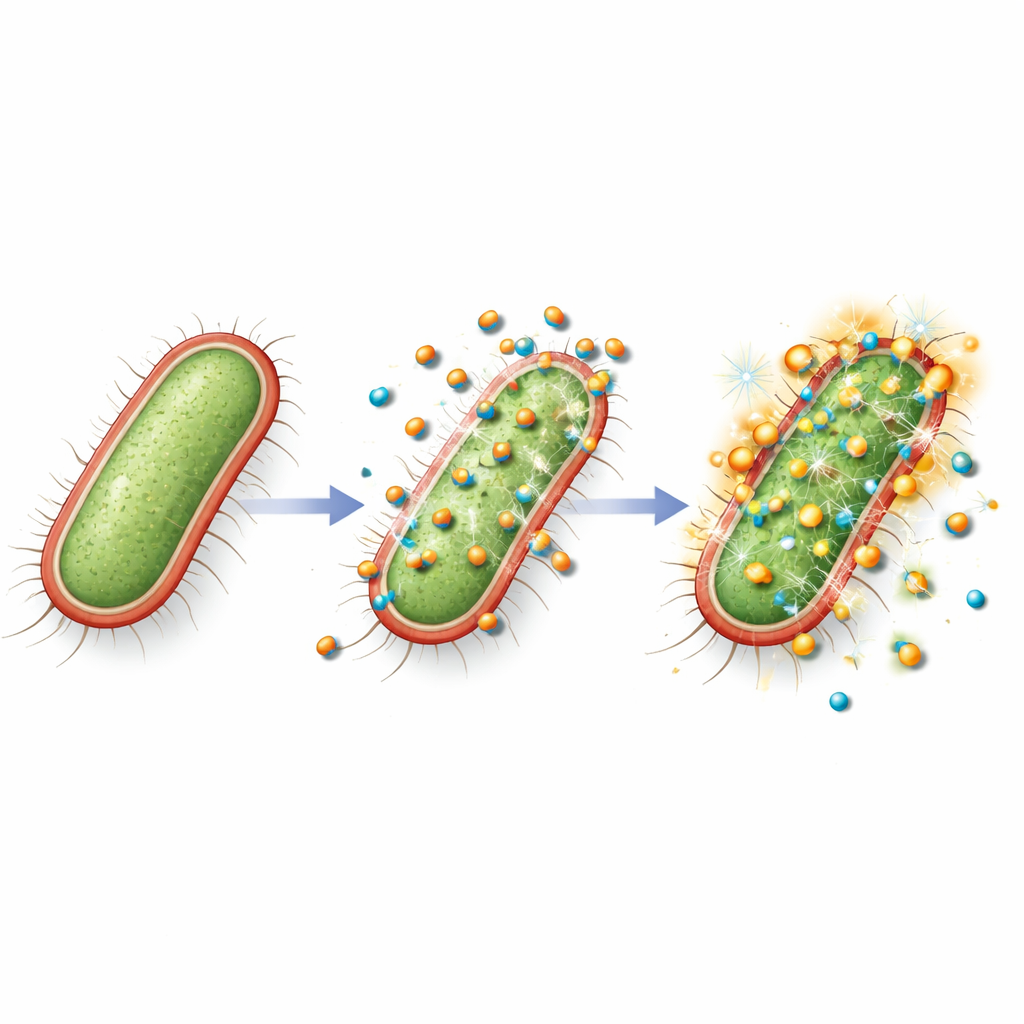
Silenciando las herramientas de la infección
De forma notable, el nanocompuesto hizo más que matar bacterias. Cuando los investigadores expusieron la E. coli multirresistente a una dosis demasiado baja para detener el crecimiento por completo, midieron la actividad de genes clave que ayudan a la bacteria a adherirse a tejidos, comunicarse con vecinas y producir toxinas. Bajo este tratamiento subletal, la actividad de genes responsables de estructuras de adhesión y de producción de toxinas se redujo varios pliegues, y un gen central de comunicación usado en el quorum sensing también quedó fuertemente suprimido. Esto significa que las bacterias que sobrevivieron a la exposición probablemente eran menos capaces de formar biopelículas, coordinar ataques y dañar células del huésped, desarmándolas efectivamente incluso cuando no eran eliminadas por completo.
Qué significa este trabajo para tratamientos futuros
En conjunto, el estudio muestra que un hongo de suelo simple puede aprovecharse para construir una mezcla de nanopartículas de cobre y zinc que actúa contra E. coli multirresistente de dos maneras: ataca las células directamente y, al mismo tiempo, atenúa los programas genéticos que las hacen peligrosas. Dado que el proceso evita reactivos tóxicos y emplea metales de bajo coste, podría escalarse de forma más sostenible que muchos nanomateriales actuales. Antes de poder aplicarse en clínicas, los científicos deben confirmar la seguridad en animales y humanos y probar su eficacia en heridas reales o en dispositivos médicos. Pero este nanocompuesto fabricado por hongos apunta hacia una nueva clase de tratamientos que no solo matan supermicrobios, sino que también les quitan sus trucos más dañinos.
Cita: Obaid, A.N., Abdelghany, T.M., Soliman, A.M. et al. Green mycosynthesis of a CuO/ZnO heterojunction nanocomposite using Aspergillus terreus and its antibacterial and anti-virulence activity against multidrug-resistant Escherichia coli. Sci Rep 16, 12350 (2026). https://doi.org/10.1038/s41598-026-44775-z
Palabras clave: E. coli multirresistente, nanotecnología verde, nanopartículas de óxidos metálicos, revestimientos antibacterianos, inhibición del quorum sensing