Clear Sky Science · pl
Warianty genetyczne i markery surowicze CXCL8, MAP3K7, LTA/TNF, EXOC3L1, PROCR i TRAF2 w zwyrodnieniu plamki związanym z wiekiem: powiązania z ryzykiem choroby i odpowiedzią na leczenie
Dlaczego ta historia o chorobie oczu ma znaczenie
W miarę jak żyjemy dłużej, coraz więcej osób staje w obliczu zwyrodnienia plamki związanego z wiekiem (AMD), schorzenia, które stopniowo odbiera ostrą, centralną widoczność niezbędną do czytania, prowadzenia samochodu i rozpoznawania twarzy. Lekarze potrafią spowolnić jedną zaawansowaną postać AMD za pomocą zastrzyków blokujących sygnał wzrostu nowych naczyń krwionośnych, jednak wielu pacjentów nie reaguje tak dobrze, jak oczekiwano. Badanie stawia dwuczęściowe pytanie ważne dla pacjentów i rodzin: które dziedziczne różnice w naszych genach zwiększają lub zmniejszają ryzyko AMD i czy te same różnice mogą pomóc przewidzieć, kto najbardziej skorzysta z dostępnych terapii?
Patrząc poza zwykłych podejrzanych genów
Wcześniejsze badania wyraźnie powiązały AMD z genami zaangażowanymi w układ dopełniacza, rodzaj molekularnej „ekipy sprzątającej” i obronnej. Jednak te znane geny nie wyjaśniają w pełni, dlaczego niektórzy ludzie rozwijają AMD, a inni nie. Autorzy zwrócili się ku innemu zestawowi genów związanych z zapaleniem, angiogenezą, stresem komórkowym i zdrowiem komórek podtrzymujących siatkówkę. Skoncentrowali się na sześciu genach — CXCL8, MAP3K7, LTA/TNF, EXOC3L1, PROCR i TRAF2 — oraz na drobnych, powszechnych zmianach w DNA w nich występujących, zwanych wariantami jednokrotnego nukleotydu. Mierzyli też poziomy odpowiadających im białek we krwi, by sprawdzić, czy różnice genetyczne przekładają się na mierzalne zmiany w organizmie.
Kto był badany i co mierzono
Zespół przebadał 946 osób leczonych w klinice okulistycznej uniwersytetu na Litwie. Uczestników pogrupowano na osoby bez AMD, z wczesnymi oznakami choroby oraz z zaawansowaną postacią „wilgotną” (wysiękową), która wiąże się z kruchemi nowymi naczyniami krwionośnymi przeciekającymi pod siatkówką. Wszyscy badani przeszli szczegółowe badania okulistyczne i obrazowe. U każdej osoby przeanalizowano DNA z próbki krwi, by ustalić, jaką wersję każdego z wybranych genów nosi. W podgrupie zmierzono także poziomy sześciu białek we krwi. Wśród chorych z wysiękowym AMD śledzono ostrość wzroku i grubość siatkówki w ciągu kilku miesięcy terapii zastrzykami przeciwko VEGF i klasyfikowano oczy jako reagujące lub niereagujące.
Sygnał ochronny i wskazówka o zwiększonym ryzyku
Najwyraźniejszy wzorzec genetyczny ujawnił się w genie EXOC3L1, który pomaga kontrolować przemieszczanie pęcherzyków z materiałem wewnątrz komórek — proces istotny dla zdrowia komórek wspierających siatkówkę. Pewna wersja tego genu, określana przez formę „G” badanego wariantu, była wyraźnie rzadsza u osób z wczesnym i wysiękowym AMD niż u osób bez choroby. Modele statystyczne sugerowały, że noszenie tej odmiany G zmniejszało szanse wystąpienia AMD mniej więcej o połowę lub więcej, zarówno u mężczyzn, jak i u kobiet, co wskazuje na rolę ochronną. Dla kontrastu wariant w genie CXCL8 — znanym z produkcji sygnału immunologicznego IL-8 — wykazywał tendencję do zwiększania prawdopodobieństwa wystąpienia wysiękowego AMD, zwłaszcza w niektórych modelach porównań genetycznych i wyraźniej u kobiet, chociaż niektóre z tych powiązań osłabły po bardzo surowej korekcie wielokrotnych porównań.
Markery we krwi i odpowiedź na leczenie
Gdy zespół spojrzał na poziomy białek we krwi, większość badanych markerów, w tym CXCL8, MAP3K7, LTA/TNF, EXOC3L1 i TRAF2, nie różniła się istotnie między osobami z AMD i bez niego. Wyjątkiem był PROCR — gen aktywny w komórkach wyściełających naczynia krwionośne. Osoby z wysiękowym AMD miały wyższe poziomy białka PROCR niż uczestnicy kontrolni, szczególnie wśród nosicieli określonego genotypu PROCR. Wzorzec ten wspiera hipotezę, że subtelne zaburzenia regulacji naczyń krwionośnych przyczyniają się do przeciekających, wrażliwych naczyń obserwowanych w AMD typu „wilgotnego”. Jednak żaden z badanych wariantów genetycznych ani poziomów białek nie rozdzielił wiarygodnie pacjentów dobrze reagujących na zastrzyki przeciw VEGF od tych, którzy nie reagowali, przynajmniej przy wielkości próbki zastosowanej w tym badaniu.
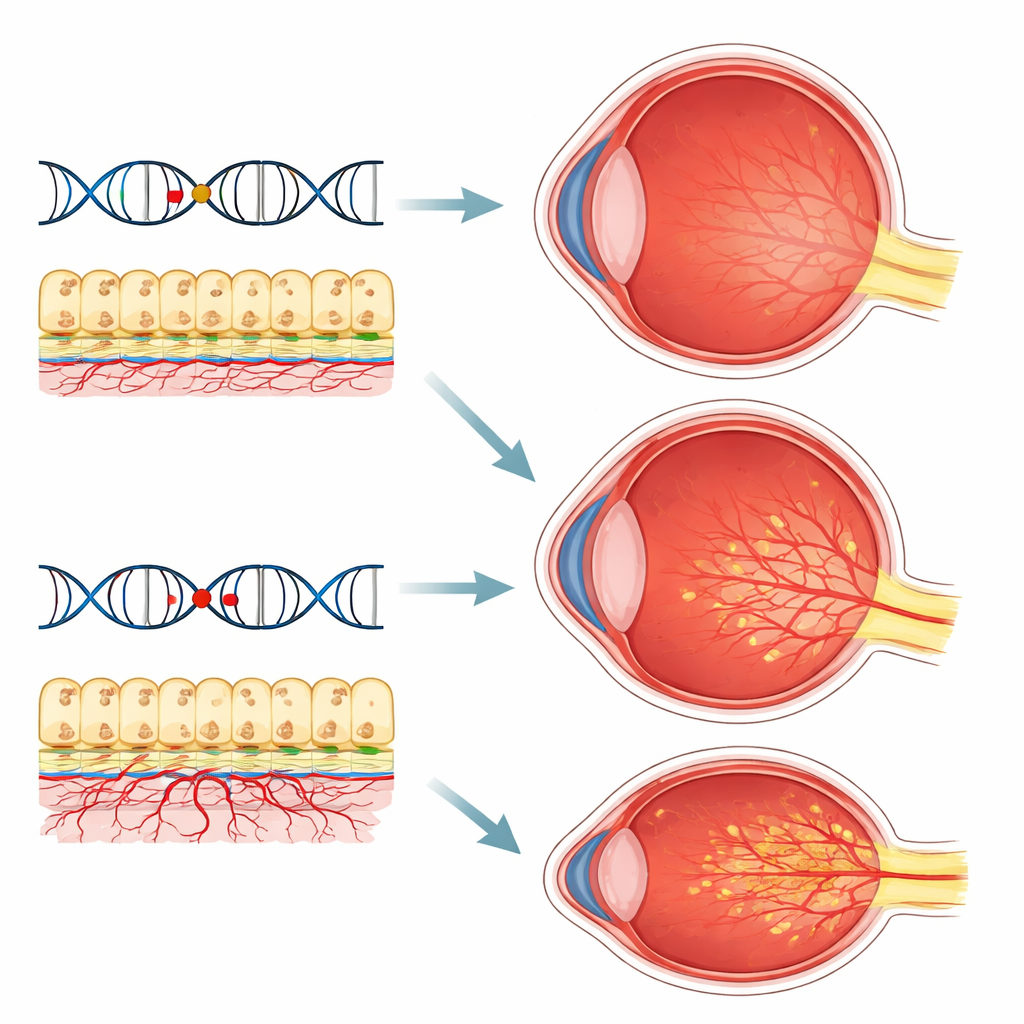
Co to oznacza dla pacjentów i przyszłej opieki
W sumie wyniki wzmacniają pogląd, że AMD jest napędzane przez kilka nakładających się dróg biologicznych — przewlekłe zapalenie, zaburzenia przepływu krwi i przeciążenie komórek wspierających siatkówkę — a nie przez jeden „zły” gen. Wariant w EXOC3L1 wydaje się zapewniać pewną naturalną ochronę, podczas gdy CXCL8 i PROCR mogą przechylać równowagę w stronę szkodliwej angiogenezy w oku. Obecnie te odkrycia nie zmienią sposobu leczenia pacjenta w klinice, ale przesuwają pole badań w kierunku przyszłości, w której prosty test krwi lub panel genetyczny mógłby pomóc zidentyfikować osoby o najwyższym ryzyku utraty wzroku oraz tych, którzy mogliby skorzystać z nowych, lepiej dopasowanych terapii wykraczających poza obecne leki przeciw VEGF.
Cytowanie: Cebatoriene, D., Vilkeviciute, A., Duseikaite-Vidike, M. et al. Genetic variants and serum biomarkers of CXCL8, MAP3K7, LTA/TNF, EXOC3L1, PROCR, and TRAF2 in Age-Related macular degeneration: associations with disease risk and therapeutic response. Sci Rep 16, 13793 (2026). https://doi.org/10.1038/s41598-026-42838-9
Słowa kluczowe: zwyrodnienie plamki związane z wiekiem, warianty genetyczne, naczynia krwionośne siatkówki, zapalenie, spersonalizowane leczenie oczu