Clear Sky Science · it
Varianti genetici e biomarcatori sierici di CXCL8, MAP3K7, LTA/TNF, EXOC3L1, PROCR e TRAF2 nella degenerazione maculare legata all’età: associazioni con il rischio di malattia e la risposta terapeutica
Perché questa storia sull’occhio è importante
Con l’aumento della durata della vita, sempre più persone sono colpite dalla degenerazione maculare legata all’età (DMA), una condizione che lentamente priva della visione centrale nitida necessaria per leggere, guidare e riconoscere i volti. I medici possono rallentare una forma avanzata di DMA con iniezioni che bloccano un segnale di crescita per i nuovi vasi sanguigni, ma molti pazienti non rispondono così bene come sperato. Questo studio pone una domanda in due parti che interessa pazienti e famiglie: quali differenze ereditarie nei nostri geni aumentano o riducono il rischio di DMA, e le stesse differenze possono aiutare a prevedere chi trarrà maggior beneficio dai trattamenti attuali?
Oltre i geni sospettati di routine
Ricerche precedenti hanno collegato saldamente la DMA a geni coinvolti nel sistema del complemento, una sorta di squadra molecolare di pulizia e difesa. Ma quei geni noti non spiegano completamente perché alcune persone sviluppano la DMA e altre no. Gli autori si sono rivolti a un diverso insieme di geni legati all’infiammazione, alla crescita dei vasi sanguigni, allo stress cellulare e alla salute delle cellule di supporto della retina. Hanno concentrato l’attenzione su sei geni—CXCL8, MAP3K7, LTA/TNF, EXOC3L1, PROCR e TRAF2—and su piccoli cambiamenti del DNA comuni al loro interno, detti varianti a singolo nucleotide. Hanno inoltre misurato i livelli delle proteine corrispondenti nel sangue per vedere se le differenze genetiche si traducevano in cambiamenti misurabili nell’organismo.
Chi è stato studiato e cosa è stato misurato
Il gruppo ha esaminato 946 persone trattate in una clinica oculistica universitaria in Lituania. I partecipanti sono stati divisi in chi non aveva DMA, chi presentava segni iniziali della malattia e chi aveva la forma avanzata “umida” o essudativa, che comporta nuovi vasi fragili che perdono sotto la retina. Tutti i partecipanti hanno effettuato esami oculari dettagliati e indagini di imaging. Per ciascuna persona i ricercatori hanno analizzato il DNA da un campione di sangue per determinare quale versione di ciascun gene selezionato fosse presente. In un sottoinsieme è stato anche misurato il livello ematico delle sei proteine. Tra i pazienti con DMA essudativa, hanno seguito l’acuità visiva e lo spessore retinico per diversi mesi durante la terapia con iniezioni anti-VEGF e hanno classificato gli occhi come responder o non-responder.
Un segnale genetico protettivo e un indizio di rischio aumentato
Il modello genetico più netto è emerso nel gene EXOC3L1, che aiuta a controllare il movimento dei pacchetti di materiale all’interno delle cellule—un processo essenziale per la salute delle cellule di supporto retiniche. Una versione particolare di questo gene, definita dalla forma “G” della variante testata, era nettamente meno comune nelle persone con DMA iniziale o essudativa rispetto a quelle senza la malattia. La modellizzazione statistica suggeriva che portare questa variante G riduceva le probabilità di avere la DMA di circa la metà o più, sia negli uomini sia nelle donne, sostenendo un ruolo protettivo. Al contrario, una variante nel gene CXCL8—meglio noto per codificare il segnale immunitario IL-8—ha mostrato una tendenza ad aumentare le probabilità di avere una DMA essudativa, specialmente in certi modelli di confronto genetico e in modo più chiaro nelle donne, anche se alcuni di questi legami si attenuavano dopo correzioni molto stringenti per test multipli.
Marcatori ematici e risposta al trattamento
Quando il gruppo ha analizzato i livelli proteici nel sangue, la maggior parte dei marker testati, inclusi CXCL8, MAP3K7, LTA/TNF, EXOC3L1 e TRAF2, non risultava significativamente diversa tra persone con e senza DMA. Un’eccezione è stata PROCR, un gene attivo nelle cellule che rivestono i vasi sanguigni. Le persone con DMA essudativa avevano livelli più alti della proteina PROCR rispetto ai controlli, e ciò era particolarmente vero per chi possedeva un genotipo PROCR specifico. Questo schema supporta l’idea che problemi sottili nella regolazione dei vasi contribuiscano ai vasi che perdono e sono fragili nella DMA umida. Tuttavia, nessuna delle varianti genetiche o dei livelli proteici testati ha distinto in modo affidabile i pazienti che rispondevano bene alle iniezioni anti-VEGF da quelli che non rispondevano, almeno con le dimensioni del campione di questo studio.
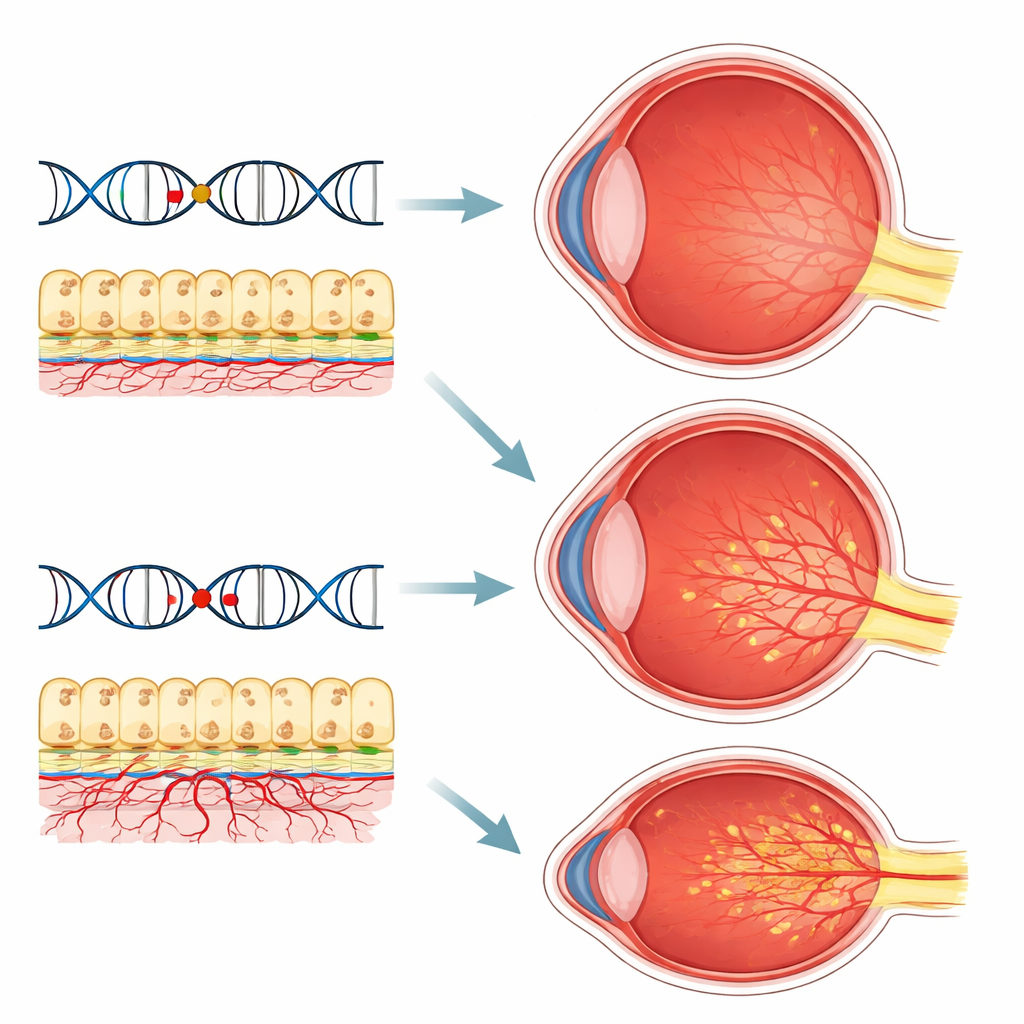
Cosa significa per i pazienti e per la cura futura
Nel complesso, i risultati rafforzano la visione che la DMA sia guidata da più vie biologiche sovrapposte—infiammazione cronica, alterato flusso vascolare e stress delle cellule di supporto retiniche—piuttosto che da un singolo “gene cattivo”. Una variante di EXOC3L1 sembra offrire una certa protezione naturale, mentre CXCL8 e PROCR possono spostare l’equilibrio verso una crescita vascolare dannosa nell’occhio. Oggi questi risultati non cambieranno il trattamento clinico del paziente, ma orientano il campo verso un futuro in cui un semplice esame del sangue o un pannello genetico potrebbe aiutare a identificare chi è a maggior rischio di perdita della vista e chi potrebbe beneficiare di nuovi trattamenti più mirati che vadano oltre gli attuali farmaci anti-VEGF.
Citazione: Cebatoriene, D., Vilkeviciute, A., Duseikaite-Vidike, M. et al. Genetic variants and serum biomarkers of CXCL8, MAP3K7, LTA/TNF, EXOC3L1, PROCR, and TRAF2 in Age-Related macular degeneration: associations with disease risk and therapeutic response. Sci Rep 16, 13793 (2026). https://doi.org/10.1038/s41598-026-42838-9
Parole chiave: degenerazione maculare legata all’età, varianti genetiche, vasi sanguigni retinici, infiammazione, trattamento oftalmico personalizzato