Clear Sky Science · pl
Wpływ dystansu taksonomicznego i scriptaidu na rozwój zarodków iSCNT u świń (Suidae)
Przywracanie zanikających świń
Wiele dzikich gatunków świń zmierza ku wyginięciu, tymczasem pobieranie komórek jajowych od tych rzadkich zwierząt jest trudne, a często niemożliwe. Jednym z proponowanych obejść jest rodzaj biologicznej „surogatki”: przeniesienie DNA zagrożonego zwierzęcia do komórki jajowej pokrewnego zwierzęcia hodowlanego, z nadzieją na wyhodowanie zarodka w laboratorium. W tym badaniu zadano pytanie, jak daleko można posunąć się tą metodą w obrębie rodziny świń i czy mała cząsteczka leku może pomóc pokonać ukryte problemy zgodności w tych hybrydowych zarodkach.
Budowanie hybrydowych zarodków w laboratorium
Naukowcy skupili się na przedstawicielach rodziny świń, Suidae, która obejmuje znane świnie domowe oraz bardziej skryte gatunki leśne, takie jak świnia brodata i babirusa. Z użyciem techniki transferu jądra komórkowego (somatic cell nuclear transfer) usunęli materiał genetyczny z komórek jajowych świń domowych i zastąpili go jądrami komórek skóry pochodzącymi z trzech źródeł: świnia domowa (punkt odniesienia), świnia brodata (inny gatunek z tego samego rodzaju) oraz babirusa (dalszy krewny z innej podrodziny). Wszystkie zarodki rozwijały się w tym samym środowisku komórek jajowych świń domowych, co pozwoliło zespołowi odizolować wpływ pokrewieństwa między gatunkiem dawcy a gatunkiem jajka. 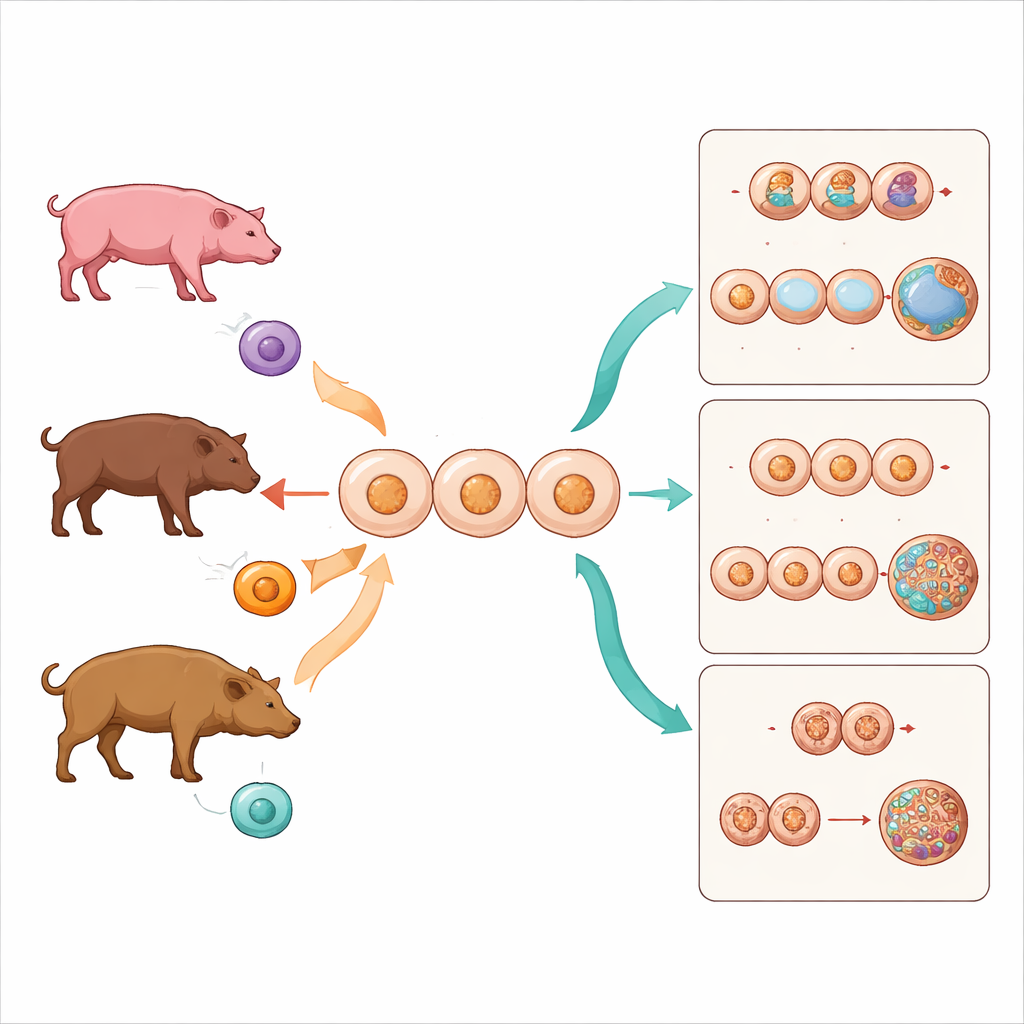
Kiedy pokrewieństwo decyduje o szansie na życie
Wynik był wyraźny. Zarodki powstałe z jąder świń domowych transferowanych do jaj świń domowych osiągały najlepsze wyniki — ponad jedna czwarta dochodziła do stadium blastocysty, zaawansowanego etapu odpowiedniego do implantacji. Jądra świni brodatej, pochodzące z innego, lecz blisko spokrewnionego gatunku, radziły sobie słabiej, ale nadal wytworzyły niektóre blastocysty. Natomiast jądra babirusy, pochodzące z dalszej gałęzi drzewa genealogicznego świń, nigdy nie dały blastocyst; zatrzymywały się wcześniej jako małe kuliste skupiska komórek. Ten stopniowy spadek sukcesu rozwojowego wraz ze wzrostem dystansu ewolucyjnego uwidacznia praktyczną barierę nazywaną czasem „ścianą taksonomiczną”: poza pewną różnicą między dawcą a jajkiem, zarodek po prostu nie może kontynuować rozwoju.
Chemiczny impuls dla zarodków, które utknęły
Zespół sprawdził następnie, czy Scriptaid — lek rozluźniający sposób, w jaki DNA jest upakowane — może poprawić te szanse. Poprzez uczynienie materiału genetycznego bardziej dostępnym, Scriptaid może w teorii pomóc zresetować jądro dawcy do wczesnego stanu embrionalnego. Gdy jądra świni brodatej traktowano Scriptaidem po transferze do jaj świń domowych, więcej zarodków osiągnęło stadium blastocysty, a ich wczesne podziały komórkowe zachodziły szybciej, bardziej zbliżone do tych obserwowanych w klonach świń domowych. Lek również krótkotrwale podnosił poziomy pewnego chemicznego znacznika na białkach upakowujących DNA (acetylacja H3K9) podczas pierwszych dwóch stadiów podziałów, co sugeruje bardziej aktywne uruchomienie programów genetycznych. Jednak Scriptaid nie był w stanie uratować bardziej odległych zarodków babirusy, które nadal nie przechodziły stadium moruli.
Elektrownie komórkowe i zaburzone sygnały
Aby zrozumieć, dlaczego pokrewieństwo miało tak duże znaczenie, naukowcy przeanalizowali, które geny były włączone lub wyłączone na kilku wczesnych etapach we wszystkich typach zarodków. Odkryli, że wiele różnic między udanymi a nieudanymi zarodkami dotyczyło „elektrowni” komórkowych — mitochondriów. Mitochondria mają własny niewielki zestaw genów, ale w dużej mierze polegają też na genach jądrowych komórki. W hybrydowych zarodkach jądro i mitochondria pochodziły z różnych gatunków, a ich komunikacja wydawała się zawodna wraz ze wzrostem dystansu ewolucyjnego. Wiele dotkniętych genów należało do rodzin odpowiedzialnych za kluczowy element łańcucha energetycznego znanego jako fosforylacja oksydacyjna. W bardziej odległych połączeniach te jądrowe geny miały tendencję do obniżonej ekspresji, podczas gdy w bliższych parowaniach mogły być bardziej aktywne. Po dodaniu Scriptaidu inny zestaw genów mitochondrialnych — tym razem zakodowanych w samych mitochondriach — odpowiedział silnie, co sugeruje, że lek częściowo przestroił to partnerstwo między jądrem a mitochondriami.
Co to oznacza dla ratowania gatunków
Podsumowując, badanie pokazuje, że klonowanie międzygatunkowe w obrębie rodziny świń to nie tylko mechaniczne zamienianie DNA; opiera się na subtelnej komunikacji między genami jądrowymi a mitochondrialnymi, które ewoluowały razem przez miliony lat. Gdy dawca i jajko są blisko spokrewnione, ta komunikacja może być zaburzona, ale nadal funkcjonować wystarczająco, by wytworzyć blastocysty, zwłaszcza jeśli wspomóc ją lekiem modyfikującym chromatynę, takim jak Scriptaid. Gdy gatunki są bardziej odległe, rozbieżność w ich komórkowej „sieci energetycznej” staje się zbyt duża i rozwój zatrzymuje się pomimo chemicznej pomocy. Dla działań konserwatorskich sugeruje to, że klonowanie międzygatunkowe ma największe perspektywy między bardzo blisko spokrewnionymi gatunkami, a przyszłe strategie będą musiały bezpośrednio adresować nie tylko reprogramowanie jądra, lecz także niedopasowanie w produkcji energii.
Cytowanie: Liu, HJ., Wong, K.W., Ma, X. et al. Effect of taxonomical distance and scriptaid on iSCNT embryo development in suidae. Sci Rep 16, 11288 (2026). https://doi.org/10.1038/s41598-026-41963-9
Słowa kluczowe: klonowanie międzygatunkowe, zagrożone świnie, mitochondria, rozwój zarodka, leki epigenetyczne