Clear Sky Science · it
Effetto della distanza tassonomica e della scriptaid sullo sviluppo degli embrioni iSCNT nei suidi
Riportare indietro i maiali in via di sparizione
Molte specie di maiali selvatici stanno scivolando verso l’estinzione, ma raccogliere ovociti da questi animali rari è difficile e spesso impossibile. Una soluzione proposta è una sorta di “surrogazione” biologica: prendere il DNA di un animale minacciato e trasferirlo in un ovocita di un animale da allevamento correlato, nella speranza di far sviluppare un embrione in laboratorio. Questo studio esplora quanto lontano si possa spingere questo approccio all’interno della famiglia dei suidi e se una piccola molecola farmacologica possa aiutare a superare problemi di compatibilità nascosti all’interno di questi embrioni ibridi.
Costruire embrioni ibridi in laboratorio
I ricercatori si sono concentrati sui membri della famiglia dei suidi, che include i maiali domestici familiari e abitanti delle foreste più elusivi come il maiale barbuto e il babirusa. Usando una tecnica chiamata trasferimento nucleare di cellule somatiche, hanno rimosso il materiale genetico dagli ovociti di maiale domestico e lo hanno sostituito con nuclei di cellule della pelle provenienti da tre sorgenti: maiale domestico (il riferimento), maiale barbuto (una specie diversa ma nello stesso genere) e babirusa (un cugino più distante appartenente a un’altra sottofamiglia). Tutti gli embrioni sono cresciuti nello stesso ambiente di ovociti di maiale domestico, permettendo al team di isolare l’effetto della vicinanza tassonomica tra il donatore e la specie dell’ovocita. 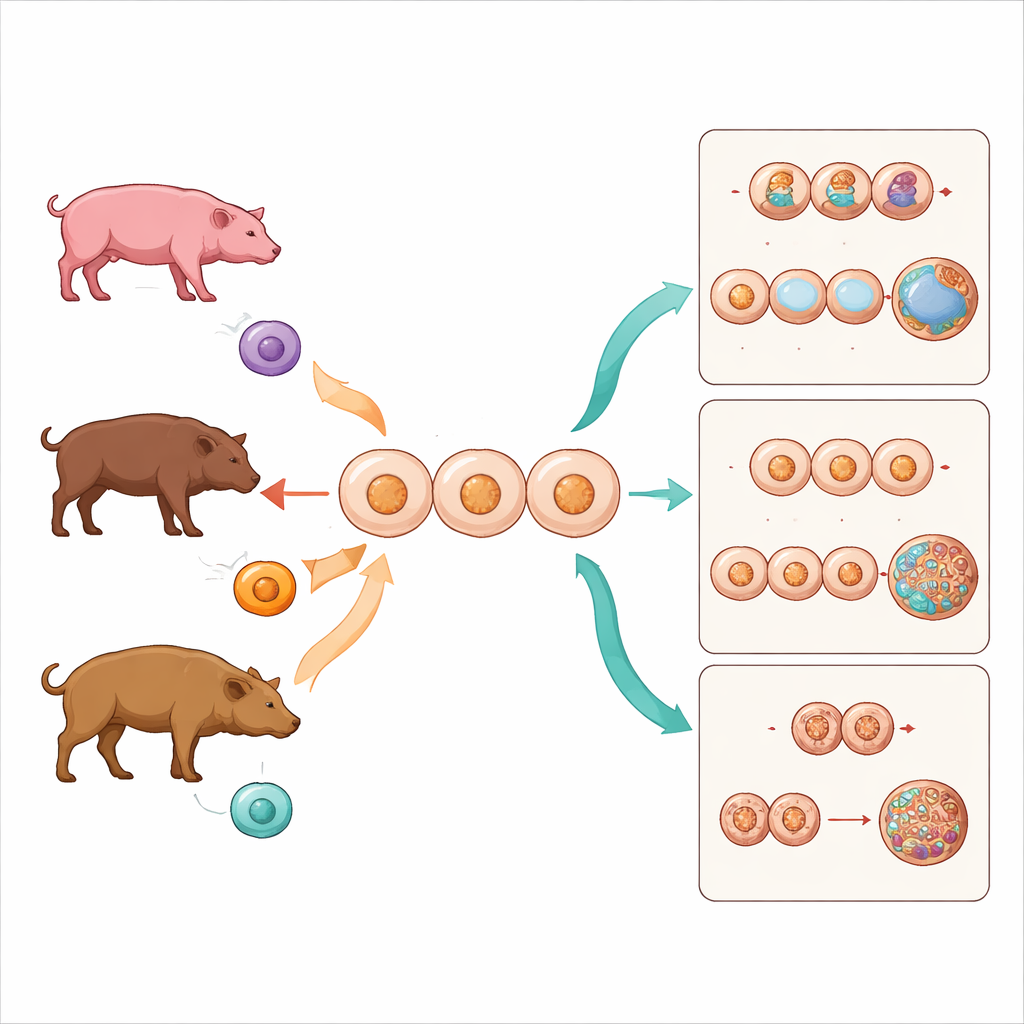
Quando la parentela determina le probabilità di vita
I risultati sono stati netti. Gli embrioni ottenuti da nuclei di maiale domestico inseriti in ovociti di maiale domestico hanno avuto il successo maggiore, con oltre un quarto che ha raggiunto lo stadio di blastocisti, un punto avanzato adatto all’impianto. I nuclei del maiale barbuto, provenienti da una specie diversa ma strettamente correlata, hanno avuto performance inferiori ma hanno comunque prodotto alcune blastocisti. Al contrario, i nuclei del babirusa, provenienti da un ramo più distante dell’albero genealogico dei suidi, non hanno mai prodotto blastocisti, arrestandosi prima come piccole sfere di cellule. Questo declino costante nel successo dello sviluppo con l’aumentare della distanza evolutiva evidenzia una barriera pratica talvolta definita «muro tassonomico»: oltre un certo divario tra donatore e ovocita, l’embrione semplicemente non può proseguire.
Una spinta chimica per embrioni arrestati
Il team ha quindi testato se la Scriptaid, un farmaco che allenta il modo in cui il DNA è impacchettato, potesse migliorare queste probabilità. Rendendo il materiale genetico più accessibile, la Scriptaid può, in linea di principio, aiutare a ripristinare un nucleo donatore a uno stato embrionale precoce. Quando i nuclei del maiale barbuto sono stati trattati con Scriptaid dopo il trasferimento in ovociti di maiale domestico, più embrioni hanno raggiunto lo stadio di blastocisti e le loro prime divisioni cellulari si sono verificate prima, avvicinandosi maggiormente a quelle dei cloni di maiale domestico. Il farmaco ha anche aumentato temporaneamente i livelli di un marcatore chimico sulle proteine che impacchettano il DNA (acetilazione di H3K9) durante i primi due stadi cellulari, segno che i loro programmi genetici erano più attivamente attivati. Tuttavia, la Scriptaid non è riuscita a salvare gli embrioni del babirusa, che hanno comunque fallito nel superare lo stadio di morula.
Centrali energetiche e segnali incrociati
Per capire perché la parentela avesse un ruolo tanto importante, gli scienziati hanno esaminato quali geni fossero attivati o disattivati in diversi stadi precoci in tutti i tipi di embrione. Hanno scoperto che molte delle differenze tra embrioni riusciti e in fallimento riguardavano le centrali energetiche della cellula, i mitocondri. I mitocondri portano un loro piccolo insieme di geni ma dipendono fortemente anche dai geni presenti nel nucleo cellulare. Negli embrioni ibridi, nucleo e mitocondri provenivano da specie diverse e la loro comunicazione sembrava vacillare con l’aumentare della distanza evolutiva. Molti dei geni interessati appartenevano a famiglie che costruiscono una parte chiave della catena energetica nota come fosforilazione ossidativa. In accoppiamenti più distanti, questi geni nucleari tendevano a essere meno espressi, mentre in accoppiamenti più prossimi potevano risultare più attivi. Con l’aggiunta della Scriptaid, un altro gruppo di geni mitocondriali — questa volta codificati all’interno degli stessi mitocondri — ha risposto con forza, suggerendo che il farmaco ha parzialmente ritarato questa cooperazione nucleo–mitocondrio. 
Che cosa significa per la salvezza delle specie
Nel complesso, il lavoro mostra che la clonazione interspecifica all’interno della famiglia dei suidi non è solo un esercizio meccanico di scambio del DNA; dipende da una conversazione delicata tra geni nucleari e mitocondriali che si sono evoluti insieme per milioni di anni. Quando donatore e ovocita sono strettamente correlati, questa conversazione può essere tesa ma comunque funzionare a sufficienza per produrre blastocisti, specialmente se aiutata da un farmaco che modifica la cromatina come la Scriptaid. Quando le specie sono più distanti, la discrepanza nella «rete elettrica» cellulare diventa troppo grande e lo sviluppo si arresta nonostante l’assistenza chimica. Per gli sforzi di conservazione, ciò suggerisce che la clonazione interspecifica è più promettente tra specie molto vicine e che le strategie future dovranno affrontare direttamente lo sbilanciamento nella produzione di energia, non solo riprogrammare il nucleo.
Citazione: Liu, HJ., Wong, K.W., Ma, X. et al. Effect of taxonomical distance and scriptaid on iSCNT embryo development in suidae. Sci Rep 16, 11288 (2026). https://doi.org/10.1038/s41598-026-41963-9
Parole chiave: clonazione interspecifica, suini a rischio, mitocondri, sviluppo embrionale, farmaci epigenetici