Clear Sky Science · de
Auswirkungen taxonomischer Entfernung und Scriptaid auf die Entwicklung von iSCNT-Embryonen bei Suidae
Aussterbende Schweine wiederbeleben
Viele Wildschweinarten bewegen sich in Richtung Aussterben, doch Eizellen dieser seltenen Tiere zu sammeln ist schwierig und oft unmöglich. Ein vorgeschlagener Umweg ist eine Art biologische „Leihmutterschaft“: die DNA eines bedrohten Tieres in die Eizelle eines verwandten Nutztieres einzusetzen, in der Hoffnung, im Labor einen Embryo heranzuziehen. Diese Studie untersucht, wie weit sich dieser Ansatz innerhalb der Schweinefamilie anwenden lässt und ob ein kleines Wirkstoffmolekül versteckte Kompatibilitätsprobleme in solchen Hybridembryonen überwinden kann.
Hybride Embryonen im Labor erzeugen
Die Forschenden konzentrierten sich auf Mitglieder der Schweinefamilie Suidae, zu der sowohl die vertrauten Hausschweine als auch scheuere Waldbewohner wie der Bartschwein und das Babirusa gehören. Mit einer Technik namens somatischer Zellkerntransfer entfernten sie das genetische Material aus Eizellen von Hausschweinen und ersetzten es durch Kerne aus Hautzellen aus drei Quellen: Hausschwein (als Referenz), Bartschwein (eine andere, aber eng verwandte Art derselben Gattung) und Babirusa (ein entfernterer Verwandter aus einer anderen Unterfamilie). Alle Embryonen entwickelten sich in derselben Umgebung der Hausschwein-Eizelle, sodass das Team den Einfluss der Verwandtschaftsnahheit zwischen Spender und Eizelle isolieren konnte. 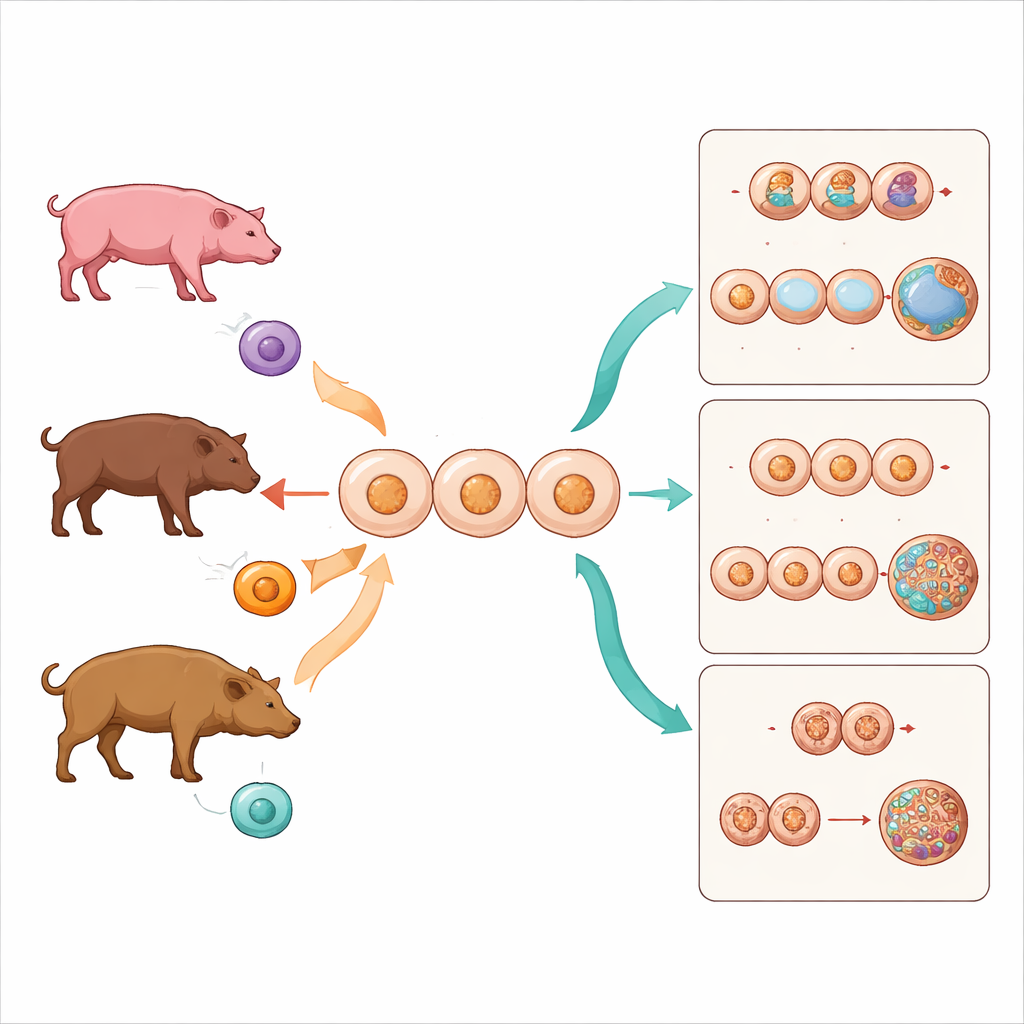
Wenn Verwandtschaft die Lebenswahrscheinlichkeit bestimmt
Das Ergebnis war eindeutig. Aus Hausschwein-Kernen in Hausschwein-Eizellen erzeugte Embryonen hatten den größten Erfolg: mehr als ein Viertel erreichte das Blastozystenstadium, einen fortgeschrittenen Punkt, der für die Einnistung geeignet ist. Kerne des Bartschweins, die aus einer anderen, aber eng verwandten Art stammen, schnitten schlechter ab, erzeugten jedoch noch einige Blastozysten. Im Gegensatz dazu produzierten Babirusa-Kerne, die aus einem weiter entfernten Zweig des Schweinefamilienstammbaums stammen, überhaupt keine Blastozysten, sondern blieben früher als kleine Zellkugeln stehen. Dieser stetige Rückgang der Entwicklungs‑Erfolge mit zunehmender evolutionärer Distanz macht eine praktische Barriere deutlich, die manchmal als „taxonomische Wand“ bezeichnet wird: jenseits einer bestimmten Lücke zwischen Spender und Eizelle kann der Embryo schlichtweg nicht weiterentwickeln.
Ein chemischer Schubs für stecken gebliebene Embryonen
Das Team prüfte anschließend, ob Scriptaid, ein Wirkstoff, der die Verpackung der DNA lockert, diese Chancen verbessern kann. Indem das genetische Material zugänglicher gemacht wird, kann Scriptaid theoretisch helfen, einen Spenderkern wieder in einen frühen embryonalen Zustand zurückzusetzen. Wenn Bartschwein-Kerne nach dem Transfer in Hausschwein-Eizellen mit Scriptaid behandelt wurden, erreichten mehr Embryonen das Blastozystenstadium, und ihre frühen Zellteilungen erfolgten schneller, näher an denen von Hausschwein-Klonen. Der Wirkstoff erhöhte außerdem vorübergehend die Werte einer chemischen Markierung an den DNA-verpackenden Proteinen (H3K9-Acetylierung) in den ersten beiden Zellstadien, ein Hinweis darauf, dass ihre genetischen Programme aktiver eingeschaltet waren. Scriptaid konnte jedoch die weiter entfernten Babirusa-Embryonen nicht retten, die weiterhin am Morula‑Stadium scheiterten.
Energiezentralen und überkreuzte Signale
Um zu verstehen, warum Verwandtschaft so wichtig war, untersuchten die Wissenschaftler, welche Gene in mehreren frühen Stadien bei allen Embryotypen an- oder abgeschaltet wurden. Sie stellten fest, dass viele der Unterschiede zwischen erfolgreichen und scheiternden Embryonen die Energieanlagen der Zelle, die Mitochondrien, betrafen. Mitochondrien tragen einen eigenen kleinen Satz von Genen, sind aber stark von Genen im Zellkern abhängig. In den Hybridembryonen stammten Kern und Mitochondrien aus unterschiedlichen Arten, und ihre Kommunikation schien mit wachsender evolutionärer Distanz zu stocken. Viele betroffene Gene gehörten zu Familien, die einen Schlüsselteil der Energiekette aufbauen, bekannt als oxidative Phosphorylierung. Bei weiter entfernten Paarungen waren diese Kern‑kodierten Gene tendenziell heruntergeregelt, während sie bei näher verwandten Paarungen hochgeregelt werden konnten. Als Scriptaid hinzugefügt wurde, reagierte eine andere Gruppe von mitochondrienkodierten Genen stark, was darauf hindeutet, dass das Medikament diese Kern‑Mitochondrien‑Partnerschaft teilweise umgestimmt hat. 
Was das für den Artenschutz bedeutet
In der Summe zeigt die Arbeit, dass interspezifisches Klonen innerhalb der Schweinefamilie nicht nur ein mechanischer Austausch von DNA ist; es beruht auf einem empfindlichen Zusammenspiel zwischen Kern‑ und Mitochondriengenen, das über Millionen von Jahren gemeinsam evolviert ist. Wenn Spender und Eizelle eng verwandt sind, kann dieses Zusammenspiel zwar belastet sein, funktioniert aber oft noch ausreichend, um Blastozysten zu erzeugen — insbesondere wenn ein chromatinmodifizierender Wirkstoff wie Scriptaid hilft. Bei weiter entfernten Arten wird die Diskrepanz im zellulären „Stromnetz“ jedoch zu groß, und die Entwicklung bleibt trotz chemischer Unterstützung stehen. Für Schutzmaßnahmen bedeutet dies, dass interspezifisches Klonen am vielversprechendsten zwischen sehr eng verwandten Arten ist und dass künftige Strategien direkt das Missverhältnis in der Energieproduktion angehen müssen, nicht nur die Reprogrammierung des Kerns.
Zitation: Liu, HJ., Wong, K.W., Ma, X. et al. Effect of taxonomical distance and scriptaid on iSCNT embryo development in suidae. Sci Rep 16, 11288 (2026). https://doi.org/10.1038/s41598-026-41963-9
Schlüsselwörter: interspezifisches Klonen, gefährdete Schweine, Mitochondrien, Embryonalentwicklung, epigenetische Wirkstoffe