Clear Sky Science · pl
Skalowalna synteza w przepływie ultraskutecznych nieorganicznych nanocząstek do zastosowań biomedycznych za pomocą zamkniętego miksera z zderzającymi się dyszami
Dlaczego maleńkie cząstki mogą mieć duże znaczenie
Szpitale coraz częściej polegają na mikroskopijnych cząstkach, by wcześniej wykrywać choroby, dostarczać leki precyzyjniej i zwalczać uporczywe infekcje. Jednak wytwarzanie tych cząstek w dużych, jednorodnych partiach okazuje się zaskakująco trudne — często wymaga wysokiej temperatury, agresywnych chemikaliów i skomplikowanego sprzętu. Niniejsze badanie przedstawia prostą, wodną metodę produkcji, która może wytwarzać jednorodne, ultraszczupłe cząstki odpowiednie do zastosowań medycznych, potencjalnie ułatwiając przejście od odkryć laboratoryjnych do praktycznych terapii i narzędzi do obrazowania. 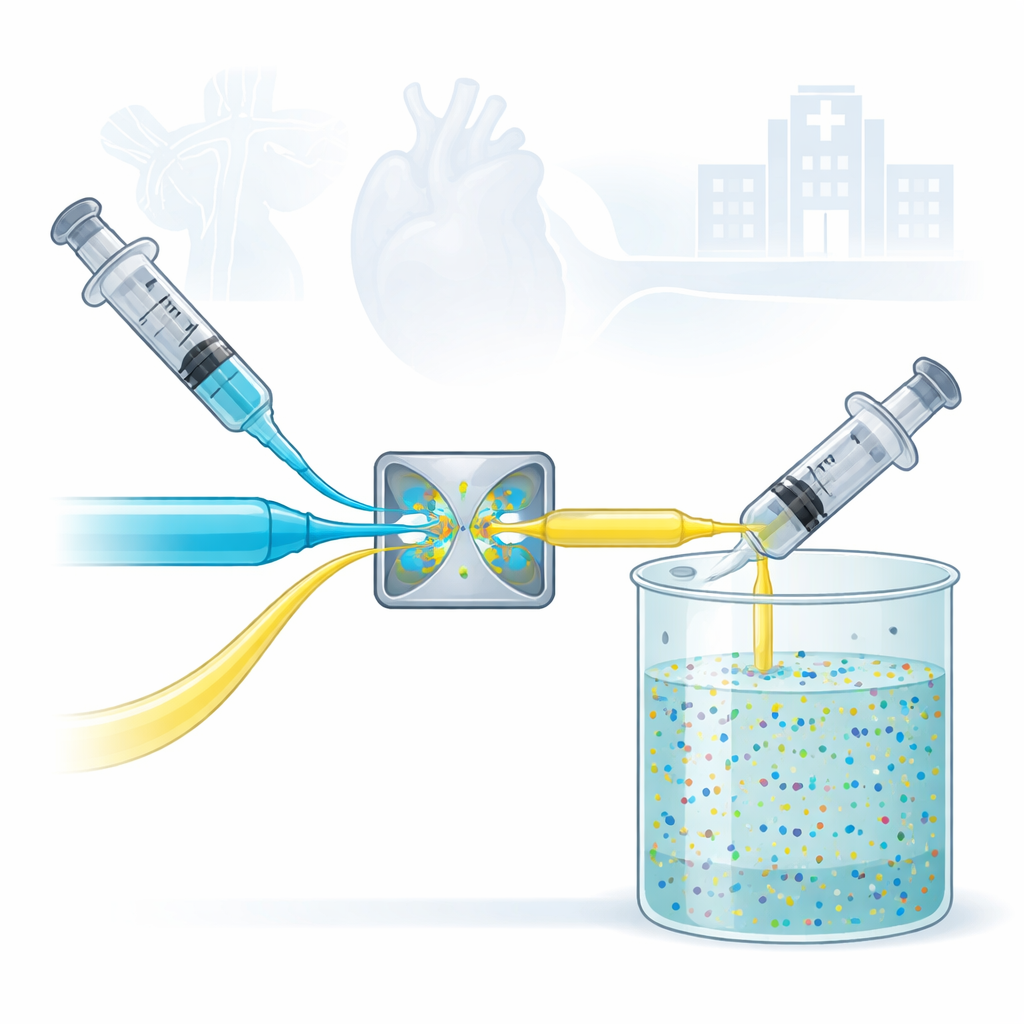
Nowy sposób mieszania na najmniejszych skalach
Rdzeniem pracy jest urządzenie zwane zamkniętym mikserem z zderzającymi się dyszami (CIJM). Wygląda niepozornie: dwa strumienie cieczy są wtłaczane naprzeciw siebie i zderzają się czołowo w małej komorze. To gwałtowne, lecz precyzyjnie kontrolowane zderzenie natychmiast miesza składniki i powoduje tworzenie się malutkich nieorganicznych cząstek w procesie zwanym szybką precypitacją. W przeciwieństwie do wielu tradycyjnych metod, cała reakcja przebiega w wodzie w temperaturze pokojowej, bez toksycznych rozpuszczalników organicznych, specjalnych atmosfer gazowych czy długich etapów ogrzewania. Czynni to podejście zarówno bezpieczniejszym, jak i łatwiejszym do skalowania do produkcji przemysłowej.
Produkcja czterech typów przydatnych nanocząstek
Wykorzystując ten pojedynczy projekt miksera, zespół wytworzył cztery różne rodzaje nanocząstek, z których każdy ma obiecujące zastosowanie medyczne. Siarczek srebra i tellurek srebra mogą działać jako jasne środki kontrastowe do badań rentgenowskich, takich jak mammografia i tomografia komputerowa. Tlenek ceru zachowuje się jak drobne przeciwutleniacz, pochłaniając reaktywne cząsteczki tlenu, które przyczyniają się do zapalenia i uszkodzeń tkanek. Tlenek żelaza ma własności magnetyczne i katalityczne, co czyni go użytecznym zarówno jako środek obrazujący, jak i pomocnik w rozkładaniu szkodliwych biofilmów bakteryjnych. Wszystkie cztery typy okazały się ekstremalnie małe — zazwyczaj od jednego do pięciu miliardowych metra średnicy — i zostały pokryte biokompatybilnymi cząsteczkami, aby utrzymać stabilność w organizmie.
Regulacja rozmiaru i kształtu jak pokrętło
Dla wielu zastosowań medycznych dokładny rozmiar cząstki ma znaczenie. Mniejsze cząstki mogą przechodzić przez nerki i być usuwane z organizmu, zmniejszając długoterminowe nagromadzenie w narządach, a rozmiar wpływa też na to, jak silnie widoczne są w skanach lub jak katalizują reakcje. Badacze systematycznie dopracowywali prędkości przepływu cieczy, stężenia składników oraz sposoby mieszania i rozcieńczania po utworzeniu. W przypadku siarczku srebra prosta zmiana stosunku napływających strumieni składników zmieniła średnicę cząstek z około dwóch do nieco ponad pięciu nanometrów bez pogorszenia jakości. Tellurek srebra reagował natomiast na siłę czynnika oddającego elektrony oraz na szybkość rozcieńczenia produktu po zmieszaniu. Cząstki tlenku żelaza wykazywały tylko niewielkie zmiany rozmiaru jądra, ale ich ogólny rozmiar „chmury” w wodzie — kluczowy dla sposobu, w jaki przemieszczają się w organizmie — można było dostroić w szerokim zakresie. Tlenek ceru był mniej podatny na regulację rozmiaru, lecz nadal można go było wytwarzać niezawodnie w temperaturze pokojowej. 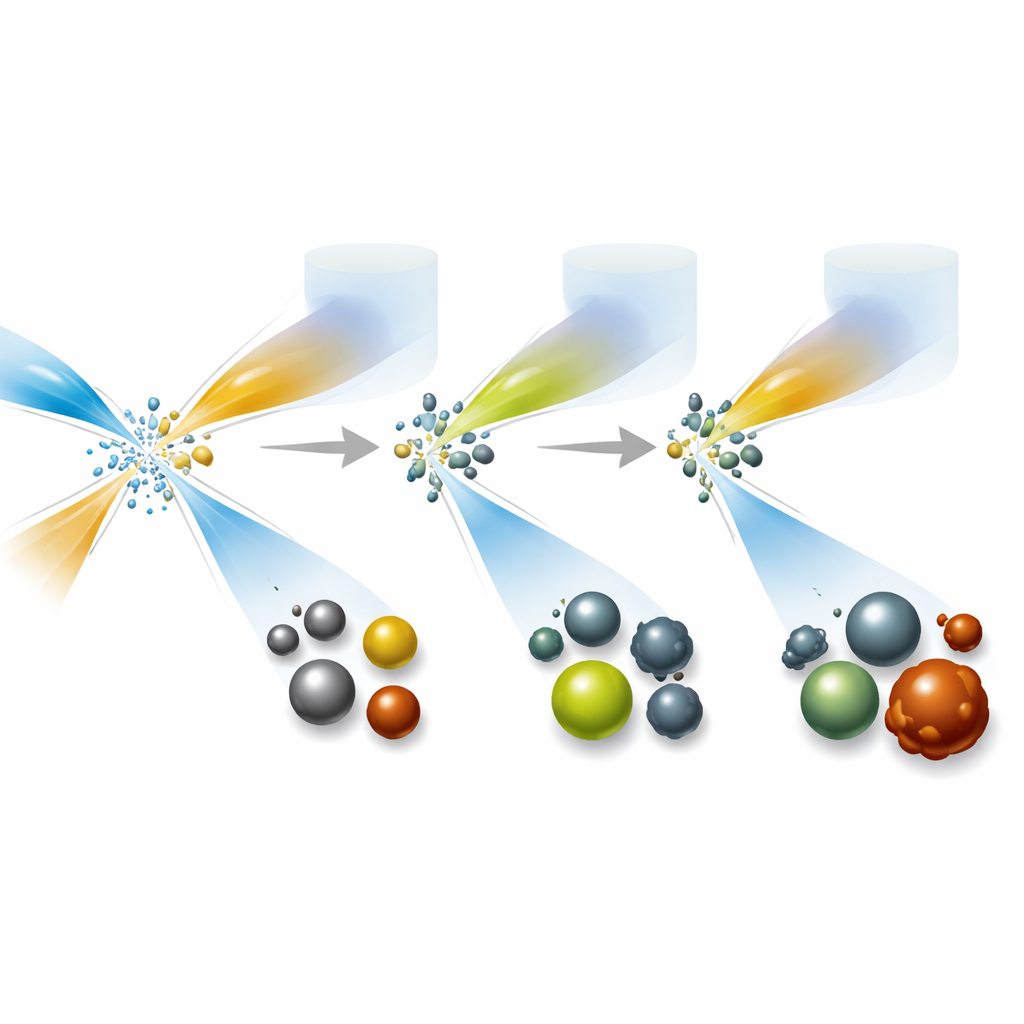
Dowód działania w testach zbliżonych do rzeczywistych
Wyprodukowanie cząstek to jedno; udowodnienie, że rzeczywiście sprawdzają się w użytecznych zastosowaniach, to co innego. W fantomach do obrazowania naśladujących tkanki ludzkie, obie cząstki na bazie srebra dały silniejszy kontrast rentgenowski niż powszechnie stosowany barwnik jodowy, co oznacza, że mogą pomóc radiologom lepiej dostrzegać subtelne cechy przy tym samym dawkowaniu metalu. Cząstki tlenku ceru chroniły hodowane komórki ludzkie przed szkodliwymi impulsami nadtlenku wodoru, działając jak miniaturowe enzymy przeciwutleniające. Cząstki tlenku żelaza współdziałały z nadtlenkiem wodoru, szybko zabijając bakterie jamy ustnej żyjące w odpornych warstwach ochronnych, co sugeruje możliwość wzmocnienia terapii próchnicy i innych zakażeń jamy ustnej. W tych testach nowe cząstki dorównywały lub przewyższały działanie wersji wytwarzanych bardziej skomplikowanymi metodami.
Od stołu laboratoryjnego do produkcji bez utraty jakości
Częstą przeszkodą w nanomedycynie jest to, że procesy działające w małych probówkach zawodzą przy skalowaniu do partii fabrycznych. Zespół wykazał, że ich mikser może to przezwyciężyć. Zwiększając prędkość przepływu i objętości roztworów wyjściowych, wyprodukowali około litra zawiesiny nanocząstek siarczku srebra w zaledwie piętnaście minut — to około sto razy większa skala. Pomiary rozmiaru, struktury i właściwości optycznych wykazały, że cząstki z dużych partii były prawie nieodróżnialne od tych wytwarzanych na małą skalę. Ponieważ CIJM jest dostępny komercyjnie, stosunkowo niedrogi i odporny na zapychanie, może zostać przyjęty bez konieczności tworzenia niestandardowych rozwiązań inżynieryjnych.
Co to może znaczyć dla medycyny przyszłości
Mówiąc prosto, badanie demonstruje praktyczną „linię montażową” do wytwarzania bardzo małych, medycznie użytecznych cząstek w wodzie, w temperaturze pokojowej i w dużych ilościach. Zamknięty mikser z zderzającymi się dyszami można dostroić do produkcji kilku rodzajów nieorganicznych nanocząstek, które zachowują zamierzone właściwości — czy to jasny kontrast rentgenowski, ochrona przeciwutleniająca, czy zdolność zabijania bakterii — przy jednoczesnym zachowaniu rozmiarów wystarczających do bezpiecznego usuwania z organizmu. Tego rodzaju niezawodna, skalowalna technologia produkcyjna jest kluczowym brakującym ogniwem między obiecującymi odkryciami w nanomedycynie a rutynowymi narzędziami stosowanymi w klinikach i może przyspieszyć pojawienie się bardziej precyzyjnych środków obrazujących i terapii ukierunkowanych.
Cytowanie: Kian, A.C., Gupta, M., Hong, H. et al. Scalable flow synthesis of ultrasmall inorganic nanoparticles for biomedical applications via a confined impinging jet mixer. Sci Rep 16, 11135 (2026). https://doi.org/10.1038/s41598-026-41509-z
Słowa kluczowe: nanocząstki, obrazowanie biomedyczne, mikrofluidyka, dostawa leków, terapia przeciwdrobnoustrojowa