Clear Sky Science · it
Sintesi di flusso scalabile di nanoparticelle inorganiche ultrasmall per applicazioni biomediche tramite un miscelatore a getto confinato
Perché le particelle piccolissime potrebbero fare la differenza
Gli ospedali fanno sempre più affidamento su particelle microscopiche per individuare le malattie prima, somministrare farmaci con maggiore precisione e combattere infezioni ostinate. Tuttavia, produrre queste particelle in lotti grandi e omogenei si è rivelato sorprendentemente difficile, spesso richiedendo alte temperature, sostanze chimiche aggressive e apparecchiature complesse. Questo studio presenta un metodo di produzione semplice a base d’acqua in grado di generare particelle ultrasmall uniformi adatte all’uso medico, facilitando potenzialmente il passaggio dalla scoperta in laboratorio a trattamenti e strumenti di imaging utilizzabili nella pratica clinica. 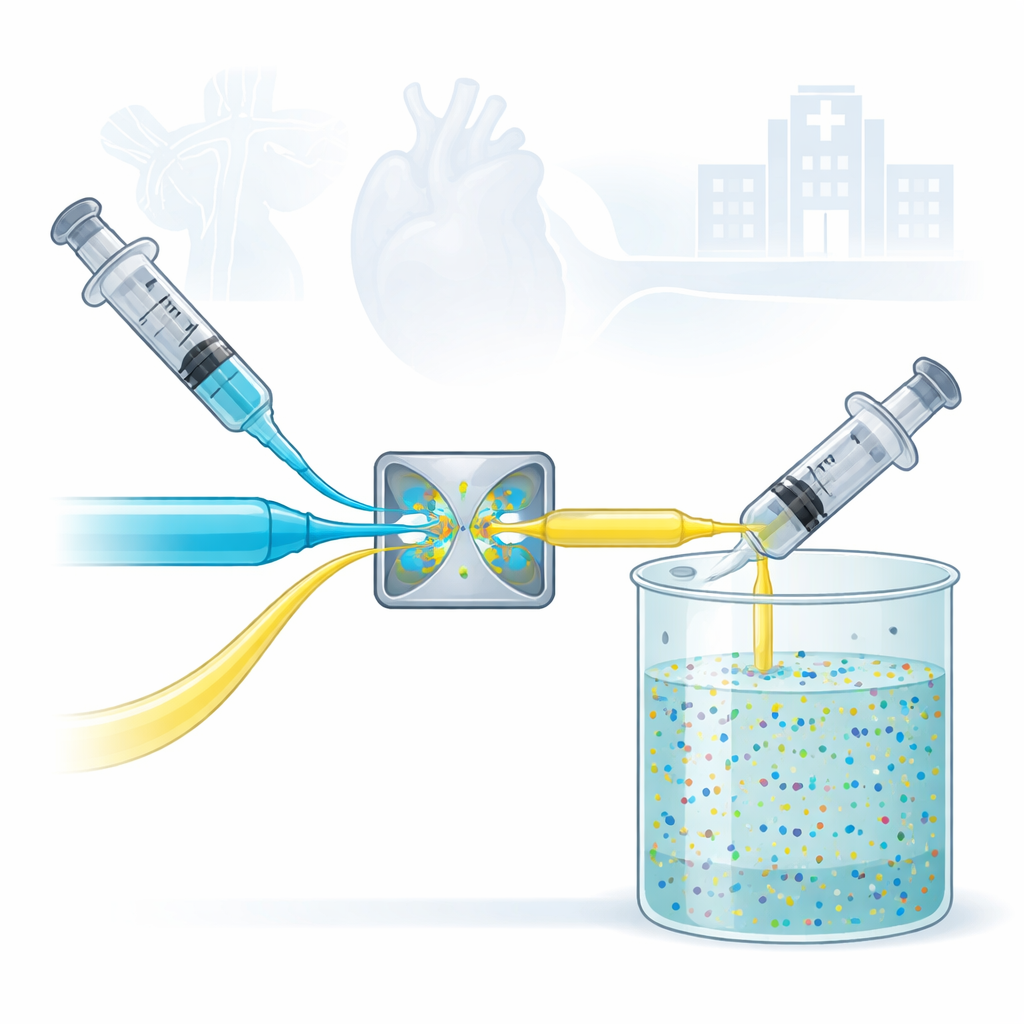
Un nuovo modo di mescolare alle scale più minute
Il cuore del lavoro è un dispositivo chiamato miscelatore a getto confinato, o CIJM. Ha un aspetto semplice: due flussi liquidi sono spinti l’uno contro l’altro e collidono frontalmente all’interno di una piccola camera. Questa collisione violenta ma controllata miscela istantaneamente gli ingredienti e provoca la formazione di piccole particelle inorganiche in un processo noto come precipitazione lampo. Diversamente da molti metodi tradizionali, l’intera reazione avviene in acqua a temperatura ambiente, senza solventi organici tossici, atmosfere gassose speciali o lunghe fasi di riscaldamento. Ciò rende l’approccio sia più sicuro sia più facile da scalare per la produzione industriale.
Costruire quattro tipi di nanoparticelle utili
Utilizzando questo singolo progetto di miscelatore, il team ha prodotto quattro diversi tipi di nanoparticelle, ognuna con promettenti applicazioni mediche. Le particelle di solfuro di argento e tellururo di argento possono fungere da agenti di contrasto brillanti per esami a raggi X come la mammografia e la tomografia computerizzata. Le particelle di ossido di cerio si comportano come piccoli antiossidanti, eliminando molecole reattive dell’ossigeno che contribuiscono a infiammazione e danno tissutale. Le particelle di ossido di ferro sono magnetiche e catalitiche, rendendole utili sia come agenti di imaging sia come aiuti nella degradazione di biofilm batterici dannosi. Tutti e quattro i tipi risultano estremamente piccoli—tipicamente tra uno e cinque miliardesimi di metro di diametro—e sono rivestiti con molecole biocompatibili per mantenerli stabili nell’organismo.
Regolare dimensione e forma come una manopola di controllo
Per molti usi medici, la dimensione esatta di una particella è importante. Particelle più piccole possono passare attraverso i reni ed essere eliminate dall’organismo, riducendo l’accumulo a lungo termine negli organi, mentre la dimensione influisce anche su quanto appaiono nelle immagini o sulla loro attività catalitica. I ricercatori hanno regolato sistematicamente la velocità dei flussi, la concentrazione degli ingredienti e le modalità di miscelazione o diluizione dopo la formazione. Per le particelle di solfuro di argento, basta modificare il rapporto dei flussi in ingresso per cambiare il diametro delle particelle da circa due a poco oltre cinque nanometri senza compromettere la qualità. Le particelle di tellururo di argento invece rispondevano alla forza di un donatore di elettroni e alla rapidità con cui il prodotto veniva diluito dopo la miscelazione. Le particelle di ossido di ferro mostrarono solo variazioni modeste nelle dimensioni del nucleo, ma la loro dimensione complessiva «a nuvola» in acqua—una caratteristica chiave per il modo in cui si spostano nell’organismo—poteva essere regolata su un ampio intervallo. Le particelle di ossido di cerio erano meno adattabili in termini di dimensione, ma potevano comunque essere prodotte in modo affidabile a temperatura ambiente. 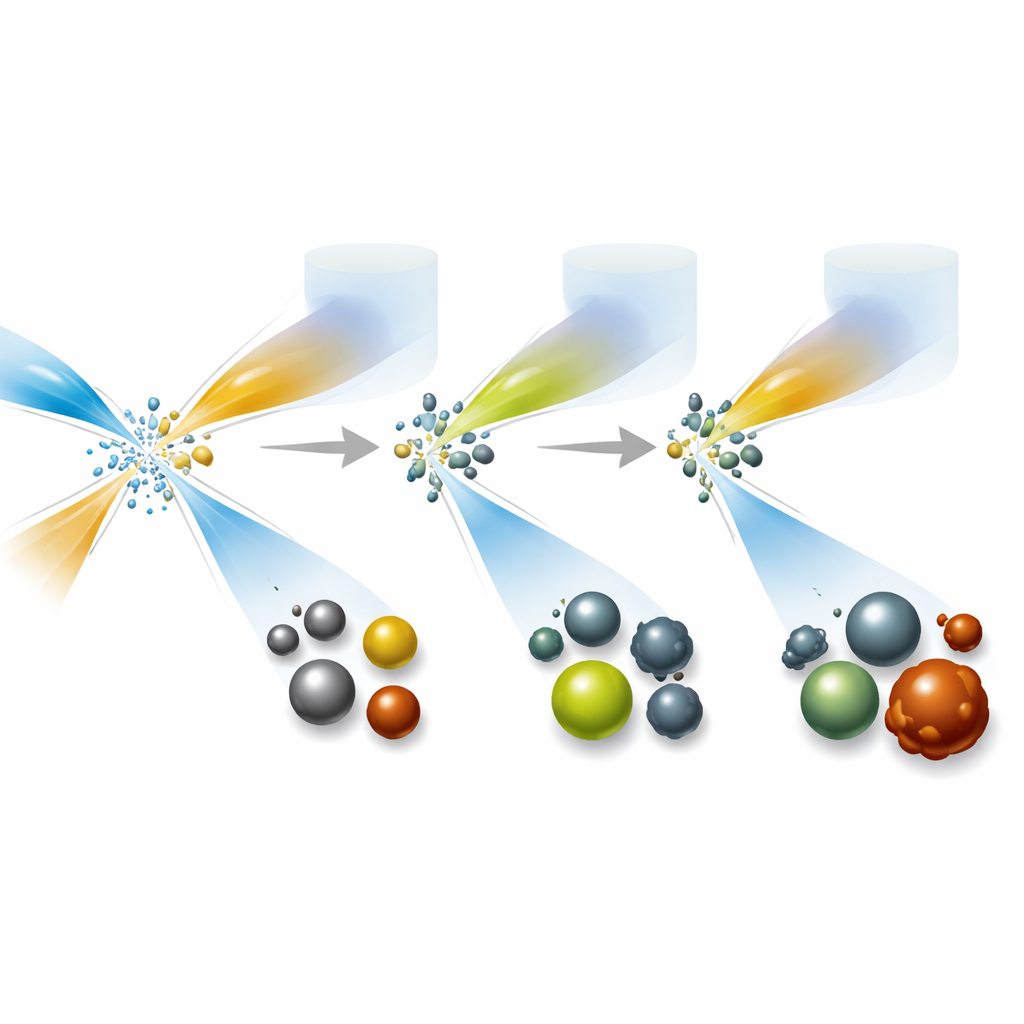
Dimostrare l’efficacia in test realistici
Produrre particelle è una cosa; dimostrare che funzionano in modo utile è un’altra. In fantocci per imaging che imitano il tessuto umano, entrambe le particelle a base di argento hanno fornito un contrasto a raggi X più forte rispetto a un comune mezzo di contrasto a base di iodio, il che significa che potrebbero aiutare i radiologi a vedere dettagli sottili più chiaramente allo stesso dosaggio di metallo. Le particelle di ossido di cerio hanno protetto cellule umane coltivate da scoppi altrimenti dannosi di perossido di idrogeno, agendo come minuscoli enzimi antiossidanti. Le particelle di ossido di ferro hanno collaborato con il perossido di idrogeno per uccidere rapidamente batteri orali che vivevano in film protettivi resistenti, suggerendo un modo per migliorare i trattamenti per la carie e altre infezioni orali. In questi test, le nuove particelle hanno eguagliato o superato le prestazioni di versioni realizzate con metodi più complicati.
Dal banco di laboratorio al secchio senza perdere qualità
Un ostacolo frequente nella nanomedicina è che processi che funzionano in provette piccole falliscono quando si scala a lotti di dimensioni industriali. Il team ha dimostrato che il loro miscelatore può superare questo problema. Aumentando la portata e i volumi delle soluzioni di partenza, hanno prodotto circa un litro di sospensione di nanoparticelle di solfuro di argento in soli quindici minuti—una scalabilità di circa cento volte. Le misure di dimensione, struttura e proprietà ottiche hanno rivelato che le particelle del lotto grande erano quasi indistinguibili da quelle realizzate su piccola scala. Poiché il CIJM è disponibile in commercio, relativamente economico e resistente all’intasamento, potrebbe essere adottato senza progettazioni personalizzate.
Cosa potrebbe significare per la medicina futura
In termini semplici, lo studio dimostra una «catena di montaggio» pratica per produrre particelle molto piccole e utili in ambito medico in acqua, a temperatura ambiente e in grandi quantità. Il miscelatore a getto confinato può essere messo a punto per produrre diversi tipi di nanoparticelle inorganiche che mantengono le proprietà desiderate—che si tratti di forte contrasto a raggi X, protezione antiossidante o potere battericida—pur rimanendo abbastanza piccole da poter essere eliminate in sicurezza dall’organismo. Questo tipo di tecnologia di produzione affidabile e scalabile è un elemento chiave mancante tra le promesse della nanomedicina e gli strumenti di uso routinario in clinica, e potrebbe accelerare l’arrivo di agenti di imaging più precisi e terapie mirate.
Citazione: Kian, A.C., Gupta, M., Hong, H. et al. Scalable flow synthesis of ultrasmall inorganic nanoparticles for biomedical applications via a confined impinging jet mixer. Sci Rep 16, 11135 (2026). https://doi.org/10.1038/s41598-026-41509-z
Parole chiave: nanoparticelle, imaging biomedico, microfluidica, consegna di farmaci, terapia antimicrobica