Clear Sky Science · fr
Synthèse en flux évolutive de nanoparticules inorganiques ultrasmall pour applications biomédicales via un mélangeur à jets confinés
Pourquoi de très petites particules pourraient faire une grande différence
Les hôpitaux s’appuient de plus en plus sur des particules microscopiques pour détecter les maladies plus tôt, délivrer des médicaments de façon plus précise et combattre des infections tenaces. Mais produire ces particules en lots importants et homogènes s’est avéré étonnamment difficile, nécessitant souvent de fortes chaleurs, des produits chimiques agressifs et des équipements complexes. Cette étude présente une méthode de production simple à base d’eau capable de fabriquer des particules ultrasmall et uniformes adaptées à un usage médical, facilitant potentiellement le passage de la découverte en laboratoire aux traitements et outils d’imagerie en conditions réelles. 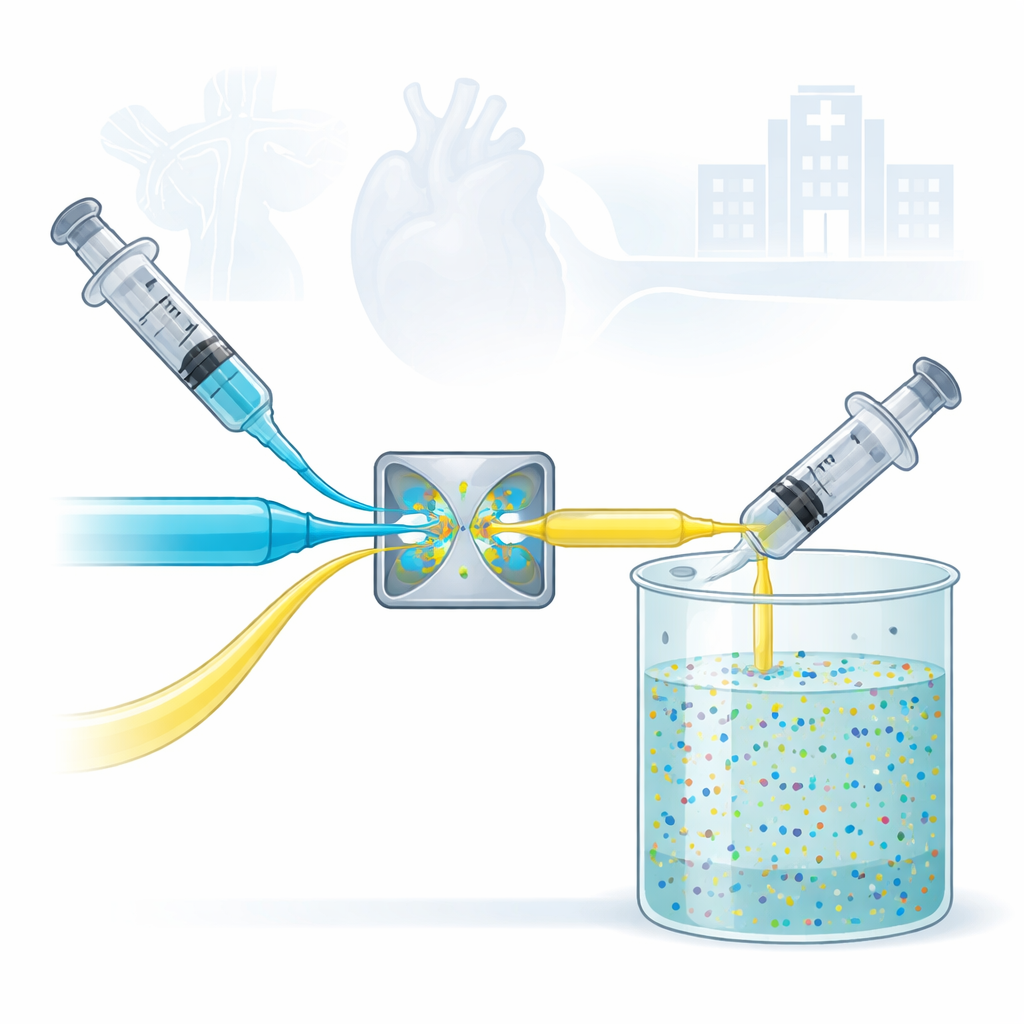
Une nouvelle façon de mélanger à l’échelle la plus petite
Le cœur du travail est un dispositif appelé mélangeur à jets confinés, ou CIJM. Il a l’air modeste : deux flux liquides sont poussés l’un vers l’autre et entrent en collision frontale dans une petite chambre. Cette collision violente mais précisément contrôlée mélange instantanément les ingrédients et provoque la formation de petites particules inorganiques dans un processus appelé précipitation éclair. Contrairement à de nombreuses méthodes traditionnelles, toute la réaction se déroule dans l’eau à température ambiante, sans solvants organiques toxiques, atmosphères gazeuses particulières ni longues étapes de chauffage. Cela rend l’approche à la fois plus sûre et plus facile à industrialiser.
Fabrication de quatre types de nanoparticules utiles
Avec ce seul design de mélangeur, l’équipe a produit quatre types différents de nanoparticules, chacune présentant un intérêt médical. Les particules de sulfure d’argent et de tellurure d’argent peuvent servir d’agents de contraste brillants pour les examens à rayons X comme la mammographie et la tomodensitométrie. Les particules d’oxyde de cérium se comportent comme de minuscules antioxydants, éliminant les molécules réactives de l’oxygène qui contribuent à l’inflammation et aux lésions tissulaires. Les particules d’oxyde de fer sont magnétiques et catalytiques, ce qui les rend utiles à la fois comme agents d’imagerie et comme assistantes pour décomposer les biofilms bactériens nocifs. Les quatre types étaient extrêmement petits — généralement entre un et cinq milliardièmes de mètre — et étaient recouverts de molécules biocompatibles pour rester stables dans l’organisme.
Régler la taille et la forme comme un bouton de commande
Pour de nombreuses applications médicales, la taille exacte d’une particule a de l’importance. Les particules plus petites peuvent passer par les reins et être éliminées de l’organisme, réduisant l’accumulation à long terme dans les organes, tandis que la taille influence aussi leur visibilité en imagerie ou leur activité catalytique. Les chercheurs ont ajusté systématiquement la vitesse d’écoulement des fluides, la concentration des ingrédients et la façon dont ils étaient mélangés ou dilués après formation. Pour les particules de sulfure d’argent, il suffisait de modifier le ratio des flux entrants pour faire varier le diamètre des particules d’environ deux à un peu plus de cinq nanomètres sans altérer la qualité. Les particules de tellurure d’argent répondaient plutôt à la force d’un donneur d’électrons et à la rapidité de dilution après le mélange. Les particules d’oxyde de fer ont montré seulement de modestes changements de taille du cœur, mais leur taille globale en suspension — un élément clé de leur comportement dans l’organisme — pouvait être ajustée sur une large plage. Les particules d’oxyde de cérium étaient moins modulables en taille, mais pouvaient néanmoins être produites de façon fiable à température ambiante. 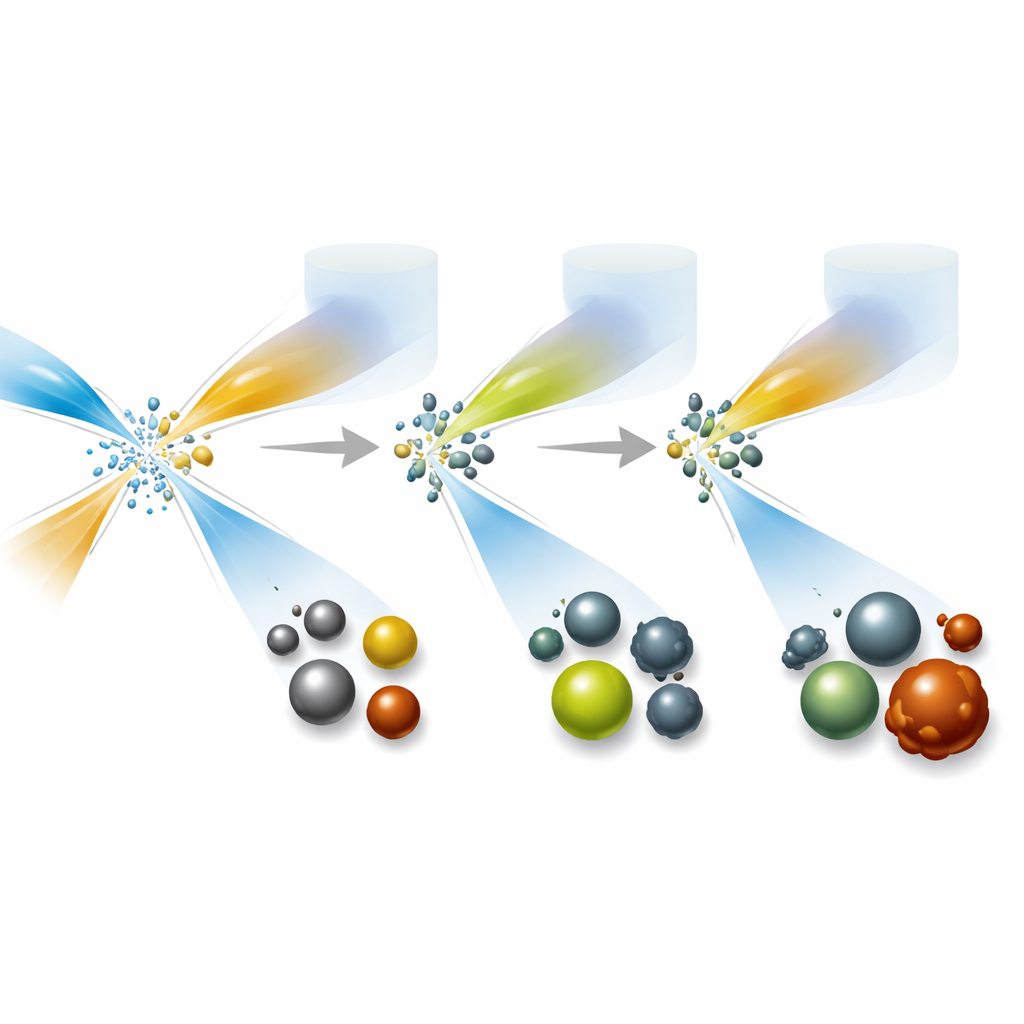
Preuves de fonctionnement dans des tests réalistes
Fabriquer des particules est une chose ; démontrer qu’elles fonctionnent réellement en est une autre. Dans des fantômes d’imagerie mimant les tissus humains, les particules à base d’argent ont produit un contraste aux rayons X plus fort qu’un colorant à base d’iode largement utilisé, ce qui signifie qu’elles pourraient aider les radiologues à mieux visualiser des détails subtils avec la même dose de métal. Les particules d’oxyde de cérium ont protégé des cellules humaines cultivées contre des attaques par du peroxyde d’hydrogène autrement dommageables, agissant comme de minuscules enzymes antioxydantes. Les particules d’oxyde de fer, associées au peroxyde d’hydrogène, ont rapidement tué des bactéries buccales vivant dans des films protecteurs épais, suggérant une voie pour améliorer les traitements de la carie et d’autres infections orales. Dans ces tests, les nouvelles particules égalent ou dépassent les performances de versions fabriquées par des méthodes plus complexes.
Du plan de travail au seau sans perte de qualité
Un obstacle fréquent en nanomédecine est que les procédés qui fonctionnent dans de petits flacons échouent lorsqu’on les transpose à des lots industriels. L’équipe a montré que leur mélangeur peut surmonter ce problème. En augmentant le débit et les volumes de solutions de départ, ils ont produit environ un litre de suspension de nanoparticules de sulfure d’argent en seulement quinze minutes — une mise à l’échelle d’environ cent fois. Les mesures de taille, de structure et des propriétés optiques ont révélé que les particules en grand volume étaient quasi indiscernables de celles fabriquées à petite échelle. Parce que le CIJM est disponible dans le commerce, relativement peu coûteux et résistant à l’encrassement, il pourrait être adopté sans ingénierie sur mesure.
Ce que cela pourrait signifier pour la médecine de demain
En termes clairs, l’étude démontre une « chaîne de montage » pratique pour fabriquer des particules très petites et utiles médicalement, dans l’eau, à température ambiante et en grandes quantités. Le mélangeur à jets confinés peut être ajusté pour produire plusieurs types de nanoparticules inorganiques qui conservent leurs propriétés voulues — qu’il s’agisse d’un contraste X lumineux, d’une protection antioxydante ou d’un pouvoir bactéricide — tout en restant suffisamment petites pour être éliminées en toute sécurité de l’organisme. Ce type de technologie de production fiable et évolutive est un maillon clé manquant entre les découvertes prometteuses en nanomédecine et les outils de routine utilisés en clinique, et il pourrait accélérer l’arrivée d’agents d’imagerie plus précis et de thérapies ciblées.
Citation: Kian, A.C., Gupta, M., Hong, H. et al. Scalable flow synthesis of ultrasmall inorganic nanoparticles for biomedical applications via a confined impinging jet mixer. Sci Rep 16, 11135 (2026). https://doi.org/10.1038/s41598-026-41509-z
Mots-clés: nanoparticules, imagerie biomédicale, microfluidique, administration de médicaments, thérapie antimicrobienne