Clear Sky Science · pl
Wielofunkcyjne hierarchiczne struktury Ni2CoS4 do zwalczania odpornych na leki infekcji i raka jelita grubego poprzez piezokatalityczne wytwarzanie ROS
Dlaczego to nowe podejście do trudnych infekcji i raka ma znaczenie
Infekcje oporne na antybiotyki i rak jelita grubego należą do największych zagrożeń dla zdrowia współczesnego społeczeństwa, a leczenie obu staje się coraz trudniejsze przy użyciu dostępnych leków. W tym badaniu zbadano zupełnie inne podejście terapeutyczne: drobne cząstki siarczku niklu i kobaltu, które aktywują się pod wpływem delikatnego ultradźwięku. Zamiast działać jak klasyczny lek, cząstki te przekształcają energię mechaniczną w impulsy reaktywnych cząsteczek, które mogą rozrywać bakterie, biofilmy i komórki nowotworowe — przy jednoczesnym względnym oszczędzeniu zdrowych komórek w praktycznych dawkach.
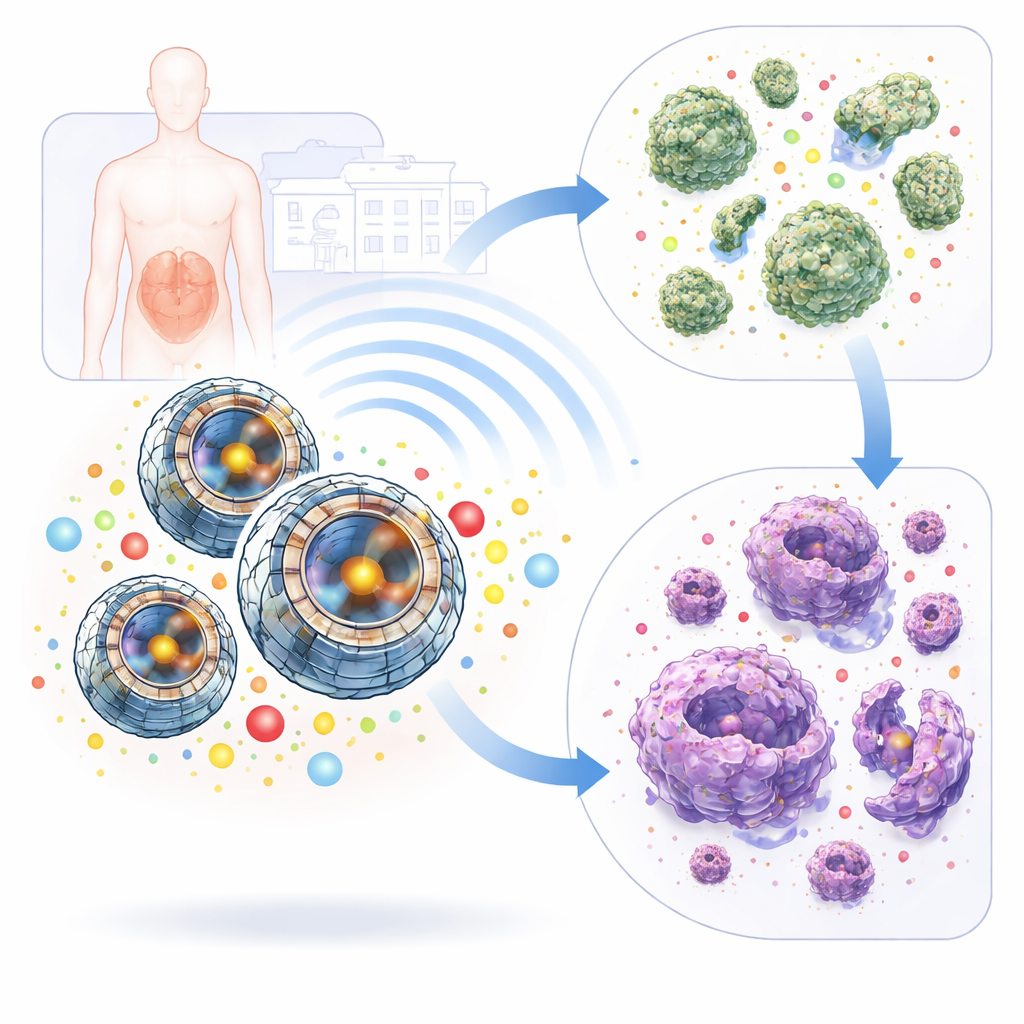
Małe zaprojektowane kule o warstwowej budowie
Naukowcy stworzyli rodzinę cząstek siarczku niklu–kobaltu (Ni₂CoS₄) przy użyciu kontrolowanego procesu ogrzewania w cieczy, następnie systematycznie zmieniali czas, temperaturę i proporcje składników, aby dostroić ich strukturę. Mikroskopia wykazała, że najlepsza formulacja, nazwana N3, tworzy niemal jednorodne puste kule z cienkich, zazębiających się nanosheetów, przypominające luźno utkaną kulę. Pomiary rentgenowskie i Ramana pokazały, że N3 jest także wysoko krystaliczny i chemicznie uporządkowany, a testy adsorpcji gazu potwierdziły, że ma stosunkowo dużą powierzchnię wewnętrzną. Te cechy razem oznaczają, że N3 może efektywnie przemieszczać ładunki elektryczne wewnątrz siebie i eksponować wiele aktywnych miejsc na zewnątrz — oba aspekty kluczowe dla jego nietypowego mechanizmu działania.
Przekształcanie dźwięku w atak chemiczny
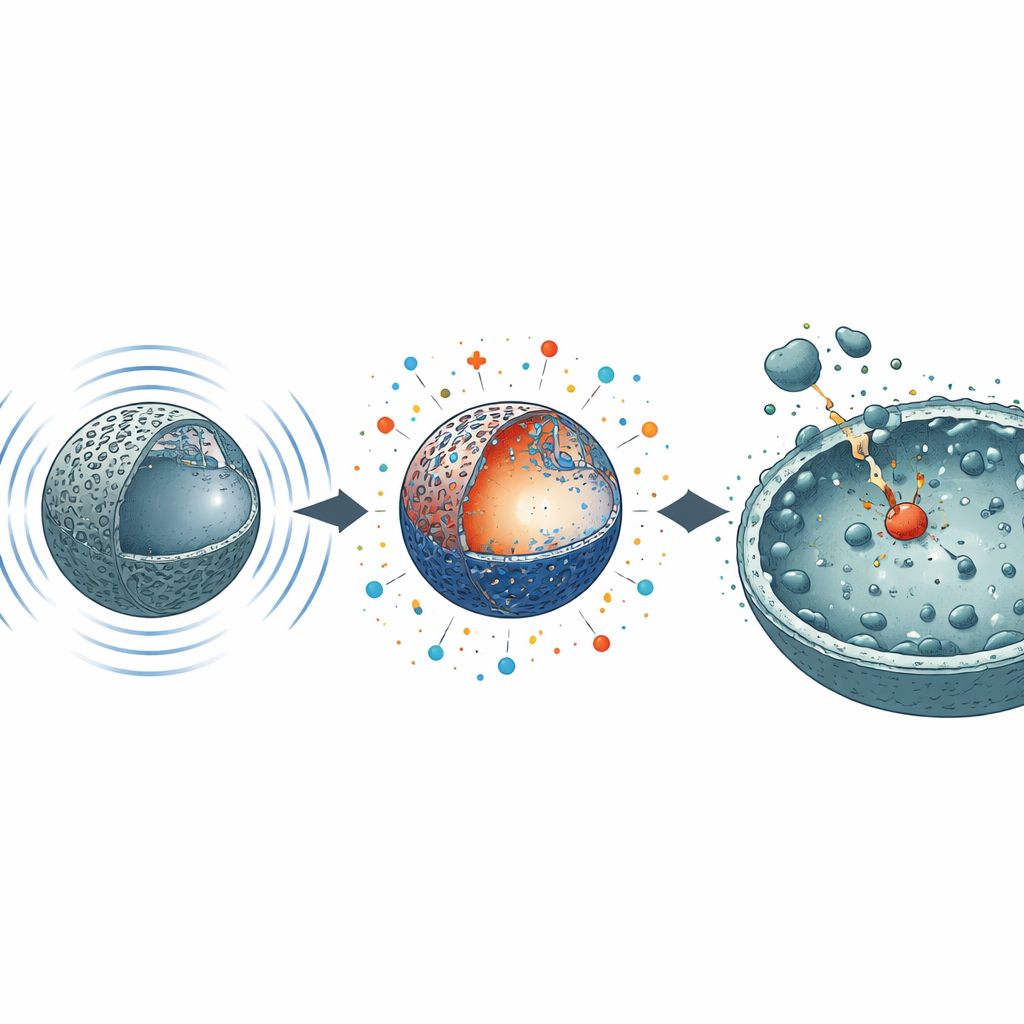
W przeciwieństwie do terapii opartych na świetle czy dodatkowych reagentach, ten system napędzany jest energią mechaniczną. Gdy kule N3 są wystawione na ultradźwięki w cieczy, fale ciśnienia ściskają i rozciągają ich sieć krystaliczną. To odkształcenie rozdziela ładunki dodatnie i ujemne wewnątrz materiału, które następnie reagują z rozpuszczonym tlenem, tworząc kilka rodzajów wysoce reaktywnych form tlenu (ROS). W testach rozkładu barwników, stosowanych jako substytut biologicznych celów, sonikowane N3 usunęły niemal 89% uporczywego niebieskiego barwnika w zaledwie cztery minuty przy 200 watach ultradźwięków — znacznie lepiej niż materiał nieaktywowany ultradźwiękami. Pomiary z sondami molekularnymi wykazały, że N3 zwiększa poziomy dwóch długotrwałych ROS, tlenu singletowego i ponadtlenku, ponad trzynastokrotnie w porównaniu z formą nieaktywną, przy jednoczesnym umiarkowanym wzroście rodników hydroksylowych. Po aktywacji N3 wykazuje silną aktywność katalityczną przez dni, co wskazuje na efekt „pamięci”, w którym jego reaktywny stan utrzymuje się długo po wyłączeniu ultradźwięków.
Rozkładanie bakterii opornych na leki i ich biofilmów
Aby ocenić wpływ w warunkach zbliżonych do rzeczywistych, zespół wystawił cząstki na działanie niebezpiecznych klinicznych szczepów wielolekoopornego Staphylococcus aureus oraz szeroko opornego Pseudomonas aeruginosa. Spośród wszystkich formulacji sonikowane N3 konsekwentnie okazały się najsilniejsze, hamując wzrost bakterii przy bardzo niskich stężeniach — nawet 5–10 mikrogramów na mililitr — i całkowicie oczyszczając hodowle w ciągu 24–48 godzin. Testy metodą dysków pokazały, że N3 wytwarza większe strefy zahamowania niż powszechnie stosowany antybiotyk, zwłaszcza przeciw szczepom opornym. Obrazy mikroskopowe traktowanych bakterii ujawniły poszarpane ściany komórkowe, zapadłe kształty i wycieki wnętrzności, a barwnik fluorescencyjny wykrywający uszkodzenia błony wykazał wyraźne skoki sygnału. N3 atakował także śluzowate społeczności ochronne zwane biofilmami: w stężeniach rzędu kilkudziesięciu mikrogramów na mililitr zapobiegał tworzeniu nowych biofilmów i usuwał ponad 99% dojrzałych, przewyższając nieaktywowane cząstki we wszystkich testach.
Celowanie w raka jelita grubego przy jednoczesnym oszczędzaniu komórek normalnych
Ponieważ ta sama chemia ROS może uszkadzać komórki nowotworowe, badacze następnie wystawili ludzkie komórki raka jelita grubego (HCT‑116) na działanie sonikowanego N3. Po 24 godzinach połowa komórek nowotworowych została unieszkodliwiona przy około 100 mikrogramach na mililitr, a większość była martwa przy 200 mikrogramach na mililitr, z całkowitą utratą żywotności przy najwyższej testowanej dawce. Obserwacja przez cztery dni wykazała, że pojedyncza ekspozycja nadal zabija komórki, obniżając przeżywalność do około 13% po 96 godzinach bez kolejnych ultradźwięków. Pomiary cytometrii przepływowej potwierdziły powszechną utratę integralności błony przy tych dawkach. Normalne ludzkie fibroblasty skóry, w przeciwieństwie do tego, znosiły to samo leczenie znacznie lepiej: przy dawce hamującej w połowie komórki nowotworowe prawie 90% fibroblastów pozostało żywych, co wskazuje na użyteczne, choć nie absolutne okno bezpieczeństwa.
Co to może oznaczać dla przyszłych terapii
Podsumowując, wyniki sugerują, że starannie zaprojektowane kule Ni₂CoS₄, takie jak N3, mogą działać jak miniaturowe, możliwe do „doładowania” reaktory w organizmie: krótki impuls ultradźwięków przełącza je w długo żyjący stan, który stale generuje ROS, które z kolei perforują błony bakterii, destabilizują biofilmy i wpędzają komórki nowotworowe w śmiertelny stres oksydacyjny. Ponieważ ten atak opiera się na szeroko zakrojonych uszkodzeniach fizycznych i chemicznych, a nie na pojedynczym celu biochemicznym, mikroorganizmom może być znacznie trudniej wyewoluować oporność. Prace te pozostają na etapie laboratoryjnym, a pytania o długoterminowe bezpieczeństwo, dostarczanie i zachowanie w organizmach żywych wciąż wymagają odpowiedzi. Jednak wskazują na nową klasę terapii „aktywowanych mechanicznie”, które pewnego dnia mogą uzupełniać lub ratować zawodzące antybiotyki i wzmocnić leczenie raka.
Cytowanie: Qurbani, K., Amiri, O. & Hamzah, H. Multifunctional hierarchical Ni2CoS4 structures for combating drug-resistant infections and colorectal cancer via piezocatalytic ROS generation. Sci Rep 16, 10294 (2026). https://doi.org/10.1038/s41598-026-41092-3
Słowa kluczowe: piezokataliza, oporność na antybiotyki, niszczenie biofilmów, terapia nanopartikelami, rak jelita grubego