Clear Sky Science · ja
耐薬性感染症と大腸癌に対抗するための多機能階層型Ni2CoS4構造:圧電触媒的ROS生成による治療法
なぜこの新しい感染症・がんへのアプローチが重要か
抗生物質耐性の感染症と大腸がんは現代医療における重大な脅威であり、既存の薬剤で治療することがますます難しくなっています。本研究はまったく異なるタイプの治療法を探ります:穏やかな超音波で刺激されると作動する微小なニッケル–コバルト硫化物粒子です。従来の薬剤のように働くのではなく、これらの粒子は機械的エネルギーを反応性分子のバーストに変換し、実用的な線量で健康な細胞を大部分損なうことなく、細菌、バイオフィルム、がん細胞を破壊します。
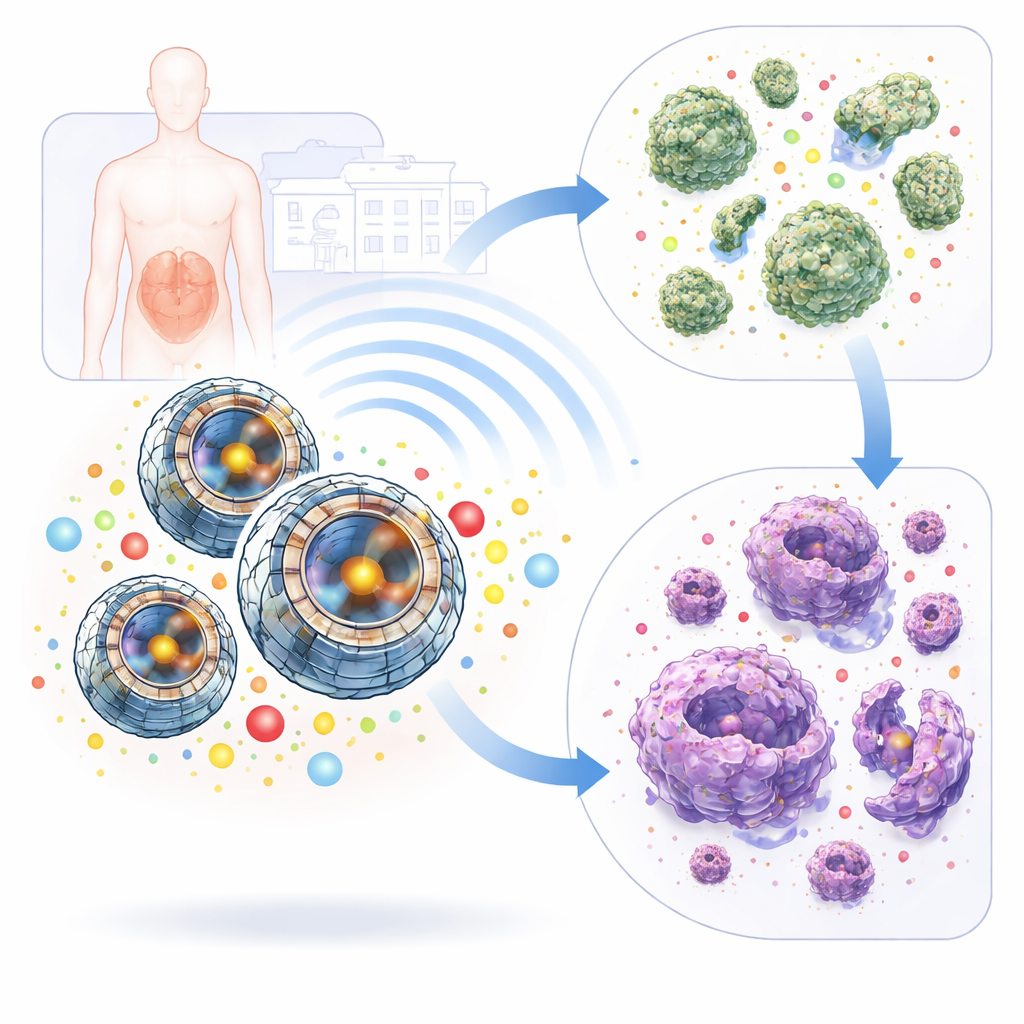
層状設計を持つ小さな設計球
研究者らは、液中での制御された加熱プロセスを用いて一連のニッケル–コバルト硫化物(Ni₂CoS₄)粒子を作製し、時間、温度、原料の比率を体系的に変えて構造を調整しました。顕微鏡観察により、最良の調製条件であるN3は、薄い相互に組み合わさったナノシートからなるほぼ均一な中空球を形成することが明らかになり、緩く織られたボールのような形状を示しました。X線およびラマン測定は、N3が高い結晶性と化学的秩序を持つことを示し、ガス吸着試験は比較的大きな内部表面積を持つことを確認しました。これらの特性により、N3は内部で電荷を効率的に移動させ、多くの活性サイトを外部に露出させることができ—これはその特異な作用機序にとって重要です。
音を化学攻撃に変える
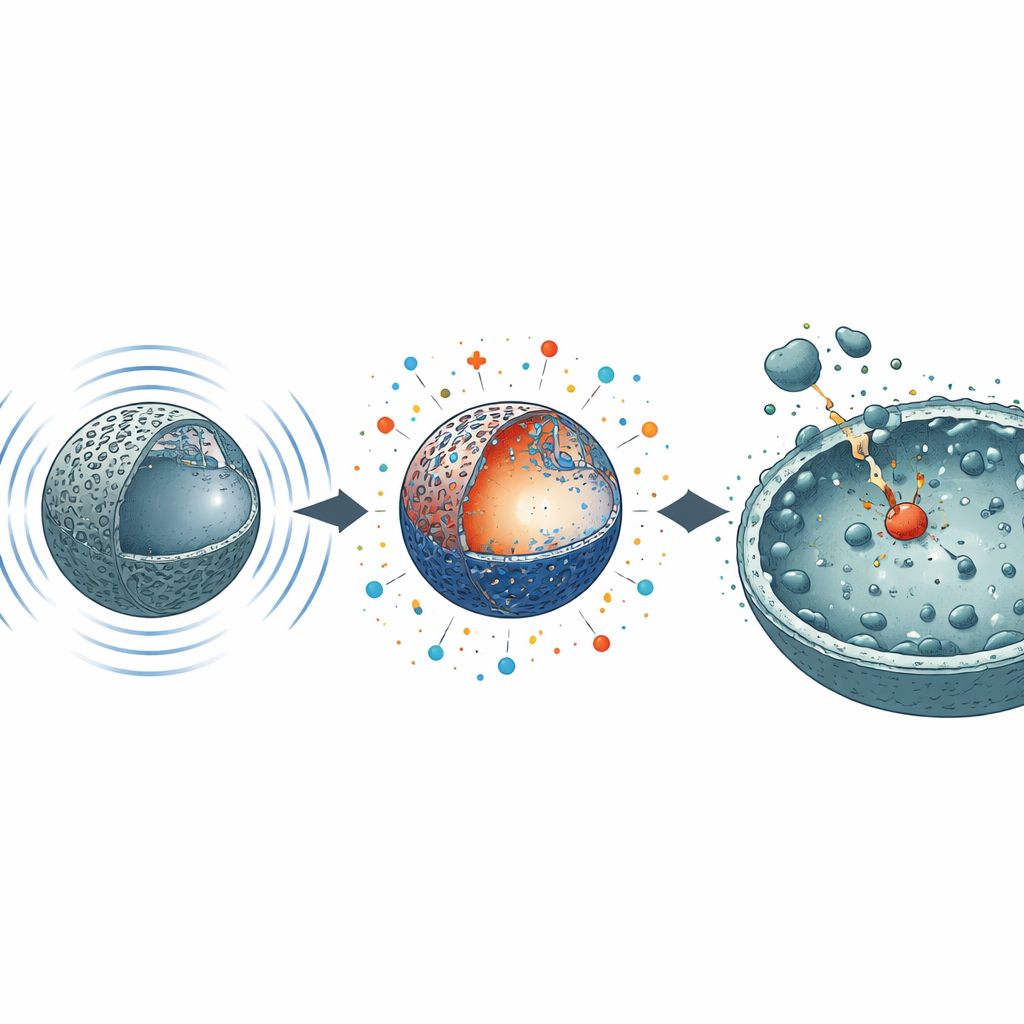
光や添加化学物質に依存する治療法とは異なり、このシステムは機械的エネルギーで駆動されます。N3球を液中で超音波にさらすと、圧力波が結晶格子を圧縮・伸張し、この歪みにより材料内部で正負の電荷が分離します。これらの電荷は溶存酸素と反応して、いくつかの種類の高反応性酸素種(ROS)を生成します。生物学的標的の代替指標として用いられる色素分解試験では、超音波処理されたN3は200ワットの超音波でわずか4分で頑強な青色染料の約89%を除去し、非処理材料を大きく凌ぎました。分子プローブによる測定は、N3が不活性形態と比べて一重項酸素とスーパーオキシドの2種の長寿命ROSを13倍以上に増強し、ヒドロキシラジカルも控えめに増加させることを示しました。一旦活性化されると、N3は数日間にわたり強い触媒活性を示し、超音波をオフにした後も反応性状態が持続する“記憶”効果を示します。
耐薬性細菌とそのバイオフィルムの分解
実世界での効果を検証するため、研究チームは多剤耐性黄色ブドウ球菌(Staphylococcus aureus)および広範囲耐性緑膿菌(Pseudomonas aeruginosa)の危険な臨床分離株に粒子を対峙させました。すべての処方の中で、超音波処理されたN3が一貫して最も強力であり、非常に低い濃度—5〜10マイクログラム毎ミリリットルまで—で細菌増殖を止め、24〜48時間以内に培養を完全に消失させました。ディスク拡散試験では、特に耐性株に対して、一般的に使用される抗生物質より大きな阻菌域をN3が生じました。処理された細菌の顕微鏡画像は細胞壁の断裂、萎縮した形状、内容物の漏出を示し、膜損傷を感知する蛍光色素は信号の急上昇を示しました。N3は粘性の保護コミュニティであるバイオフィルムにも作用し、数十マイクログラム毎ミリリットルの濃度で新規バイオフィルムの形成を防ぎ、成熟したバイオフィルムの99%以上を除去し、非活性化粒子を一貫して上回りました。
正常細胞を残しつつ大腸がんを標的化
同じROS化学が腫瘍細胞を損傷するため、研究者らはヒト大腸がん細胞(HCT‑116)を超音波処理したN3にさらしました。24時間後、がん細胞の半数は約100マイクログラム毎ミリリットルで機能不全になり、200マイクログラム毎ミリリットルではほとんどが死滅し、最高投与量では生存能が完全に失われました。その後の4日間の追跡では、単回曝露で細胞死が続き、追加の超音波を与えなくても96時間で生存率は約13%まで低下しました。フローサイトメトリーの測定は、これらの用量で膜の完全性が広範に失われていることを確認しました。対照として正常なヒト皮膚線維芽細胞は同じ処置をはるかに良く耐え、がん細胞の半抑制用量においてほぼ90%の線維芽細胞が生存しており、有用ではあるが絶対的ではない安全域を示しました。
将来の治療にとっての意味
総じて、N3のように注意深く設計されたNi₂CoS₄球は、体内でミニチュアの充電可能なリアクターとして働く可能性があることを示唆しています:短い超音波パルスがそれらを長寿命の活性状態に切り替え、持続的にROSを生成し、それが細菌膜に穴を開け、バイオフィルムを不安定化し、がん細胞を致命的な酸化ストレスに追い込みます。この攻撃は単一の生化学的標的ではなく広範な物理化学的損傷に依存するため、微生物が耐性を進化させるのはより困難かもしれません。本研究はまだ実験室段階にあり、長期的な安全性、送達方法、および生体内での挙動に関する課題は残ります。しかし、将来的に失敗した抗生物質を補完または救済し、がん治療を強化する可能性のある「機械的に活性化される」治療クラスへの道を指し示しています。
引用: Qurbani, K., Amiri, O. & Hamzah, H. Multifunctional hierarchical Ni2CoS4 structures for combating drug-resistant infections and colorectal cancer via piezocatalytic ROS generation. Sci Rep 16, 10294 (2026). https://doi.org/10.1038/s41598-026-41092-3
キーワード: 圧電触媒, 抗菌薬耐性, バイオフィルム破壊, ナノ粒子療法, 大腸がん