Clear Sky Science · fr
Structures hiérarchiques multifonctionnelles Ni2CoS4 pour lutter contre les infections résistantes aux médicaments et le cancer colorectal via la génération piézocatalytique d’ESP
Pourquoi cette nouvelle approche des infections difficiles et du cancer est importante
Les infections résistantes aux antibiotiques et le cancer colorectal comptent parmi les plus grandes menaces pour la santé moderne, et tous deux deviennent plus difficiles à traiter avec les médicaments existants. Cette étude explore une thérapie très différente : de minuscules particules de sulfure de nickel‑cobalt qui s’activent lorsqu’elles sont sollicitées par de l’échographie douce. Plutôt que d’agir comme un médicament classique, ces particules convertissent l’énergie mécanique en bouffées de molécules réactives capables de déchirer bactéries, biofilms et cellules cancéreuses — tout en épargnant dans une large mesure les cellules saines à des doses pratiques.
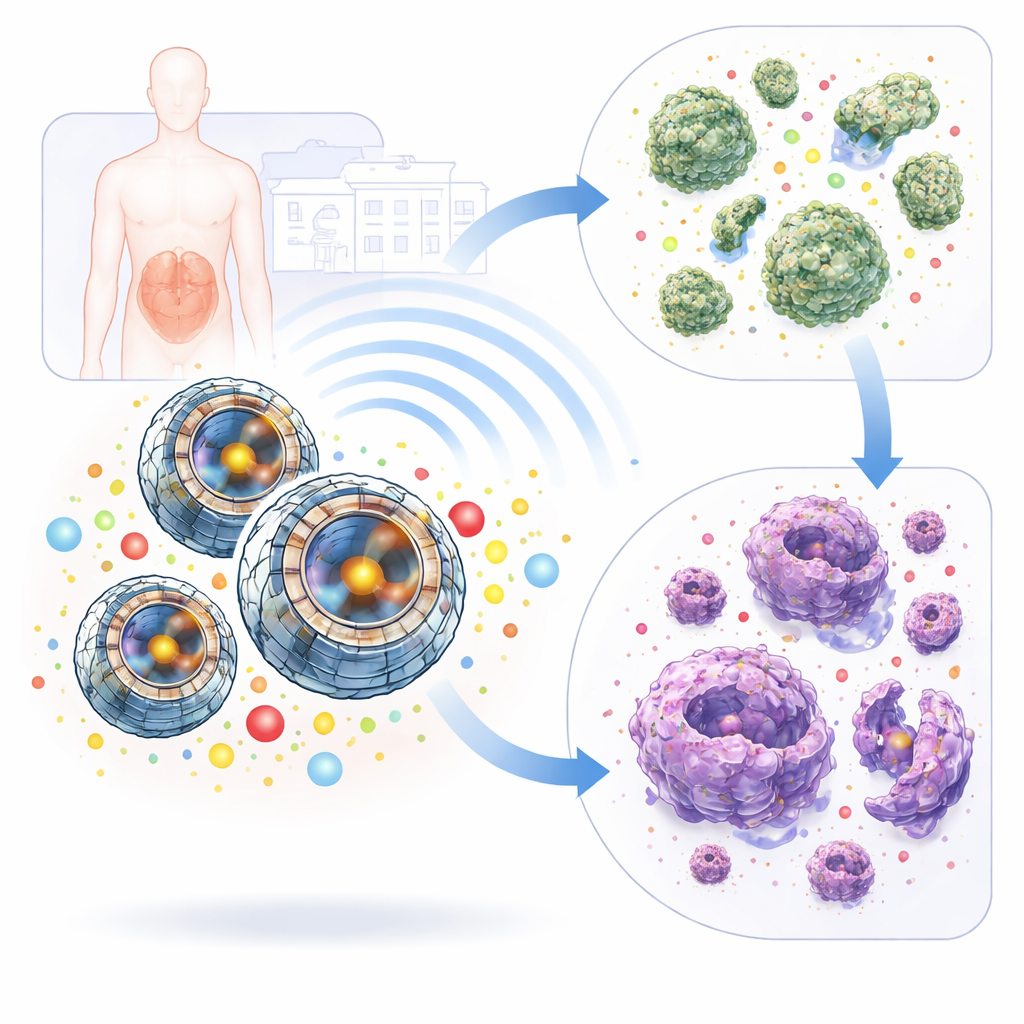
Petites sphères ingénierées à structure stratifiée
Les chercheurs ont synthétisé une famille de particules de sulfure de nickel‑cobalt (Ni₂CoS₄) par un procédé de chauffage contrôlé en phase liquide, puis ont fait varier systématiquement le temps, la température et les proportions des réactifs pour ajuster leur structure. La microscopie a révélé que la meilleure formulation, baptisée N3, forme des sphères creuses presque uniformes constituées de nanosheets minces et emboîtés, comme une balle tissée grossièrement. Les mesures par rayons X et Raman ont montré que N3 est également très cristallin et chimiquement bien ordonné, et des tests d’adsorption de gaz ont confirmé qu’elle présente une surface interne relativement grande. Ces caractéristiques permettent à N3 de déplacer efficacement des charges électriques en son sein et d’exposer de nombreux sites actifs à l’environnement — deux propriétés cruciales pour son mode d’action inhabituel.
Transformer le son en attaque chimique
Contrairement aux thérapies qui reposent sur la lumière ou des additifs chimiques, ce système est mû par l’énergie mécanique. Lorsque les sphères N3 sont exposées à l’échographie en milieu liquide, les ondes de pression compressent et étirent leur réseau cristallin. Cette déformation sépare charges positives et négatives à l’intérieur du matériau, lesquelles réagissent ensuite avec l’oxygène dissous pour former plusieurs types d’espèces réactives de l’oxygène (ESP). Dans des essais de dégradation de colorant utilisés comme substitut de cibles biologiques, le N3 soniqué a éliminé près de 89 % d’un colorant bleu tenace en seulement quatre minutes à 200 watts d’échographie — bien mieux que le matériau non soniqué. Des mesures avec des sondes moléculaires ont montré que N3 augmente plus de treize fois deux ESP longuement vivantes, l’oxygène singulet et le superoxyde, par rapport à sa forme inactive, tout en augmentant modérément les radicaux hydroxyles. Une fois activé, N3 conserve une forte activité catalytique pendant des jours, indiquant un effet de « mémoire » où son état réactif persiste bien après l’arrêt de l’échographie.
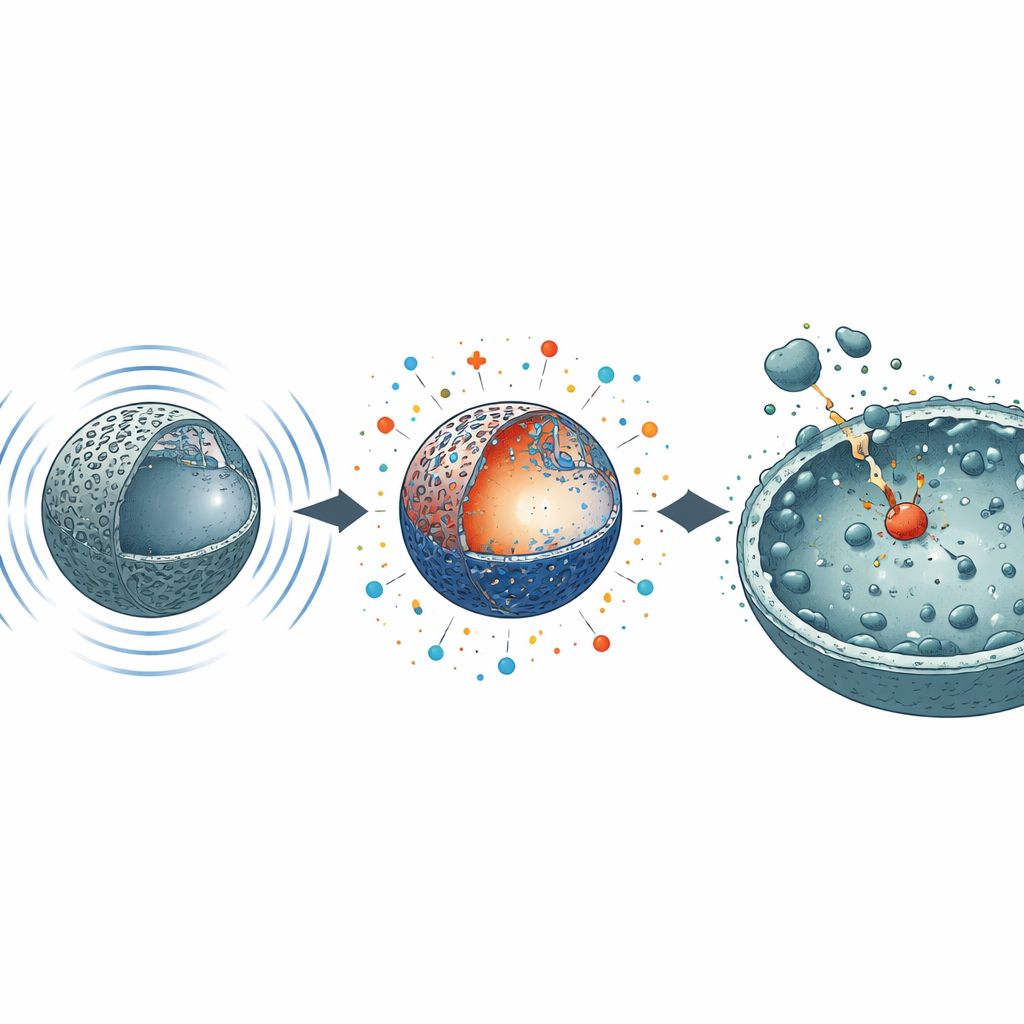
Démantèlement des bactéries résistantes aux médicaments et de leurs biofilms
Pour évaluer l’impact en conditions réelles, l’équipe a confronté les particules à des souches cliniques dangereuses de Staphylococcus aureus multirésistant aux antibiotiques et de Pseudomonas aeruginosa largement résistante. Parmi toutes les formulations, le N3 soniqué a été systématiquement le plus puissant, empêchant la croissance bactérienne à des concentrations très faibles — jusque 5–10 microgrammes par millilitre — et éliminant complètement les cultures en 24–48 heures. Des tests sur disque ont montré que N3 produisait des zones d’inhibition plus larges qu’un antibiotique couramment utilisé, en particulier contre les souches résistantes. Les images microscopiques des bactéries traitées ont révélé des parois cellulaires lacérées, des formes effondrées et des contenus cellulaires fuyants, tandis qu’un colorant fluorescent détectant les atteintes membranaires montrait des augmentations nettes du signal. N3 a aussi attaqué les communautés protectrices muqueuses appelées biofilms : à des dizaines de microgrammes par millilitre il a empêché la formation de nouveaux biofilms et éliminé plus de 99 % des biofilms matures, surpassant les particules non activées dans tous les cas.
Cibler le cancer colorectal tout en épargnant les cellules normales
Parce que la même chimie des ESP peut endommager les cellules tumorales, les chercheurs ont ensuite exposé des cellules humaines de cancer colorectal (HCT‑116) au N3 soniqué. Après 24 heures, la moitié des cellules cancéreuses étaient désactivées à environ 100 microgrammes par millilitre, et la plupart étaient mortes à 200 microgrammes par millilitre, avec une perte complète de viabilité à la dose la plus élevée testée. Un suivi sur quatre jours a montré qu’une seule exposition continuait à tuer les cellules, faisant chuter la survie à environ 13 % à 96 heures sans échographie supplémentaire. Des mesures par cytométrie en flux ont confirmé une perte étendue de l’intégrité membranaire à ces doses. Les fibroblastes cutanés humains normaux, en revanche, ont mieux toléré le même traitement : à la dose inhibitrice médiane pour les cellules cancéreuses, près de 90 % des fibroblastes restaient viables, indiquant une fenêtre de sécurité utile bien que non absolue.
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, les résultats suggèrent que des sphères Ni₂CoS₄ soigneusement conçues comme N3 peuvent agir comme de petits réacteurs rechargeables à l’intérieur du corps : une brève impulsion d’échographie les bascule dans un état de longue durée qui génère en continu des ESP, lesquelles perforent les membranes bactériennes, déstabilisent les biofilms et poussent les cellules cancéreuses vers un stress oxydatif létal. Parce que cette attaque repose sur des dommages physiques et chimiques larges plutôt que sur une cible biochimique unique, il pourrait être beaucoup plus difficile pour les microbes d’évoluer vers la résistance. Les travaux en sont encore au stade laboratoire, et des questions concernant la sécurité à long terme, la délivrance et le comportement in vivo restent à trancher. Mais cela ouvre la voie à une nouvelle classe de thérapies « activées mécaniquement » qui pourraient un jour compléter ou sauver des antibiotiques défaillants et renforcer les traitements du cancer.
Citation: Qurbani, K., Amiri, O. & Hamzah, H. Multifunctional hierarchical Ni2CoS4 structures for combating drug-resistant infections and colorectal cancer via piezocatalytic ROS generation. Sci Rep 16, 10294 (2026). https://doi.org/10.1038/s41598-026-41092-3
Mots-clés: piézocatalyse, résistance antimicrobienne, rupture de biofilm, thérapie par nanoparticules, cancer colorectal