Clear Sky Science · pl
Unikalne cechy fenotypowe i receptora T komórek CD8+ zgromadzonych w mózgach myszy z chorobą Alzheimera
Dlaczego komórki odpornościowe w mózgu mają znaczenie dla Alzheimera
Choroba Alzheimera bywa zwykle opisywana przez pryzmat lepko-sklejających się złogów białkowych i obumierających neuronów, jednak układ odpornościowy mózgu zyskuje coraz większe znaczenie. W tym badaniu skupiono się na jednej grupie komórek odpornościowych — komórkach CD8, które osiedlają się w mózgu na dłużej. Ponowna analiza szczegółowych danych pojedynczych komórek pochodzących od modeli myszy choroby Alzheimera i od myszy starzejących się normalnie pozwoliła badaczom odkryć dwa główne typy tych rezydujących w mózgu limfocytów T, które mogą wpływać na chorobę w przeciwnych kierunkach — jeden potencjalnie ochronny, drugi możliwie podtrzymujący trwające uszkodzenia.
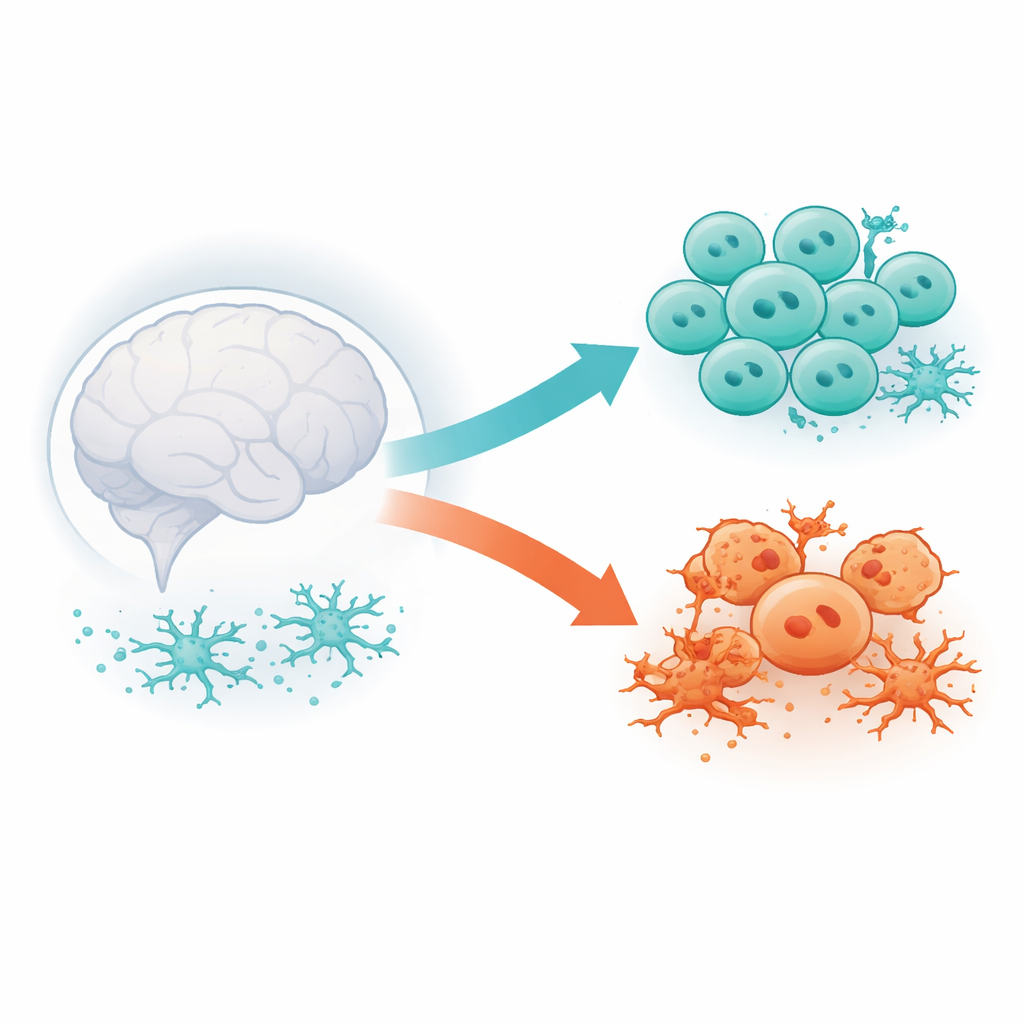
Dwie twarze rezydujących w mózgu komórek T
Zespół skoncentrował się na komórkach CD8, które zamieszkują tkankę mózgową, zamiast jedynie przepływać z krwią. Wykorzystując publicznie dostępne dane sekwencjonowania RNA pojedynczych komórek z myszy podatnych na Alzheimera, z ich genetycznie zmodyfikowanych krewnych oraz z normalnie starzejących się myszy, pogrupowali tysiące tych komórek na klastry w oparciu o włączone geny. Wyłoniły się dwa duże klastry. Jeden zależał silnie od cząsteczki zwanej CXCR6 do wnikania lub pozostawania w mózgu i wykazywał cechy stanu „hamulca” immunologicznego. Drugi klaster pojawiał się tylko przy obecnej patologii podobnej do Alzheimera i miał bardziej „czuły”, przypominający komórki macierzyste profil, co sugeruje, że te komórki mogą przetrwać i generować nowe fale aktywnych komórek T w czasie.
Komórki związane ze starzeniem, które mogą chronić mózg
Klaster związany z CXCR6 dominował w normalnie starzejących się mózgach i występował także u myszy z Alzheimera, lecz praktycznie znikał po wyeliminowaniu CXCR6. Te komórki nosiły zestaw markerów związanych z długotrwałą rezydencją w tkankach oraz z tłumieniem odpowiedzi immunologicznych, nie wykazując jednocześnie oznak całkowitego wyczerpania czy zużycia. Wcześniejsze eksperymenty innych zespołów sugerowały, że komórki CD8 kierowane przez CXCR6 mogą pomagać w redukcji złogów amyloid-beta, białkowych grudek definiujących Alzheimera. Składając te elementy razem, autorzy twierdzą, że niektóre komórki T indukowane wiekiem nie są wyłącznie szkodliwe; zamiast tego mogą pomagać utrzymywać mikroglej — rezydujące w mózgu komórki odpornościowe — w ryzach i pośrednio ograniczać odkładanie amyloidu, działając jako wrodzona warstwa ochronna w starzejącym się mózgu.
Komórki związane z chorobą o trwałym wpływie
Klaster powiązany z Alzheimera opowiadał inną historię. Te komórki T wykazywały wysokie poziomy genów związanych z przeżywalnością i „macierzystością”, a także genów natychmiastowej odpowiedzi, które włączają się, gdy komórki są niedawno aktywowane. Produkowały też sygnały zapalne, takie jak interferon-gamma. Śledząc unikalne kody receptorów T (TCR) noszone przez każdy klon, badacze odkryli, że komórki związane z chorobą dzieliły wiele klonów z innymi aktywowanymi klastrami, sugerując ciągłość od komórek przypominających komórki macierzyste do bardziej agresywnych efektorów. W kontraście nie dzieliły one żadnych TCR z klastrem związanym z CXCR6, co sugeruje, że są napędzane przez inne bodźce. Analiza komunikacji między komórkami T a mikroglejem wskazała na specyficzną ścieżkę obejmującą galektynę-9 i enzym nazwany P4HB, który może zmieniać stan redoks powierzchni komórkowej T i tłumić sygnalizację receptorową — warunki sprzyjające utrzymaniu długowiecznych, przypominających komórki macierzyste limfocytów T.
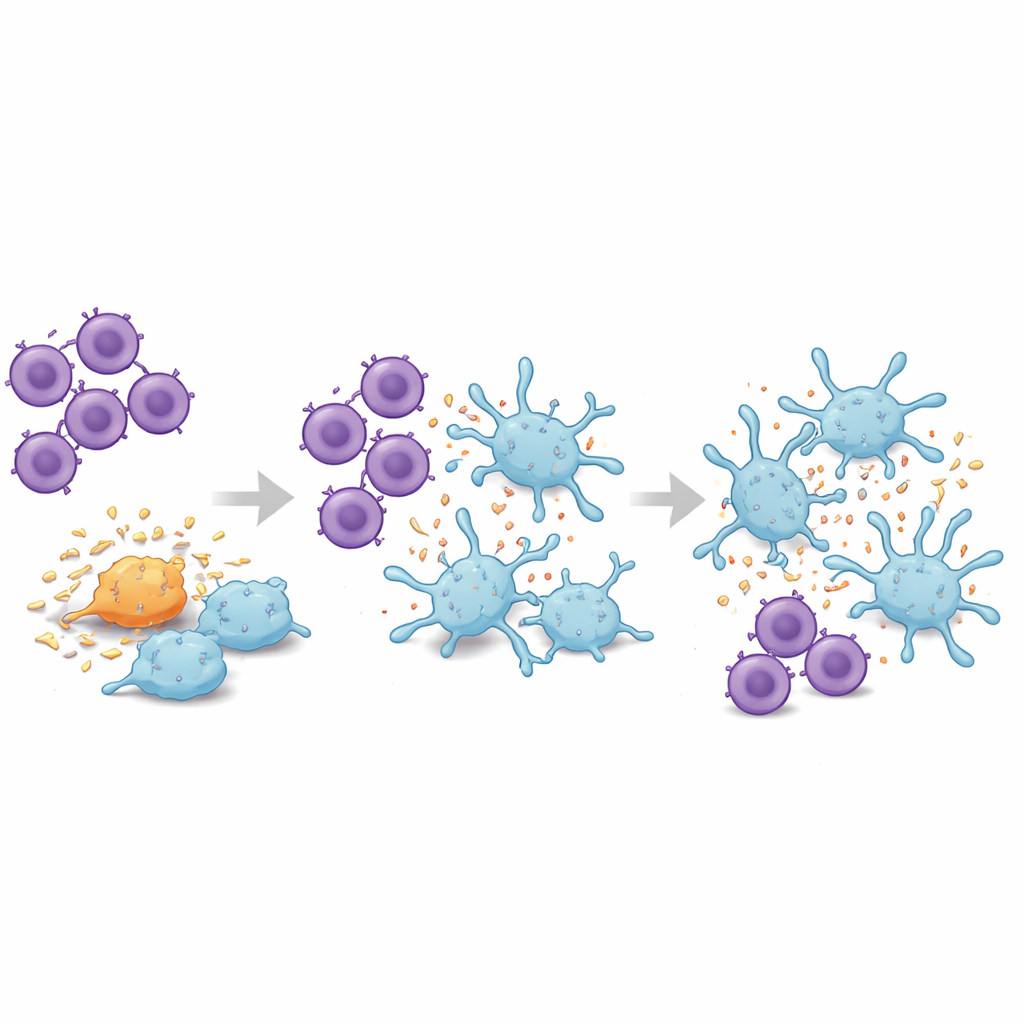
Czy te komórki T rozpoznają białka charakterystyczne dla Alzheimera?
Aby zbadać, co może napędzać komórki związane z chorobą, zespół przeanalizował właściwości biofizyczne i strukturalne ich najsilniej rozszerzonych TCR. Korzystając z narzędzi obliczeniowych, pogrupowali TCR według właściwości chemicznych ich kluczowych regionów kontaktowych i odkryli, że dwie wiodące receptory w klastrze związanym z Alzheimera miały nietypowo odrębne profile, inne niż większość pozostałych w zbiorze danych. Następnie modelowali, jak te receptory mogłyby fizycznie dokować na mysię cząsteczki prezentujące krótkie fragmenty amyloid-beta, zasadniczego białka Alzheimera. Dla jednego silnie ekspandowanego receptora kilka fragmentów amyloid-beta dało stabilne, wiarygodne modele wiązania z wieloma bliskimi kontaktami między receptorem a peptydem, co sugeruje, że przynajmniej niektóre z tych komórek T mogą specyficznie rozpoznawać amyloid-beta w chorym mózgu.
Co to oznacza dla Alzheimera i starzenia
Dla laika kluczowy wniosek jest taki, że nie wszystkie najeżdżające mózg komórki T są takie same. Badanie pokazuje, że samo starzenie może generować dużą pulę rezydujących komórek CD8, które wydają się nastawione na powściąganie zapalenia i mogą pomagać ograniczać zmiany podobne do Alzheimera, podczas gdy patologia Alzheimera wywołuje odrębną, długowieczną populację komórek T, które mogą rozpoznawać białka choroby i podtrzymywać trwającą aktywność immunologiczną. Zrozumienie, jak wzmocnić ochronne komórki związane z CXCR6 i złagodzić lub przekierować związane z Alzheimera komórki przypominające komórki macierzyste, może otworzyć nowe drogi terapeutyczne współpracujące, zamiast działać przeciwko, własnemu układowi odpornościowemu mózgu.
Cytowanie: Zhihuan, W., Furusawa-Nishii, E. & Miyake, S. Unique phenotypic and T cell receptor characteristics of CD8+ T cells accumulated in the brains of Alzheimer’s disease mice. Sci Rep 16, 12518 (2026). https://doi.org/10.1038/s41598-026-38351-8
Słowa kluczowe: choroba Alzheimera, komórki odpornościowe mózgu, komórki T CD8, mikroglej, amyloid-beta