Clear Sky Science · de
Einzigartige phänotypische und T‑Zellrezeptor‑Eigenschaften von CD8+-T‑Zellen, die sich in den Gehirnen von Alzheimer‑Mäusen ansammeln
Warum Immunzellen im Gehirn für Alzheimer wichtig sind
Die Alzheimer‑Krankheit wird meist als Problem mit klebrigen Proteinablagerungen und sterbenden Nervenzellen beschrieben, doch das Immunsystem des Gehirns rückt zunehmend in den Mittelpunkt. Diese Studie betrachtet eine spezielle Gruppe von Immunzellen, die sogenannten CD8‑T‑Zellen, die langfristig im Gehirn verweilen. Durch die erneute Auswertung detaillierter Einzelzell‑Daten aus Mausmodellen für Alzheimer und normaler Alterung entdeckten die Forschenden zwei Haupttypen dieser im Gehirn ansässigen T‑Zellen, die die Krankheit möglicherweise in entgegengesetzte Richtungen beeinflussen — der eine potenziell schützend, der andere möglicherweise anhaltende Schäden fördernd.
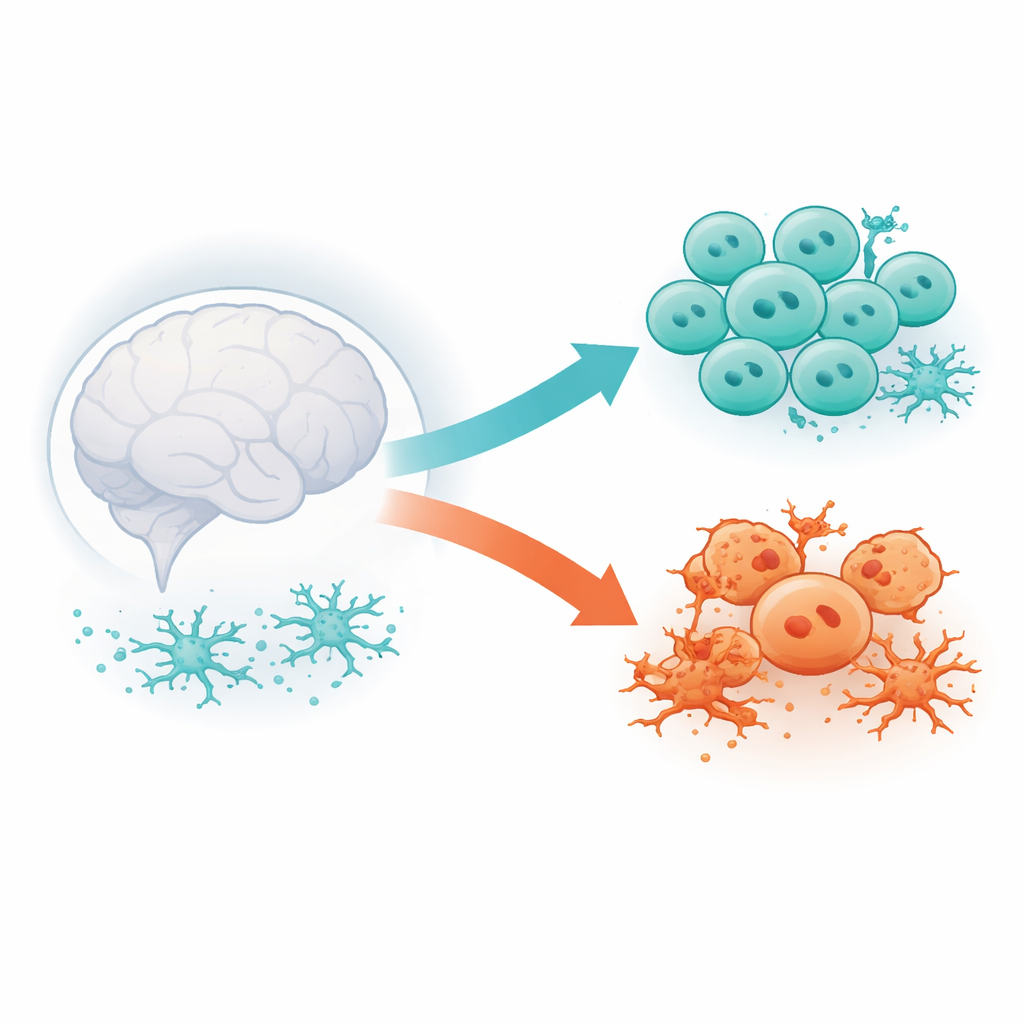
Zwei Gesichter der im Gehirn siedelnden T‑Zellen
Das Team konzentrierte sich auf CD8‑T‑Zellen, die im Gehirngewebe leben und nicht nur im Blut zirkulieren. Mit öffentlich verfügbaren Einzelzell‑RNA‑Sequenzierungsdaten von Alzheimer‑anfälligen Mäusen, ihren genetisch veränderten Verwandten und normal gealterten Mäusen gruppierten sie Tausende dieser Zellen in Cluster anhand der aktivierten Gene. Zwei große Cluster stachen hervor. Das eine war stark abhängig von einem Molekül namens CXCR6, um ins Gehirn einzudringen oder dort zu verbleiben, und zeigte Merkmale eines immunologischen "Brems"‑Zustands. Das andere Cluster trat nur bei Alzheimer‑ähnlicher Pathologie auf und zeigte ein wacheres, stammzellähnliches Profil, was darauf hindeutet, dass diese Zellen persistieren und im Laufe der Zeit neue Wellen aktiver T‑Zellen erzeugen können.
Altersassoziierte Zellen, die das Gehirn schützen könnten
Das CXCR6‑assoziierte Cluster dominierte in normal gealterten Gehirnen und trat auch in Alzheimer‑Mäusen auf, war jedoch nahezu vollständig verschwunden, wenn CXCR6 ausgeschaltet wurde. Diese Zellen trugen eine Kombination von Markern, die mit langfristigem Verweilen in Geweben und mit der Dämpfung von Immunreaktionen assoziiert sind, ohne Anzeichen vollständiger Erschöpfung oder Funktionsunfähigkeit zu zeigen. Frühere Experimente anderer Gruppen hatten nahegelegt, dass CXCR6‑gesteuerte CD8‑T‑Zellen helfen können, Amyloid‑Beta‑Ablagerungen zu reduzieren, die proteinischen Klumpen, die Alzheimer definieren. Zusammengenommen argumentieren die Autorinnen und Autoren, dass einige altersinduzierten T‑Zellen nicht ausschließlich schädlich sind; vielmehr könnten sie die Microglia — die residenten Immunzellen des Gehirns — in Schach halten und indirekt die Amyloid‑Anhäufung begrenzen, somit als eingebaute Schutzschicht im alternden Gehirn wirken.
Krankheitsassoziierte Zellen mit anhaltender Wirkung
Das Alzheimer‑assoziierte Cluster erzählte eine andere Geschichte. Diese T‑Zellen zeigten hohe Werte von Genen, die mit Überleben und "Stammhaftigkeit" verbunden sind, sowie von sofort‑frühreaktiven Genen, die bei kürzlich aktivierten Zellen hochfahren. Sie erzeugten zudem entzündliche Signale wie Interferon‑gamma. Durch die Verfolgung der einzigartigen T‑Zell‑Rezeptor‑(TCR‑)Codes, die jeder Klon trägt, fanden die Forschenden heraus, dass diese krankheitsassoziierten Zellen viele Klone mit anderen aktivierten Clustern teilten, was auf ein Kontinuum von stammzellähnlichen Zellen zu aggressiveren Effektorzellen hindeutet. Im Gegensatz dazu teilten sie keinerlei TCRs mit dem CXCR6‑assoziierten Cluster, was darauf schließen lässt, dass unterschiedliche Auslöser zugrunde liegen. Eine Kommunikationsanalyse zwischen T‑Zellen und Microglia wies auf einen spezifischen Weg hin, an dem Galectin‑9 und ein Enzym namens P4HB beteiligt sind; dieses kann den Redox‑Zustand der T‑Zelloberfläche verändern und Rezeptorsignale dämpfen — Bedingungen, die die Erhaltung langlebiger, stammzellähnlicher T‑Zellen begünstigen könnten.
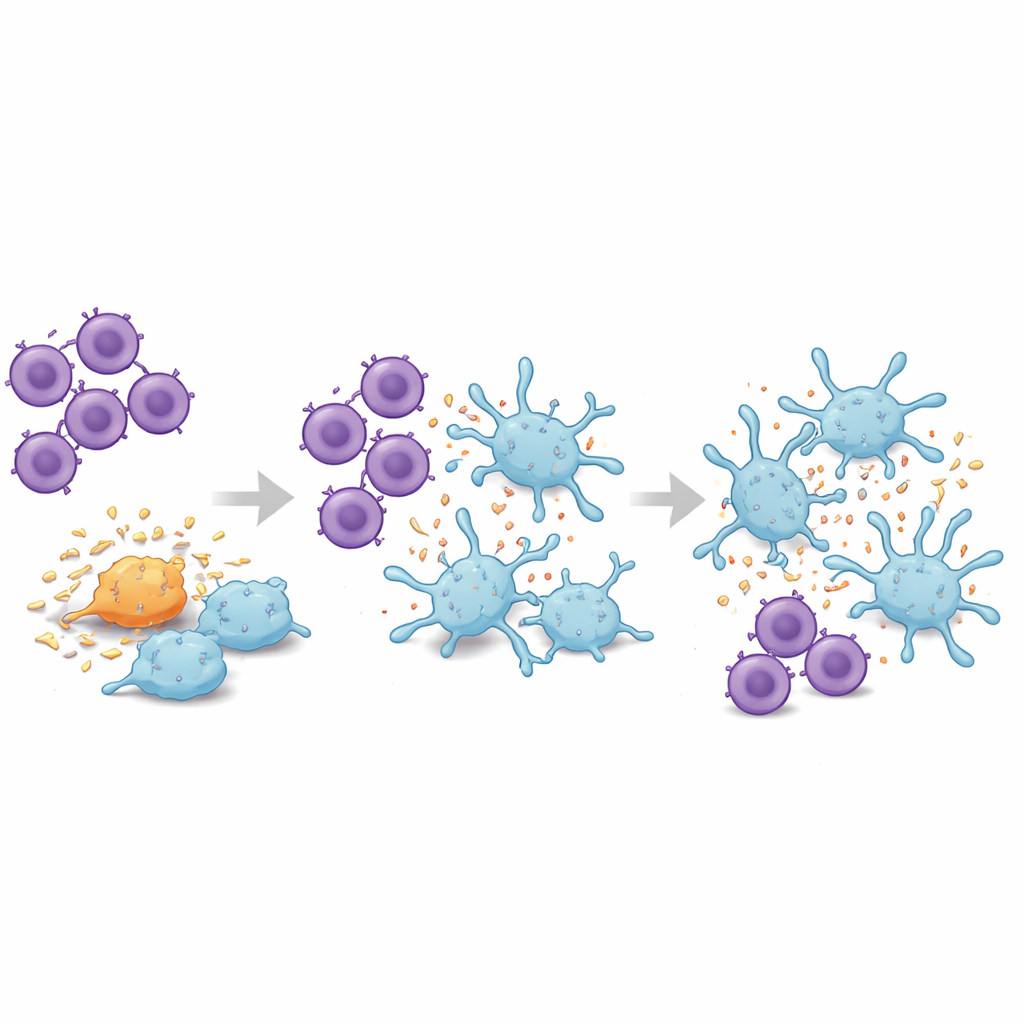
Erkennen diese T‑Zellen Alzheimer‑Proteine?
Um zu untersuchen, was die krankheitsassoziierten Zellen antreiben könnte, analysierte das Team die biophysikalischen und strukturellen Eigenschaften ihrer am stärksten expandierten TCRs. Mithilfe rechnerischer Werkzeuge gruppierten sie TCRs nach den chemischen Eigenschaften ihrer Schlüsselkontaktregionen und stellte fest, dass die beiden dominanten Rezeptoren im Alzheimer‑assoziierten Cluster ungewöhnlich distinkte Profile hatten, anders als die meisten anderen in den Daten. Anschließend modellierten sie, wie diese Rezeptoren physisch an Maus‑Immunmoleküle andocken könnten, die kurze Fragmente von Amyloid‑Beta präsentieren, dem zentralen Alzheimer‑Protein. Für einen stark expandierten Rezeptor lieferten mehrere Amyloid‑Beta‑Fragmente stabile, plausible Bindungsmodelle mit vielen engen Kontakten zwischen Rezeptor und Peptid, was darauf hindeutet, dass mindestens einige dieser T‑Zellen Amyloid‑Beta im erkrankten Gehirn spezifisch erkennen könnten.
Was das für Alzheimer und Alterung bedeutet
Für Nicht‑Spezialisten ist die wichtigste Botschaft, dass nicht alle ins Gehirn eindringenden T‑Zellen gleich sind. Diese Studie zeigt, dass allein durch Alterung ein großer Pool residenter CD8‑T‑Zellen entstehen kann, die offenbar darauf ausgerichtet sind, Entzündungen zu dämpfen und möglicherweise Alzheimer‑ähnliche Veränderungen einzuschränken, während Alzheimer‑Pathologie eine separate, langlebige T‑Zell‑Population auslöst, die Krankheitsproteine erkennen und die anhaltende Immunaktivität aufrechterhalten könnte. Zu verstehen, wie man die schützenden CXCR6‑assoziierten Zellen stärkt und die Alzheimer‑assoziierten stammzellähnlichen Zellen dämpft oder umlenkt, könnte neue Wege für Therapien eröffnen, die mit dem Immunsystem des Gehirns zusammenarbeiten statt dagegen.
Zitation: Zhihuan, W., Furusawa-Nishii, E. & Miyake, S. Unique phenotypic and T cell receptor characteristics of CD8+ T cells accumulated in the brains of Alzheimer’s disease mice. Sci Rep 16, 12518 (2026). https://doi.org/10.1038/s41598-026-38351-8
Schlüsselwörter: Alzheimer‑Krankheit, immunzellen des gehirns, CD8‑T‑Zellen, Microglia, Amyloid‑beta