Clear Sky Science · it
Caratteristiche fenotipiche e del recettore delle cellule T uniche dei CD8+ accumulate nei cervelli di topi con morbo di Alzheimer
Perché le cellule immunitarie nel cervello contano per l’Alzheimer
Il morbo di Alzheimer viene di solito descritto in termini di aggregati proteici appiccicosi e neuroni in degenerazione, ma il sistema immunitario cerebrale sta assumendo un ruolo sempre più centrale. Questo studio esamina un particolare gruppo di cellule immunitarie, chiamate linfociti T CD8, che si insediano a lungo termine nel cervello. Riesaminando dati dettagliati a singola cellula provenienti da modelli murini di Alzheimer e dall’invecchiamento normale, i ricercatori hanno identificato due principali tipi di queste T residenti nel cervello che potrebbero orientare la malattia in direzioni opposte: uno potenzialmente protettivo e l’altro forse promotore di danno persistente.
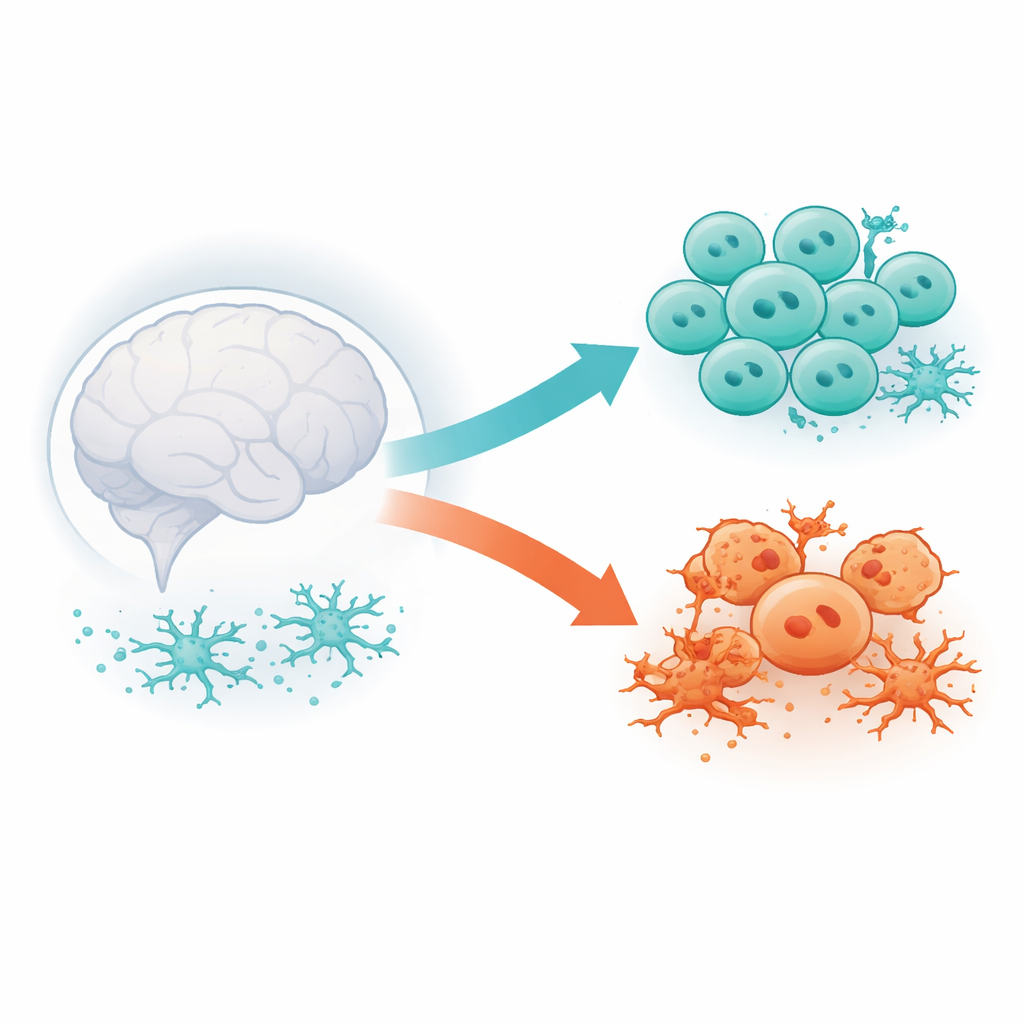
Le due facce dei linfociti T residenti nel cervello
Il gruppo si è concentrato sui linfociti T CD8 che risiedono nel tessuto cerebrale anziché transitare nel sangue. Utilizzando dati pubblici di sequenziamento dell’RNA a singola cellula da topi predisposti all’Alzheimer, i loro omologhi geneticamente modificati e topi invecchiati normalmente, hanno raggruppato migliaia di cellule in cluster in base ai geni espressi. Sono emersi due ampi cluster. Uno dipendeva fortemente da una molecola chiamata CXCR6 per entrare o restare nel cervello e mostrava i segni distintivi di uno stato di “freno” immunitario. L’altro cluster compariva solo in presenza di una patologia simile all’Alzheimer e presentava un profilo più vigilante e simile a cellule staminali, suggerendo che queste cellule possono persistere e generare nuove ondate di T attive nel tempo.
Cellule associate all’invecchiamento che potrebbero proteggere il cervello
Il cluster correlato a CXCR6 dominava nei cervelli invecchiati normalmente ed era presente anche nei topi con Alzheimer, ma risultava quasi assente quando CXCR6 veniva eliminato. Queste cellule esprimevano una combinazione di marcatori associati alla residenza a lungo termine nei tessuti e all’attenuazione delle risposte immunitarie, senza mostrare segni di esaurimento completo. Esperimenti precedenti di altri gruppi avevano suggerito che linfociti T CD8 guidati da CXCR6 possono contribuire a ridurre i depositi di amiloide-beta, gli aggregati proteici che caratterizzano l’Alzheimer. Nel complesso, gli autori sostengono che alcuni linfociti indotti dall’età non sono puramente dannosi; al contrario, potrebbero aiutare a mantenere sotto controllo le microglia — le cellule immunitarie residenti del cervello — e limitare indirettamente l’accumulo di amiloide, agendo come uno strato protettivo intrinseco nel cervello invecchiato.
Cellule associate alla malattia con impatto duraturo
Il cluster associato alla malattia racconta una storia diversa. Queste T esprimevano elevati livelli di geni legati alla sopravvivenza e alla “stamminalità”, insieme a geni di risposta precoce che si attivano quando le cellule sono di recente stimolate. Producevano anche segnali infiammatori come l’interferone-gamma. Tracciando i codici unici del recettore delle cellule T (TCR) che ogni clone porta, i ricercatori hanno scoperto che queste cellule legate alla malattia condividevano molti cloni con altri cluster attivati, suggerendo un continuum dalle cellule simili a staminali verso effettori più aggressivi. Al contrario, non condividevano alcun TCR con il cluster correlato a CXCR6, implicando che siano indotte da stimoli differenti. L’analisi delle comunicazioni tra T e microglia ha indicato una via specifica che coinvolge la galectina-9 e un enzima chiamato P4HB, che può alterare lo stato redox della superficie delle T e attenuare la segnalazione recettoriale — condizioni che possono favorire il mantenimento di T a lunga vita e con caratteristiche di staminalità.
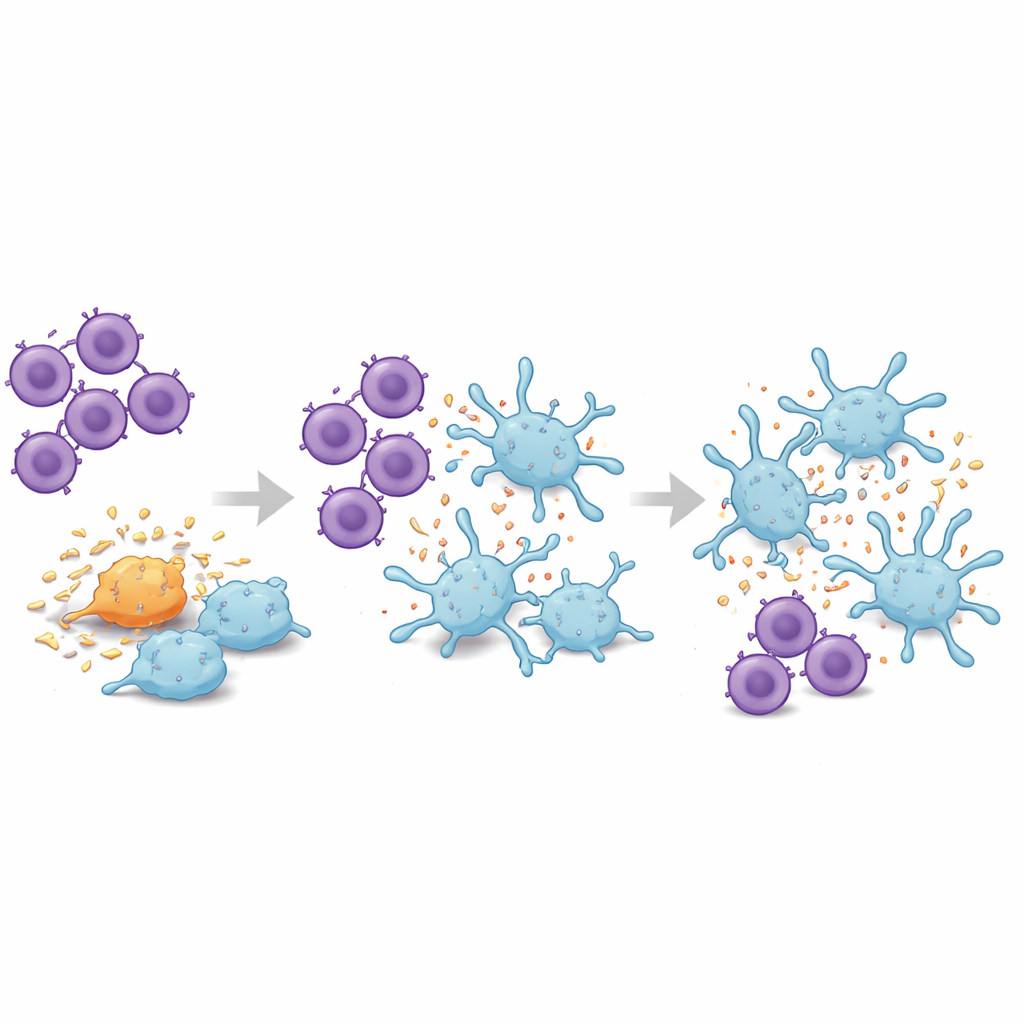
Queste T riconoscono le proteine dell’Alzheimer?
Per indagare cosa possa guidare le cellule associate alla malattia, il team ha esaminato le caratteristiche biofisiche e strutturali dei TCR più espansi. Utilizzando strumenti computazionali, hanno raggruppato i TCR in base alle proprietà chimiche delle loro regioni chiave di contatto e hanno trovato che i due recettori principali nel cluster associato all’Alzheimer presentavano profili insoliti e distinti, diversi dalla maggior parte degli altri nel dataset. Hanno quindi modellato come questi recettori potrebbero legarsi fisicamente a molecole immunitarie murine che presentano brevi frammenti di amiloide-beta, la proteina centrale dell’Alzheimer. Per un recettore altamente espanso, diversi frammenti di amiloide-beta hanno prodotto modelli di legame stabili e plausibili con numerosi contatti ravvicinati tra recettore e peptide, suggerendo che almeno alcune di queste T potrebbero riconoscere specificamente l’amiloide-beta nel cervello malato.
Cosa significa per l’Alzheimer e l’invecchiamento
Per un non specialista, il messaggio chiave è che non tutte le T che invadono il cervello sono uguali. Questo studio mostra che il solo invecchiamento può generare un ampio pool di T CD8 residenti che sembrano orientate a contenere l’infiammazione e potrebbero contribuire a limitare i cambiamenti simili all’Alzheimer, mentre la patologia alzheimeriana innesca una popolazione distinta e duratura di T che potrebbe riconoscere proteine della malattia e alimentare l’attività immunitaria continua. Capire come potenziare le cellule protettive correlate a CXCR6 e moderare o reindirizzare le cellule staminali associate all’Alzheimer potrebbe aprire nuove strade terapeutiche che lavorino con, piuttosto che contro, il sistema immunitario cerebrale.
Citazione: Zhihuan, W., Furusawa-Nishii, E. & Miyake, S. Unique phenotypic and T cell receptor characteristics of CD8+ T cells accumulated in the brains of Alzheimer’s disease mice. Sci Rep 16, 12518 (2026). https://doi.org/10.1038/s41598-026-38351-8
Parole chiave: Morbo di Alzheimer, cellule immunitarie cerebrali, linfociti T CD8, microglia, amiloide-beta