Clear Sky Science · pl
Sygnalizacja Hh i EGFR-Ras promuje różne etapy progresji guza w nabłonku pęcherzyka jajnika Drosophila
Jak komórki utrzymują równowagę tkanek
Nasze ciało, podobnie jak u muszek owocowych, nieustannie odnawia tkanki. Aby zachować zdrowie, komórki macierzyste muszą dzielić się i dojrzewać w odpowiednie typy komórek we właściwym czasie, unikając jednocześnie niekontrolowanego wzrostu prowadzącego do raka. W tym badaniu wykorzystano jajnik Drosophila jako wydajny model do odkrycia, jak dwa główne systemy komunikacji między komórkami współpracują, by utrzymać prawidłowy wzrost — i jak ich zaburzenie może prowadzić do nadmiernego, przypominającego guza rozrostu.
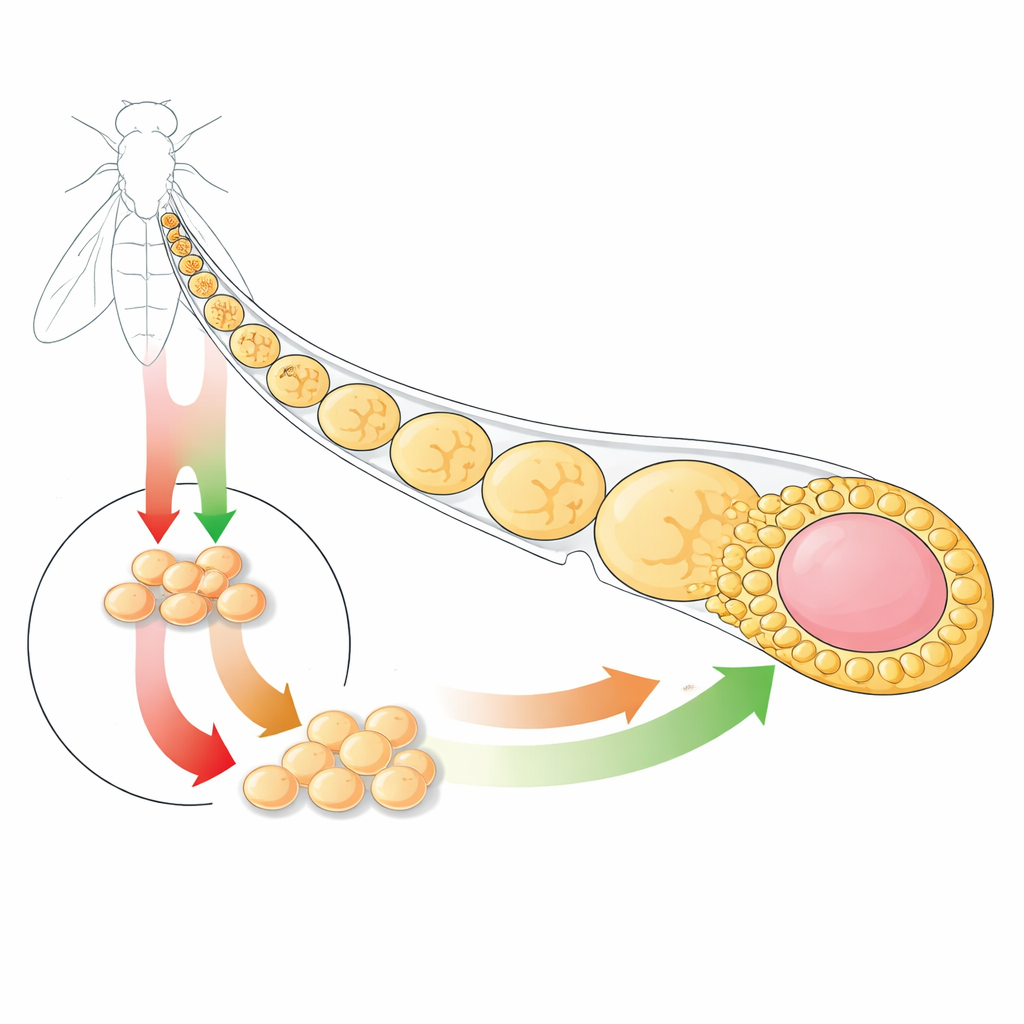
Mały narząd, wielkie wnioski
Naukowcy skupili się na nabłonku pęcherzyka w jajniku muszki owocowej, prostym arkuszu komórek otaczającym rozwijające się komory jajowe. Tę tkankę utrzymują komórki macierzyste pęcherzyka, które siedzą w określonej niszy i dają potomstwo specjalizujące się w kilku rolach, takich jak komórki główne pokrywające jajo, komórki szypułkowe łączące komory jajowe oraz komórki polarne pomagające organizować strukturę. Ponieważ wszystkie te wydarzenia zachodzą w bardzo małym obszarze i powtarzają się wielokrotnie, system jest idealny do badania, jak sygnały kontrolują zarówno proliferację, jak i różnicowanie w żywym nabłonku.
Dwie kluczowe wiadomości: wzrost i zmiana
Zespół analizuje dwa główne szlaki sygnalizacyjne: Hedgehog (Hh) i EGFR-Ras. Oba są znane w kontekście nowotworów u ludzi i są aktywne w obszarze komórek macierzystych pęcherzyka. Przy użyciu fluorescencyjnych reporterów i narzędzi genetycznych autorzy pokazują, że w normalnych warunkach te ścieżki są włączone w pokrywających się, ale odrębnych wzorcach. Co ważne, każdy szlak kontroluje własny zestaw genów docelowych i nie po prostu włącza lub wyłącza drugi. Ta niezależność oznacza, że komórka integruje dwie oddzielne informacje o tym, kiedy się dzielić, a kiedy przechodzić w dojrzały stan.
Gdy Hedgehog lub EGFR-Ras idą w złym kierunku
Aby sprawdzić, co się dzieje, gdy te sygnały są nadmiernie silne, badacze sztucznie zwiększyli aktywność Hh lub EGFR-Ras w dorosłych jajnikach, a następnie zastosowali sekwencjonowanie RNA pojedynczych komórek dla dziesiątek tysięcy pojedynczych komórek. Nadaktywne EGFR-Ras przede wszystkim popycha komórki do kontynuowania cykli podziałowych zamiast wychodzenia z typowego programu podziałowego, opóźniając kluczowy przełącznik na bardziej zrelaksowany endocycl w komórkach głównych. Nadaktywne Hh ma inny efekt: uwięzi wiele komórek w mieszanej tożsamości. Zachowują cechy niedojrzałych komórek, jednocześnie włączając geny typowe dla komórek szypułkowych oraz markery związane z przejściem epitelialno-mezenchymalnym (EMT), procesem związanym ze zwiększoną ruchliwością i rozprzestrzenianiem się raka. W tych jajnikach z podwyższonym Hh komórki tracą zwykłą polaryzację, przemieszczają się nietypowo i czasem inwazują obszary, których normalnie nie zajmują.
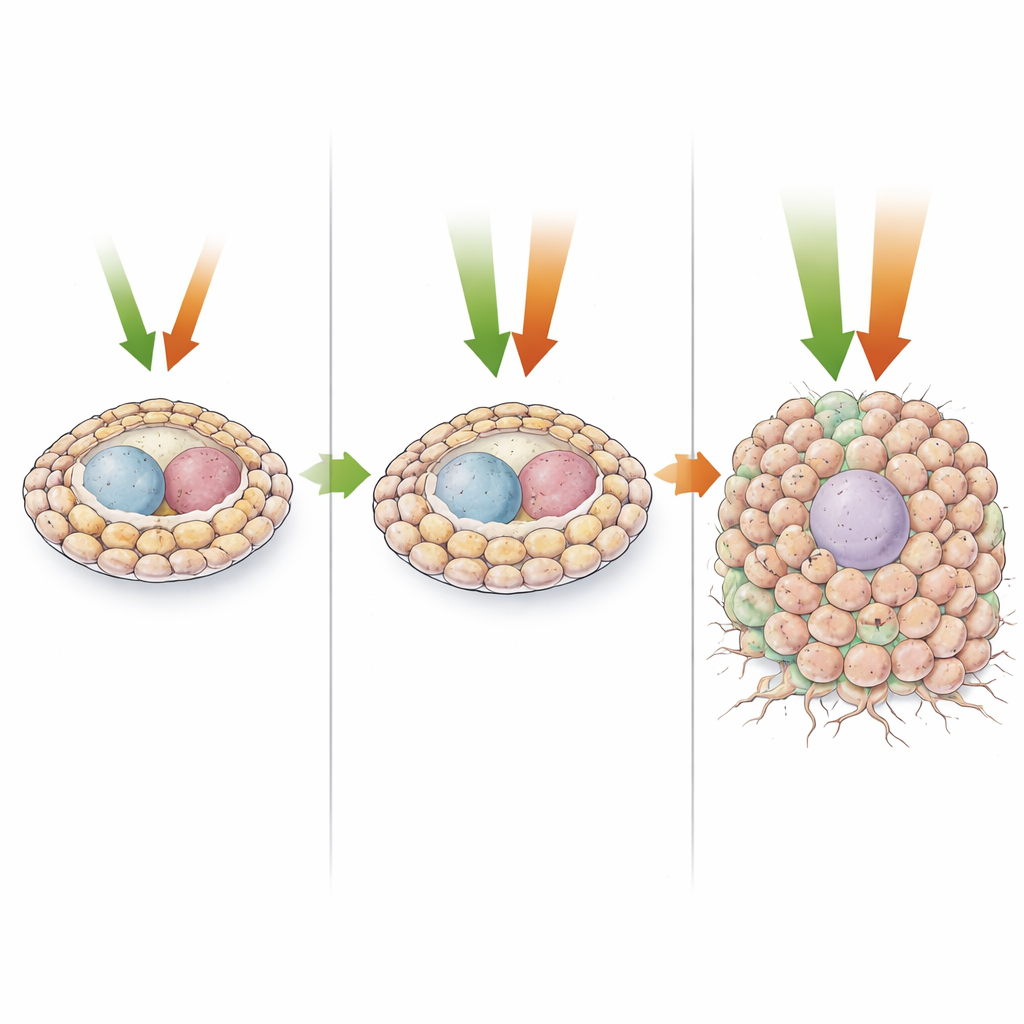
Gdy obie ścieżki uruchamiają się jednocześnie
Najbardziej dramatyczne zmiany pojawiają się, gdy oba szlaki są jednocześnie nadaktywowane. Wtedy potomstwo przypominające komórki macierzyste rozrasta się masowo, nie dojrzewając, tworząc duże, nieuporządkowane skupiska komórek z niewielką liczbą pozostających komórek germinalnych. Analizy pojedynczych komórek ujawniają, że większość tych komórek przypomina wczesnych progenitorów raczej niż w pełni zróżnicowane typy i znajduje się na samym początku trajektorii rozwojowych. Te przerosłe tkanki wykazują wiele cech złośliwości: utrzymującą się proliferację z skróconymi fazami odpoczynku, zdezorganizowaną architekturę tkanki, utratę polaryzacji, zmieniony metabolizm oraz poważne obciążenie dla przeżycia gospodarza. Badanie wyznacza także dwa czynniki transkrypcyjne, Zfh1 (powiązany z ludzkimi ZEB1/2) i Pointed (powiązany z ETS1/2), jako kluczowych graczy pośredniczących odpowiednio w zachowaniu przypominającym EMT i nadmiernej proliferacji.
Co to znaczy dla biologii raka
Mówiąc prościej, praca ta pokazuje, że normalne zdrowie tkanki w jajniku zależy od ostrożnej równowagi między dwoma niezależnymi, lecz zbieżnymi systemami sygnalizacyjnymi. Sam Hedgehog popycha komórki ku częściowo ruchliwemu, przypominającemu komórki szypułkowe stanowi, podczas gdy sam EGFR-Ras utrzymuje ich podziały. Gdy obie ścieżki są jednocześnie nadmiernie włączone, komórki utkną w niedojrzałym, wysoce proliferacyjnym i inwazyjnym stanie, który blisko przypomina wczesne etapy rozwoju guza. Ponieważ podstawowe składniki tych ścieżek są zachowane od muszek po ludzi, wyniki dostarczają genetycznie przystępnego modelu do zrozumienia, jak kombinacje sygnałów wzrostu i przełączników tożsamości mogą współpracować, by napędzać raka, oraz dlaczego jednoczesne ukierunkowanie zarówno sygnalizacji Hedgehog, jak i EGFR-Ras może być szczególnie skuteczne w leczeniu niektórych nowotworów nabłonkowych.
Cytowanie: Anschütz, S., Müller, H., Schubert, A. et al. Hh and EGFR-Ras signaling promote distinct steps of tumor progression in the Drosophila follicle epithelium. Nat Commun 17, 2790 (2026). https://doi.org/10.1038/s41467-026-70844-y
Słowa kluczowe: Jajnik Drosophila, Sygnalizacja Hedgehog, Szlak EGFR-Ras, progresja guza nabłonkowego, epithelial-mesenchymal transition