Clear Sky Science · fr
La signalisation Hh et EGFR-Ras favorise des étapes distinctes de la progression tumorale dans l’épithélium folliculaire de Drosophila
Comment les cellules maintiennent l’équilibre des tissus
Nos organismes, comme ceux des mouches du vinaigre, renouvellent constamment leurs tissus. Pour rester en bonne santé, les cellules souches doivent se diviser et se différencier en types cellulaires appropriés au bon moment, tout en évitant les comportements incontrôlés qui conduisent au cancer. Cette étude utilise l’ovaire de Drosophila comme modèle puissant pour révéler comment deux grands systèmes de communication entre cellules coopèrent pour maintenir une croissance normale — et comment leur dérèglement peut entraîner une surcroissance de type tumoral.
Un petit organe aux grandes leçons
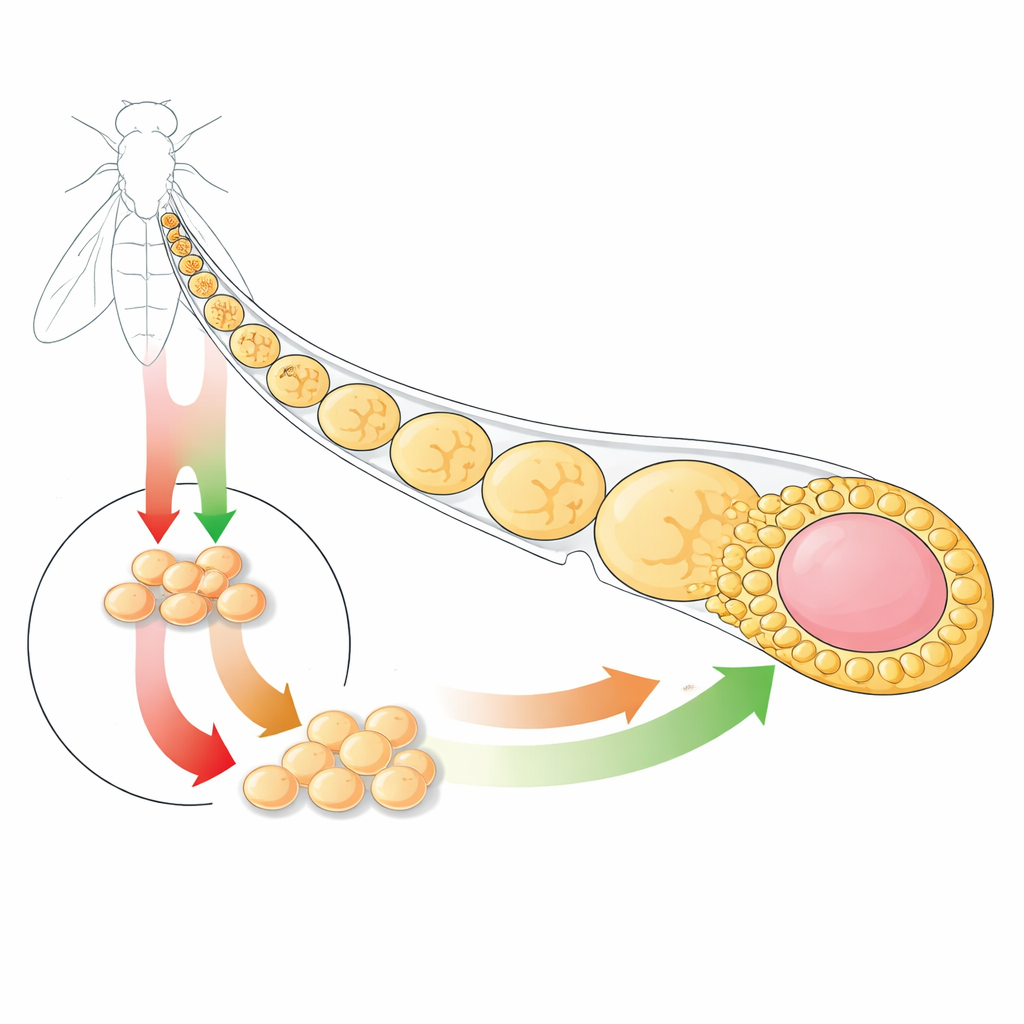
Les chercheurs se concentrent sur l’épithélium folliculaire de l’ovaire de la mouche, une mince couche cellulaire qui entoure les chambres ovocytaires en développement. Ce tissu est entretenu par des cellules souches folliculaires installées dans une niche définie et qui produisent des cellules filles se spécialisant ensuite en plusieurs rôles, comme les cellules du corps principal qui recouvrent l’œuf, les cellules de pédicule qui relient les chambres ovocytaires, et les cellules polaires qui aident à organiser la structure. Parce que tous ces événements se déroulent dans une zone très restreinte et se répètent de nombreuses fois, ce système est idéal pour étudier comment les signaux contrôlent à la fois la prolifération et la différenciation dans un épithélium vivant.
Deux messages clés : croissance et changement
L’équipe examine deux voies de signalisation majeures : Hedgehog (Hh) et EGFR-Ras. Toutes deux sont impliquées dans le cancer humain et sont actives dans la région des cellules souches folliculaires chez la mouche. À l’aide de témoins fluorescents et d’outils génétiques, les auteurs montrent que dans des conditions normales ces voies sont activées selon des motifs qui se chevauchent mais demeurent distincts. Surtout, chaque voie contrôle son propre ensemble de gènes cibles et n’agit pas simplement en allumant ou en éteignant l’autre. Cette indépendance signifie que la cellule intègre deux messages séparés sur le moment de proliférer et celui d’évoluer vers un destin mature.
Quand Hedgehog ou EGFR-Ras dysfonctionnent
Pour observer ce qui se passe lorsque ces signaux sont trop intenses, les chercheurs augmentent artificiellement l’activité de Hh ou d’EGFR-Ras dans des ovaires adultes puis appliquent le séquençage ARN unicellulaire à des dizaines de milliers de cellules individuelles. L’hyperactivation d’EGFR-Ras pousse principalement les cellules à continuer de se diviser au lieu de quitter le programme normal de division, retardant un passage clé vers un endocycle plus relaxé dans les cellules du corps principal. L’hyperactivation de Hh a un effet différent : elle piège de nombreuses cellules dans une identité mixte. Elles conservent des caractéristiques de cellules immatures tout en exprimant des gènes typiques des cellules de pédicule et des marqueurs liés à la transition épithélio-mésenchymateuse (EMT), un processus associé à une motilité accrue et à la dissémination cancéreuse. Dans ces ovaires stimulés par Hh, les cellules perdent leur polarité habituelle, se déplacent anormalement et envahissent parfois des régions qu’elles n’occupent normalement pas.
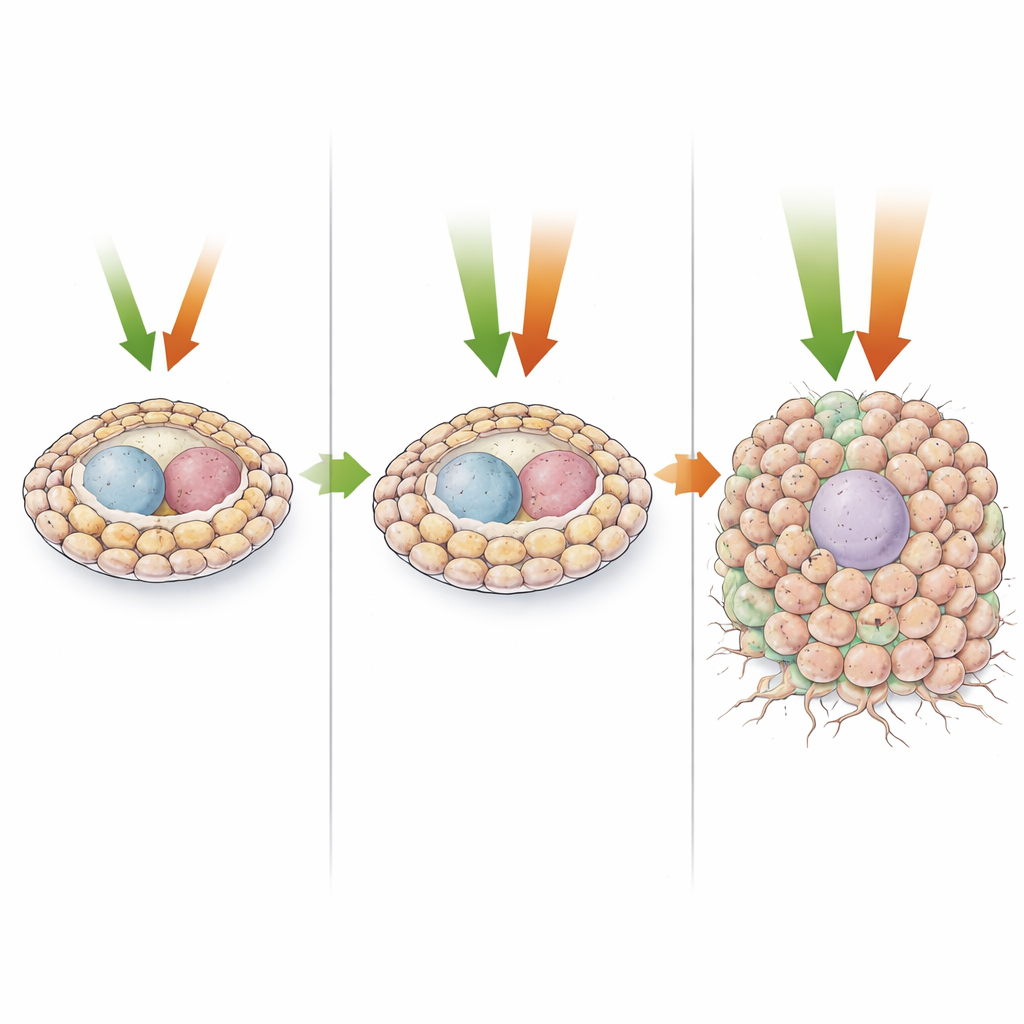
Quand les deux signaux s’activent simultanément
Les modifications les plus spectaculaires apparaissent lorsque les deux voies sont suractivées ensemble. Ici, les descendants ressemblant à des cellules souches se multiplient massivement sans mûrir, formant de grandes masses cellulaires désorganisées avec peu de cellules germinales résiduelles. Les analyses unicellulaires montrent que la plupart de ces cellules ressemblent à des progéniteurs précoces plutôt qu’à des types différenciés et se situent au tout début des trajectoires de développement. Ces tissus hypertrophiés présentent de nombreux signes de malignité : division cellulaire soutenue avec phases de repos raccourcies, architecture tissulaire bouleversée, perte de polarité, métabolisme altéré et coût sévère pour la survie de l’hôte. L’étude identifie également deux facteurs de transcription, Zfh1 (lié aux humains ZEB1/2) et Pointed (lié à ETS1/2), comme acteurs en aval essentiels pour conduire respectivement un comportement de type EMT et une prolifération excessive.
Ce que cela signifie pour la biologie du cancer
En termes simples, ce travail montre que la santé tissulaire normale dans l’ovaire dépend d’un équilibre délicat entre deux systèmes de signalisation indépendants mais convergents. Hedgehog, seul, pousse les cellules vers un état partiellement mobile et ressemblant aux cellules de pédicule, tandis qu’EGFR-Ras, seul, les maintient en division. Lorsque les deux sont exagérément activés, les cellules restent bloquées dans un état indifférencié, fortement prolifératif et invasif qui rappelle de près les premiers stades du développement tumoral. Parce que les composants centraux de ces voies sont conservés des mouches aux humains, ces résultats fournissent un modèle génétique exploitable pour comprendre comment des combinaisons de signaux de croissance et de basculements d’identité peuvent coopérer pour entraîner le cancer, et pourquoi cibler à la fois la signalisation Hedgehog et EGFR-Ras pourrait être particulièrement efficace pour traiter certains tumeurs épithéliales.
Citation: Anschütz, S., Müller, H., Schubert, A. et al. Hh and EGFR-Ras signaling promote distinct steps of tumor progression in the Drosophila follicle epithelium. Nat Commun 17, 2790 (2026). https://doi.org/10.1038/s41467-026-70844-y
Mots-clés: Ovaire de Drosophila, Signalisation Hedgehog, Voie EGFR-Ras, progression tumorale épithéliale, transition épithélio-mésenchymateuse