Clear Sky Science · de
Hh- und EGFR‑Ras‑Signale fördern unterschiedliche Schritte der Tumorprogression im Follikelepithel von Drosophila
Wie Zellen das Gewebe im Gleichgewicht halten
Unsere Körper, ebenso wie die von Fruchtfliegen, erneuern ständig ihr Gewebe. Um gesund zu bleiben, müssen Stammzellen sich zur richtigen Zeit teilen und in die passenden Zelltypen ausreifen, während sie das unkontrollierte Verhalten vermeiden, das zu Krebs führt. Diese Studie nutzt den Ovar von Drosophila als leistungsfähiges Modell, um zu untersuchen, wie zwei wichtige Kommunikationssysteme zwischen Zellen zusammenarbeiten, um normales Wachstum zu erhalten — und wie ihr Versagen tumorähnliche Überwüchse antreiben kann.
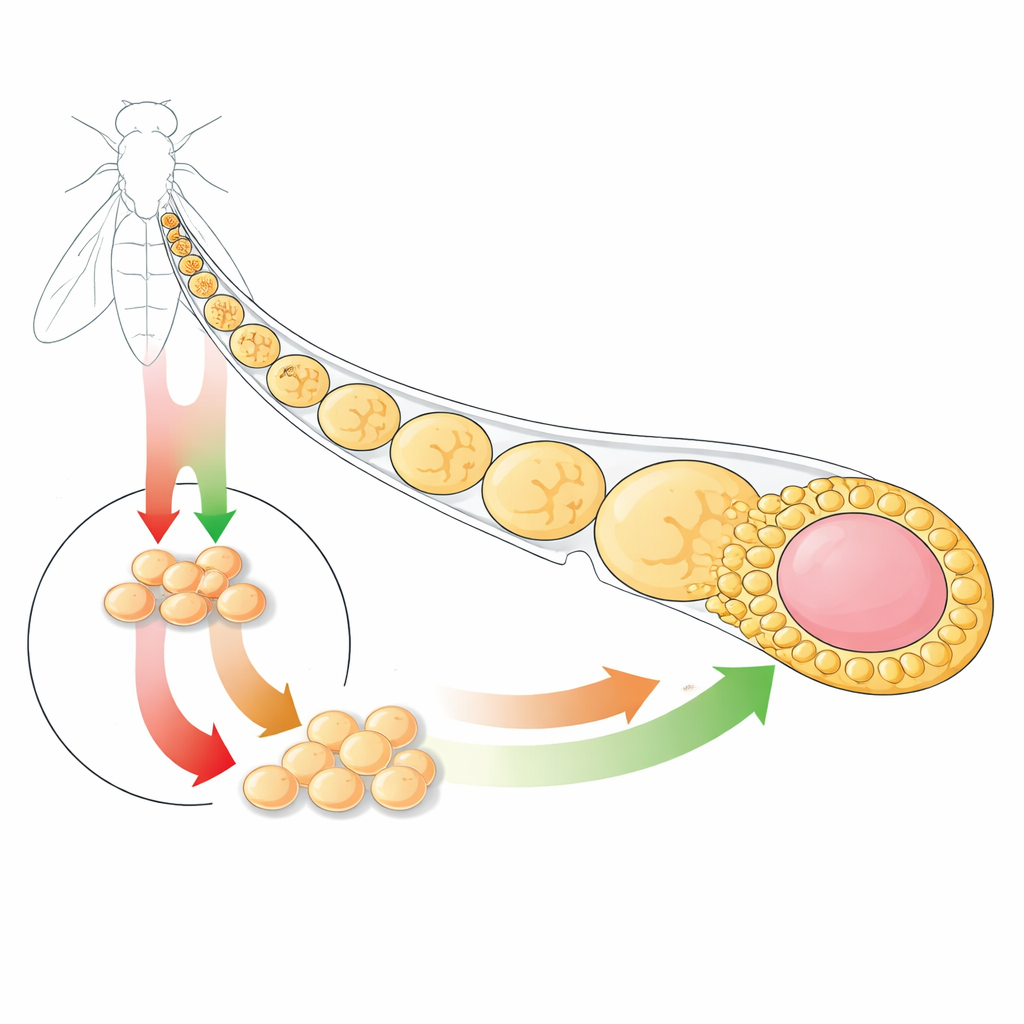
Ein winziges Organ mit großen Lehren
Die Forschenden konzentrieren sich auf das Follikelepithel im Ovar der Fruchtfliege, eine einfache Zellschicht, die sich um die sich entwickelnden Eizellen legt. Dieses Gewebe wird von Follikelstammzellen erhalten, die in einer definierten Nische sitzen und Tochterzellen produzieren, die sich dann in verschiedene Rollen spezialisieren, etwa Hauptkörperzellen, die das Ei bedecken, Stielzellen, die Eikammern verbinden, und Polzellen, die die Struktur organisieren helfen. Da all diese Ereignisse in einem sehr kleinen Bereich stattfinden und vielfach wiederholt werden, ist das System ideal, um zu untersuchen, wie Signale Proliferation und Differenzierung in einem lebenden Epithel steuern.
Zwei zentrale Botschaften: Wachstum und Umwandlung
Das Team untersucht zwei wichtige Signalwege: Hedgehog (Hh) und EGFR‑Ras. Beide sind aus dem menschlichen Krebs bekannt und sind in der Region der Follikelstammzellen der Fliege aktiv. Mit fluoreszenten Reportern und genetischen Werkzeugen zeigen die Autorinnen und Autoren, dass diese Wege unter normalen Bedingungen in überlappenden, aber unterschiedlichen Mustern aktiviert sind. Wichtig ist: Jeder Weg steuert seine eigene Menge an Zielgenen und schaltet den anderen nicht einfach ein oder aus. Diese Unabhängigkeit bedeutet, dass die Zelle zwei getrennte Botschaften darüber integriert, wann sie proliferieren und wann sie in Richtung eines reifen Schicksals voranschreiten soll.
Wenn Hedgehog oder EGFR‑Ras fehlregulieren
Um zu sehen, was passiert, wenn diese Signale zu stark sind, verstärken die Forschenden künstlich entweder Hh oder EGFR‑Ras in adulten Ovarien und wenden dann Einzelzell‑RNA‑Sequenzierung auf zigtausende einzelne Zellen an. Überaktives EGFR‑Ras treibt Zellen überwiegend dazu, weiter zu teilen statt das übliche Teilungsprogramm zu verlassen und einen wichtigen Wechsel in einen entspannten Endozyklus der Hauptkörperzellen zu vollziehen. Überaktives Hh hat einen anderen Effekt: Es fängt viele Zellen in einer gemischten Identität ein. Sie behalten Merkmale unreifer Zellen, schalten aber zugleich Gene an, die für Stielzellen typisch sind, sowie Marker, die mit der epithelial‑mesenchymalen Transition (EMT) verknüpft sind — einem Prozess, der mit erhöhter Beweglichkeit und Krebsstreuung assoziiert ist. In diesen Hh‑verstärkten Ovarien verlieren Zellen ihre typische Polarität, kriechen abnormal und dringen mitunter in Bereiche ein, die sie normalerweise nicht besetzen.
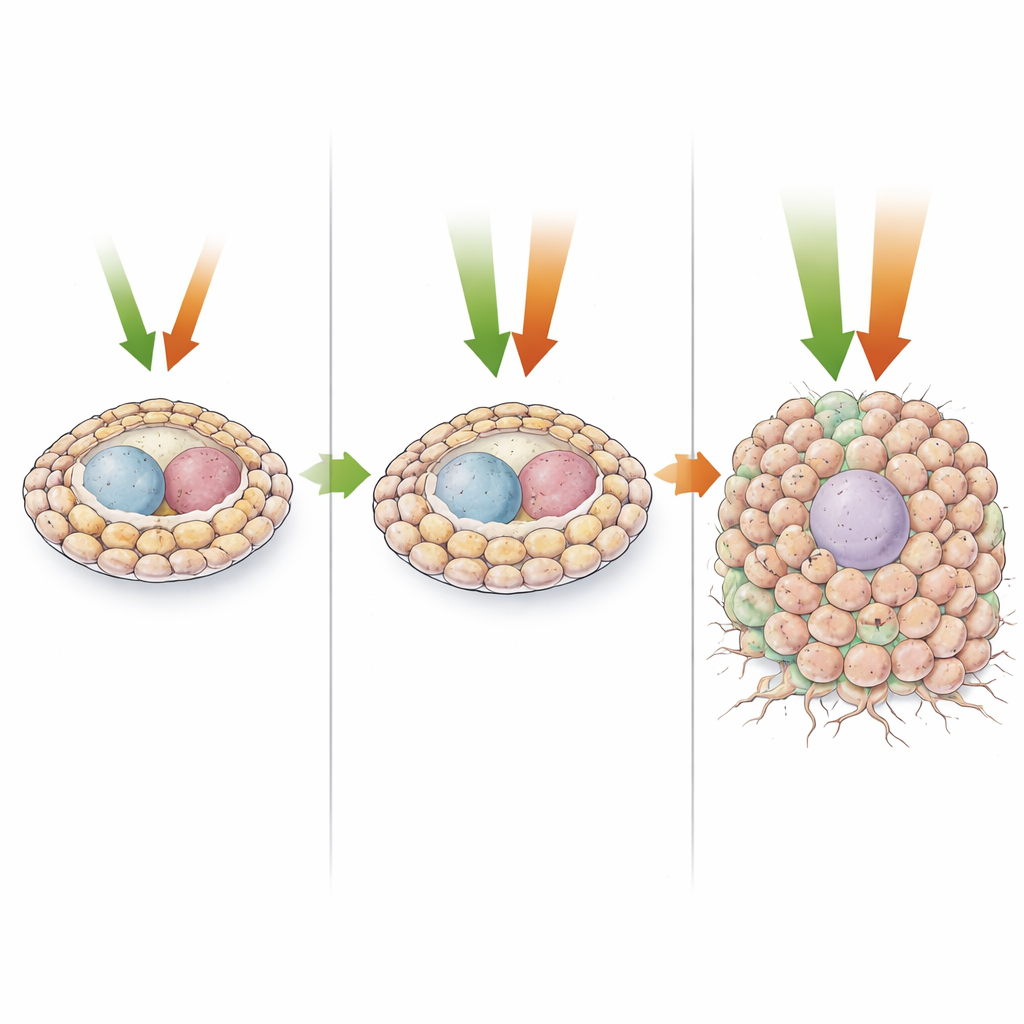
Wenn beide Signale gleichzeitig feuern
Die dramatischsten Veränderungen treten auf, wenn beide Wege gleichzeitig überaktiviert werden. Hier expandieren stammzellähnliche Nachfahren massiv, ohne auszureifen, und bilden große, desorganisierte Zellmassen mit nur wenigen verbleibenden Keimzellen. Einzelzellanalysen zeigen, dass die meisten dieser Zellen frühen Vorläufern ähneln statt vollständig differenzierten Typen und am Beginn der Entwicklungstrajektorien stehen. Diese überwachsenen Gewebe zeigen viele Kennzeichen von Malignität: anhaltende Zellteilung mit verkürzten Ruhephasen, zerstörte Gewebearchitektur, Verlust der Polarität, veränderten Stoffwechsel und schwere Folgen für das Überleben des Wirts. Die Studie identifiziert außerdem zwei Transkriptionsfaktoren, Zfh1 (verwandt mit humanen ZEB1/2) und Pointed (verwandt mit ETS1/2), als wichtige nachgeschaltete Akteure, die jeweils die EMT‑ähnlichen Eigenschaften bzw. die übermäßige Proliferation antreiben.
Was das für die Krebsbiologie bedeutet
Vereinfacht gesagt zeigt diese Arbeit, dass die normale Gesundheit des Ovargewebes von einem sorgfältigen Gleichgewicht zwischen zwei unabhängigen, aber konvergierenden Signalsystemen abhängt. Hedgehog allein schiebt Zellen in einen teilweise mobilen, stielzelligen Zustand, während EGFR‑Ras sie allein zur Teilung zwingt. Wenn beide ectopisch hochreguliert sind, bleiben Zellen in einem undifferenzierten, hochproliferativen und invasiven Zustand stecken, der frühen Schritten der Tumorentwicklung sehr ähnlich ist. Da die Kernkomponenten dieser Wege von Fliegen bis zu Menschen konserviert sind, liefern die Befunde ein genetisch gut zugängliches Modell, um zu verstehen, wie Kombinationen von Wachstumssignalen und Identitätswechseln zusammenarbeiten können, um Krebs zu treiben, und warum die gleichzeitige Zielansteuerung von Hedgehog‑ und EGFR‑Ras‑Signalgebung insbesondere bei bestimmten epithelialen Tumoren besonders wirksam sein könnte.
Zitation: Anschütz, S., Müller, H., Schubert, A. et al. Hh and EGFR-Ras signaling promote distinct steps of tumor progression in the Drosophila follicle epithelium. Nat Commun 17, 2790 (2026). https://doi.org/10.1038/s41467-026-70844-y
Schlüsselwörter: Drosophila‑Ovary, Hedgehog‑Signalvermittlung, EGFR‑Ras‑Weg, epitheliale Tumorprogression, epitheliale‑mesenchymale Transition