Clear Sky Science · pl
Neurotroficzny czynnik pochodzenia mózgowego i pochodny dodekapeptyd działają jako antagoniści receptora Toll‑like 4 w ostrym uszkodzeniu płuc
Dlaczego łagodzenie zapalenia płuc ma znaczenie
Ostre uszkodzenie płuc i jego ciężka postać, zespół ostrej niewydolności oddechowej (ARDS), mogą przekształcić rutynową infekcję lub uraz w zagrażający życiu kryzys w ciągu kilku godzin. W tych stanach płuca wypełniają się płynem i komórkami zapalnymi, co utrudnia lub uniemożliwia oddychanie. Obecne terapie głównie wspomagają oddychanie, ale niewiele robią, by stłumić leżącą u podstaw burzę zapalną. Badanie to odkrywa zaskakujący, naturalny hamulec wewnątrz samych płuc — białko związane z nerwami i niewielki jego fragment — które potrafią przygasić postępującą reakcję immunologiczną i mogą zainspirować nowe leki zarówno przeciw niewydolności płuc, jak i sepsie.
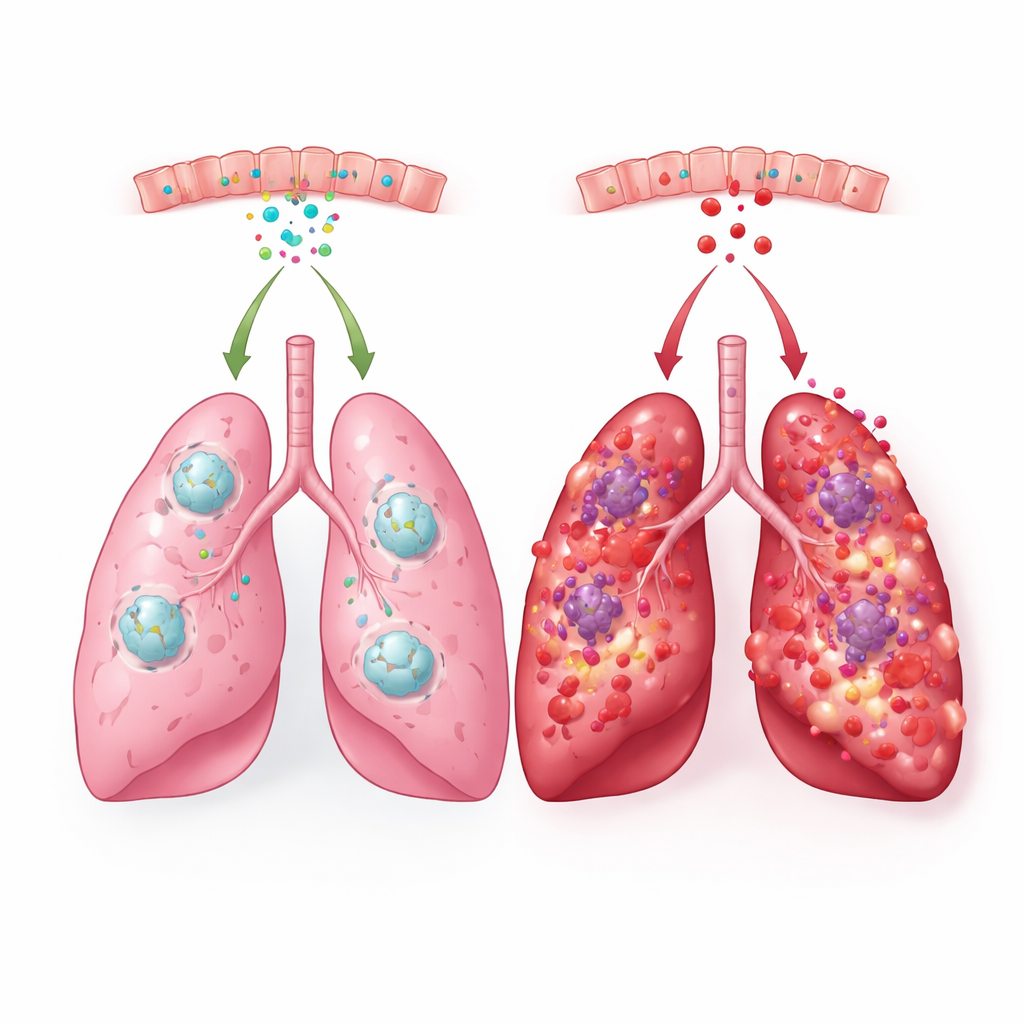
Pomocnik nerwowy z niespodziewaną rolą w płucach
Neurotroficzny czynnik pochodzenia mózgowego (BDNF) jest najbardziej znany jako cząsteczka wspierająca wzrost, przeżycie i tworzenie nowych połączeń przez komórki nerwowe. Autorzy zastanawiali się, czy BDNF i powiązane czynniki mają znaczenie także w nagłych chorobach zapalnych poza mózgiem. Wykorzystując kilka modeli mysich ostrego uszkodzenia płuc i sepsy oraz publiczne zbiory danych od ludzi i zwierząt, przebadali dziewięć członków tej rodziny. Wśród nich wyróżnił się BDNF: jego aktywność genowa systematycznie spadała w uszkodzonych płucach, a poziomy białka zmniejszały się specyficznie w płynie kąpiącym pęcherzyki płucne, ale nie we krwi. Analizy pojedynczych komórek wykazały, że komórki nabłonka płuc — wyściełające pęcherzyki, gdzie zachodzi wymiana gazowa — są głównym lokalnym źródłem BDNF, a ich produkcja BDNF maleje podczas ciężkiego zapalenia.
Więcej BDNF, mniej uszkodzeń
Aby sprawdzić, czy ten spadek BDNF jedynie towarzyszy chorobie, czy rzeczywiście ma na nią wpływ, zespół zwiększył poziomy BDNF na różne sposoby. Zmienili genetycznie myszy tak, by komórki nabłonka płuc produkowały dodatkowy BDNF, a także leczyli normalne myszy wstrzykiwanym rekombinowanym białkiem BDNF. W modelach, gdzie toksyny bakteryjne wywoływały ostre uszkodzenie płuc, podany BDNF zmniejszał gromadzenie się płynu, przeciekanie białek do przestrzeni pęcherzykowych i pogrubienie cienkich ścianek pęcherzyków. Do płuc napływało mniej komórek odpornościowych, zwłaszcza neutrofili i makrofagów, a zwierzęta miały większe szanse przeżyć eksperymentalną sepsę. Pomiar mediatorów zapalnych, takich jak TNF‑α i IL‑6, był niższy zarówno w tkance płucnej, jak i w płynie płucnym, łącząc wyższe poziomy BDNF ze stonowaną odpowiedzią immunologiczną.
Makrofagi i kluczowy sensor niebezpieczeństwa
Naukowcy zapytali następnie, na które komórki działa BDNF. Odkryli, że kiedy makrofagi — komórki odpornościowe, które jako pierwsze wyczuwają inwazję bakterii w płucach — zostały usunięte z myszy, leczenie BDNF przestało chronić przed uszkodzeniem płuc i sepsą. W hodowanych makrofagach BDNF wyraźnie zmniejszał aktywność dziesiątek genów związanych z zapaleniem oraz uwalnianie wielu cytokin po ekspozycji na składniki bakteryjne. Dzięki przesiewom proteomicznym i testom wiązania autorzy odkryli, że BDNF przyłącza się bezpośrednio do receptora Toll‑like 4 (TLR4), głównego sensora niebezpieczeństwa na makrofagach, który rozpoznaje endotoksynę bakteryjną i uruchamia silne kaskady zapalne. BDNF konkuruje z częścią zwykłego kompleksu pomocniczego TLR4 o dostęp do zewnętrznej domeny receptora, blokując łańcuch sygnałów, który normalnie wzmacniałby zapalenie.
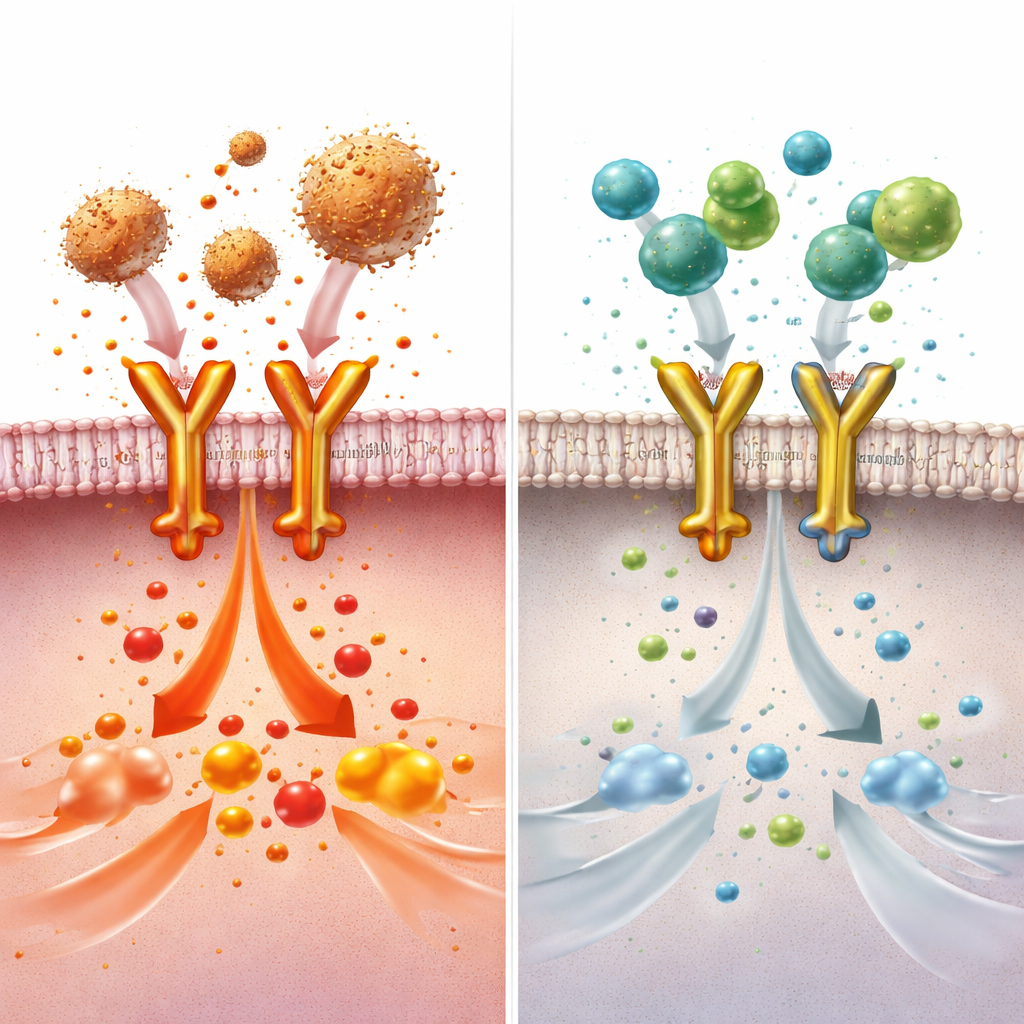
Maleńki peptyd o dużym potencjale
Ponieważ pełnej długości BDNF może stymulować wzrost komórek przez jego klasyczny receptor nerwowy i w niektórych kontekstach wiązano go z rakiem, badacze poszukiwali mniejszego, bezpieczniejszego fragmentu zachowującego efekt przeciwzapalny. Poprzez trawienie BDNF i mapowanie, które fragmenty wiążą się z zewnętrzną częścią TLR4, zidentyfikowali 12‑aminokwasowy odcinek nazwany BDP‑12, który mocno przyłącza się do TLR4, ale nie aktywuje szlaków promujących wzrost. W testach komórkowych BDP‑12 blokował formowanie kompleksu pomocniczego TLR4 i silniej niż pełny BDNF tłumił aktywność genów zapalnych, a jego działanie znikało po usunięciu TLR4, co wskazuje na wysoką specyficzność. U myszy z toksyną wywołującą uszkodzenie płuc lub z polimikrobaialną sepsą BDP‑12 zmniejszał uszkodzenia tkanek, obrzęk płuc i infiltrację komórek odpornościowych w płucach, sercu i nerkach, jednocześnie poprawiając przeżywalność. Co ważne, powtarzane podawanie nie wywołało dodatkowej proliferacji komórek w tkance płucnej, sugerując niższe ryzyko efektów ubocznych przypominających rozwój nowotworów.
Co to może znaczyć dla przyszłych terapii
Praca ta ujawnia dotąd nieznaną rozmowę między komórkami powierzchni płuc a komórkami odpornościowymi: nabłonkowy BDNF zwykle pomaga powściągać zapalenie napędzane przez makrofagi, bezpośrednio blokując kluczowy receptor niebezpieczeństwa. Kiedy poziomy BDNF spadają podczas ciężkiej infekcji, ten hamulec zostaje zwolniony, a uszkodzenia przyspieszają. Zdestylowanie BDNF do krótkiego peptydu BDP‑12, który nadal antagonizuje TLR4, ale nie wykazuje aktywności stymulującej wzrost, daje obiecujący plan działania przy opracowywaniu leków, które mogłyby uspokoić przytłaczające zapalenie płuc i całego organizmu w ostrym uszkodzeniu płuc, sepsie i być może w innych chorobach zapalnych.
Cytowanie: Zhu, W., Jin, L., Zhang, Q. et al. Brain-derived neurotrophic factor and the derived dodecapeptide function as Toll-like receptor 4 antagonists in acute lung injury. Nat Commun 17, 2786 (2026). https://doi.org/10.1038/s41467-026-69541-7
Słowa kluczowe: ostre uszkodzenie płuc, BDNF, TLR4, zapalenie makrofagów, peptyd terapeutyczny