Clear Sky Science · de
Hirn‑abgeleiteter neurotropher Faktor und das abgeleitete Dodekapetid wirken als TLR4‑Antagonisten bei akutem Lungenschaden
Warum die Beruhigung von Lungenentzündungen wichtig ist
Akuter Lungenschaden und seine schwere Form, das akute Atemnotsyndrom (ARDS), können eine alltägliche Infektion oder ein Trauma innerhalb weniger Stunden in eine lebensbedrohliche Krise verwandeln. Bei diesen Zuständen füllen sich die Lungen mit Flüssigkeit und entzündlichen Zellen, sodass das Atmen schwer oder unmöglich wird. Die aktuellen Therapien stützen vor allem die Atmung, zielen aber nur wenig auf den zugrunde liegenden Entzündungssturm ab. Diese Studie deckt eine überraschende natürliche Bremse in den Lungen selbst auf — ein nervenbezogenes Protein und ein winziges Fragment davon — die überschiessende Immunreaktionen dämpfen kann und neue Arzneimittel für Lungenversagen und Sepsis anregen könnte.
Ein Helfer der Nerven mit unerwarteter Lungenrolle
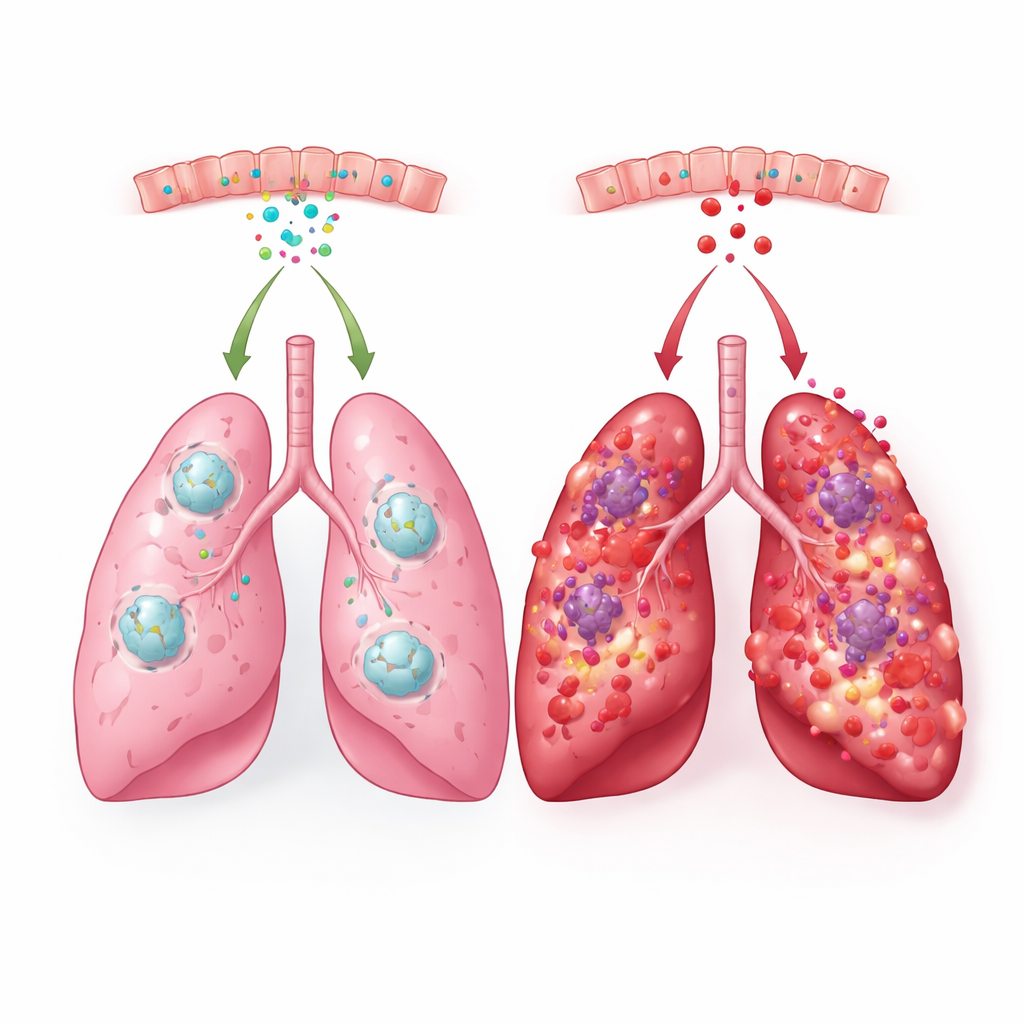
Der hirn‑abgeleitete neurotrope Faktor (BDNF) ist vor allem als Molekül bekannt, das Nervenzellen beim Wachsen, Überleben und beim Ausbilden neuer Verbindungen hilft. Die Autoren fragten, ob BDNF und verwandte Faktoren auch bei plötzlichen entzündlichen Erkrankungen außerhalb des Gehirns eine Rolle spielen. Mithilfe mehrerer Mausmodelle für akuten Lungenschaden und Sepsis sowie öffentlicher humaner und tierischer Datensätze untersuchten sie neun Mitglieder dieser Familie. Unter ihnen hob sich BDNF ab: Seine Genaktivität ging in verletzten Lungen konstant zurück, und die Proteinspiegel sanken speziell in der Flüssigkeit, die die Lungenbläschen umgibt, jedoch nicht im Blut. Einzelzellanalysen zeigten, dass Lungenepithelzellen — die Zellen, die die Luftbläschen auskleiden, wo der Gasaustausch stattfindet — die wichtigste lokale Quelle von BDNF sind und dass deren BDNF‑Produktion bei starker Entzündung abnimmt.
Mehr BDNF, weniger Schaden
Um zu prüfen, ob dieser Abfall von BDNF lediglich ein Begleiter der Krankheit ist oder sie tatsächlich beeinflusst, verstärkte das Team BDNF auf verschiedene Weise. Sie erzeugten Mäuse, bei denen Lungenepithelzellen zusätzliches BDNF produzierten, und behandelten außerdem normale Mäuse mit injiziertem rekombinantem BDNF‑Protein. In Modellen, in denen bakterielle Toxine einen akuten Lungenschaden auslösten, verringerte zusätzliches BDNF die Flüssigkeitsansammlung, das Austreten von Proteinen in die Lufträume und die Verdickung der feinen Alveolarwände. Weniger Immunzellen, insbesondere Neutrophile und Makrophagen, strömten in die Lungen, und die Tiere überlebten experimentelle Sepsis häufiger. Messungen entzündlicher Botenstoffe wie TNF‑α und IL‑6 fielen sowohl im Lungengewebe als auch in der Lungenflüssigkeit, was höheren BDNF‑Werten eine ruhigere Immunantwort zuordnet.
Makrophagen und ein wichtiger Gefahrensensor
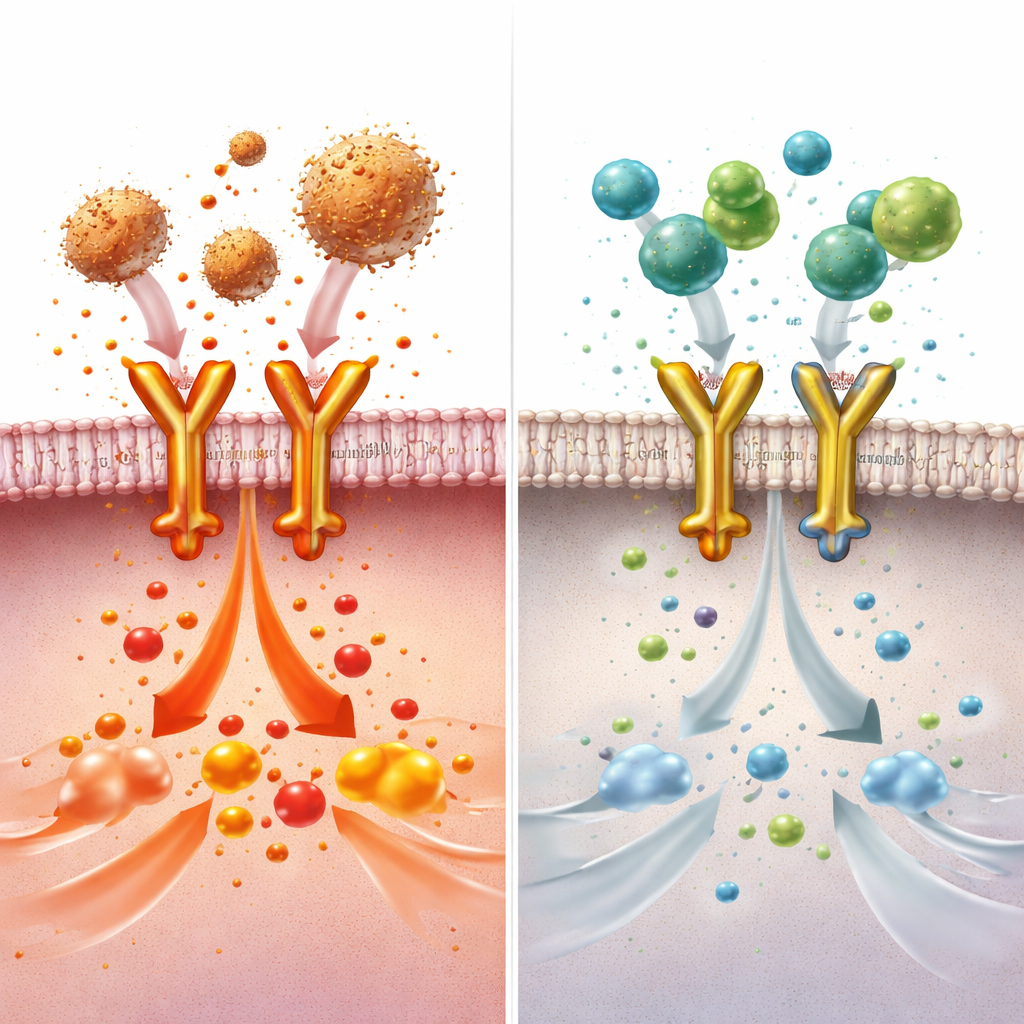
Die Forscher stellten als Nächstes die Frage, auf welche Zellen BDNF wirkt. Sie fanden heraus, dass BDNF‑Behandlung nicht mehr vor Lungenschaden oder Sepsis schützte, wenn Makrophagen — die Immunzellen, die in den Lungen als Erste eindringende Bakterien wahrnehmen — aus Mäusen entfernt wurden. In kultivierten Makrophagen reduzierte BDNF die Aktivität Dutzender entzündungsbezogener Gene stark und verringerte die Freisetzung mehrerer Zytokine nach Exposition gegenüber bakteriellen Komponenten. Mithilfe proteomischer Screens und Bindungsassays entdeckten die Autoren, dass BDNF direkt an Toll‑like‑Rezeptor 4 (TLR4) bindet, einen wichtigen Gefahrensensor auf Makrophagen, der bakterielles Endotoxin erkennt und mächtige Entzündungskaskaden auslöst. BDNF konkurriert mit einem Teil des üblichen TLR4‑Helferkomplexes um den Zugang zur äußeren Domäne des Rezeptors und blockiert dadurch die Signalkette, die normalerweise die Entzündung verstärkt.
Ein winziges Peptid mit großem Potenzial
Da voll‑length BDNF über seinen klassischen Nervenzellrezeptor Zellwachstum stimulieren kann und in einigen Kontexten mit Krebs in Verbindung gebracht wurde, suchten die Forscher nach einem kleineren, sichereren Fragment, das die anti‑entzündliche Wirkung bewahrt. Durch Verdau von BDNF und Kartierung der Stücke, die an die äußere Portion von TLR4 binden, identifizierten sie eine 12‑Aminosäure‑Sequenz, genannt BDP‑12, die stark an TLR4 anhaftet, aber keine wachstumsfördernden Signalwege aktiviert. In Zelltests blockierte BDP‑12 die Bildung des TLR4‑Helferkomplexes und unterdrückte die Aktivität entzündlicher Gene stärker als voll‑ständiges BDNF; seine Wirkung verschwand, wenn TLR4 entfernt wurde, was auf hohe Spezifität hinweist. Bei Mäusen mit toxininduziertem Lungenschaden oder polymikrobieller Sepsis verringerte BDP‑12 Gewebeschäden, Lungenödem und die Infiltration von Immunzellen in Lunge, Herz und Nieren und verbesserte das Überleben. Wichtig ist, dass wiederholte Gaben kein zusätzliches Zellwachstum im Lungengewebe förderten, was auf ein geringeres Risiko tumortypischer Nebenwirkungen hindeutet.
Was das für künftige Therapien bedeuten könnte
Diese Arbeit zeigt eine zuvor unerkannte Kommunikation zwischen Oberflächenzellen der Lunge und Immunzellen auf: Epitheliales BDNF hilft normalerweise, von Makrophagen gesteuerte Entzündungen in Schach zu halten, indem es direkt einen Schlüssel‑Gefahrensensor blockiert. Fällt der BDNF‑Spiegel bei schwerer Infektion, löst sich diese Bremse und der Schaden beschleunigt sich. Indem die Autoren BDNF auf das kurze Peptid BDP‑12 destillieren, das weiterhin TLR4 antagonisiert, aber keine wachstumsstimulierende Aktivität besitzt, liefert die Studie einen vielversprechenden Bauplan für Medikamente, die überwältigende Lungen‑ und systemische Entzündungen bei akutem Lungenschaden, Sepsis und möglicherweise anderen entzündlichen Erkrankungen dämpfen könnten.
Zitation: Zhu, W., Jin, L., Zhang, Q. et al. Brain-derived neurotrophic factor and the derived dodecapeptide function as Toll-like receptor 4 antagonists in acute lung injury. Nat Commun 17, 2786 (2026). https://doi.org/10.1038/s41467-026-69541-7
Schlüsselwörter: akuter Lungenschaden, BDNF, TLR4, Makrophagen‑Entzündung, therapeutisches Peptid