Clear Sky Science · nl
Een generaliseerbare methode voor het opsporen van oogziekten gebaseerd op Zero‑Shot Learning
Waarom vroege oogwaarschuwingen belangrijk zijn
Veel ernstige oogaandoeningen beginnen met zo subtiele veranderingen dat zelfs getrainde specialisten ze soms moeilijk kunnen zien. Milde diabetische retinopathie, een vroeg complicatie van diabetes, is zo’n stil waarschuwingssignaal: vroegtijdige opsporing kan verlies van gezichtsvermogen voorkomen, maar vereist nauwkeurige inspectie van retinafoto’s en een enorm aantal deskundig gelabelde afbeeldingen om de huidige kunstmatige intelligentiesystemen (AI) te trainen. Deze studie introduceert een nieuw type AI dat kan leren vroege ziekte te herkennen, zelfs wanneer artsen nooit voorbeelden van die specifieke aandoening hebben gelabeld, wat mogelijk de weg vrijmaakt voor snellere en betaalbaardere oogscreening wereldwijd.
Een nieuwe manier om machines zonder voorbeelden te leren
De onderzoekers bouwen voort op het concept zero‑shot learning, waarbij een AI‑systeem iets nieuws leert herkennen zonder eerder gelabelde voorbeelden te hebben gezien. In plaats van ziekten te memoriseren, bootst het systeem na hoe clinici redeneren: het zoekt naar verwante aandoeningen die visuele patronen delen en draagt het geleerde daarvan over. Hier richtte het team zich op milde diabetische retinopathie (DR1), maar trainde hun methode zonder één enkele als zodanig gelabelde DR1‑afbeelding. In plaats daarvan stelden ze een enorme verzameling retinafoto’s samen, het LCFP‑14M‑dataset, met meer dan een miljoen afbeeldingen en elf oogziektecategorieën afkomstig uit vele openbare databanken. Deze rijke mix van beelden biedt de visuele "ervaring" waaruit de AI patronen van ziekte kan afleiden.
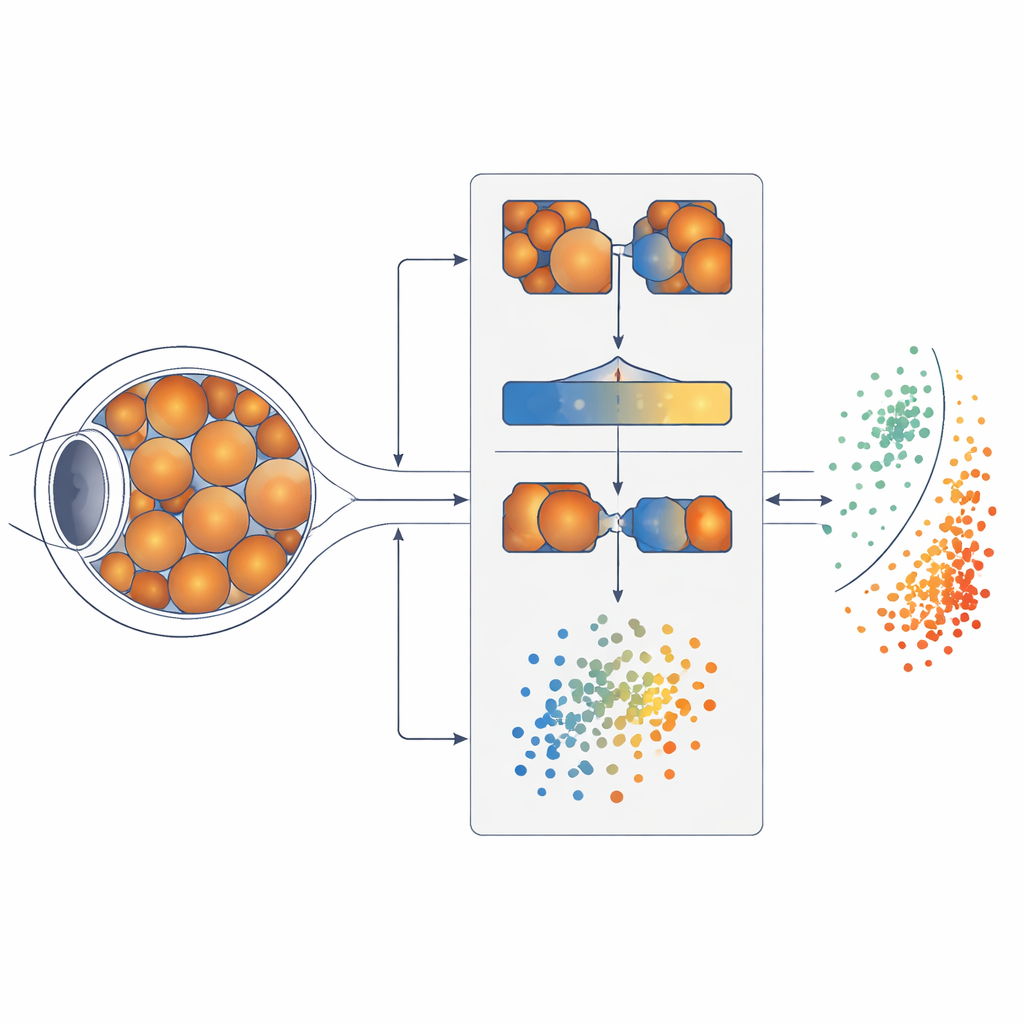
Een uiterlijk gelijkende ziekte vinden
Om te bepalen waar kennis te lenen valt, is de eerste stap van het systeem het meten van hoe vergelijkbaar verschillende oogaandoeningen eruitzien. Het team gebruikte een Siamese neurale netwerk, een paar identieke AI‑modellen die telkens twee retinabeelden inspecteren en leren te bepalen of ze waarschijnlijk bij dezelfde ziekte horen. Door duizenden afbeeldingsparen te vergelijken, bouwde het model een kaart van hoe nauw elf ziekten overeenkomen met milde diabetische retinopathie. Het ontdekte dat degeneratieve myopie, een aandoening waarbij de achterkant van het oog uitrekt en dunner wordt, retinabeelden opleverde die het sterkst correleerden met die vroege diabetische veranderingen. In menselijke termen werd degeneratieve myopie de "dichtstbijzijnde verwant" die het systeem kon leren waar het op moest letten.
Het systeem leren hoe kleine laesies eruitzien
Zodra een geschikte "leraar"‑ziekte was gevonden, was de volgende taak het laten zien aan de AI welke specifieke plekken op het netvlies het meest van belang zijn voor vroege diabetische schade. Met een tweede model, U‑Net genoemd, trainden de onderzoekers een segmentatiesysteem op gevestigde datasets waarin experts drie sleutelverschijnselen hadden aangeduid: kleine uitpuilingen in bloedvaten bekend als microaneurysma’s, kleine bloedingen en bleke cotton‑wool‑vlekken. Hoewel niet alle verschijnselen uniek zijn voor het milde stadium, schetsen ze samen een vroeg spoor van schade in de retinale circulatie. U‑Net leerde deze laesies in afbeeldingen te benadrukken, waardoor ruwe foto’s werden omgezet in gerichte kaarten waarop belangrijke waarschuwingssignalen opvallen terwijl minder relevante details vervagen.
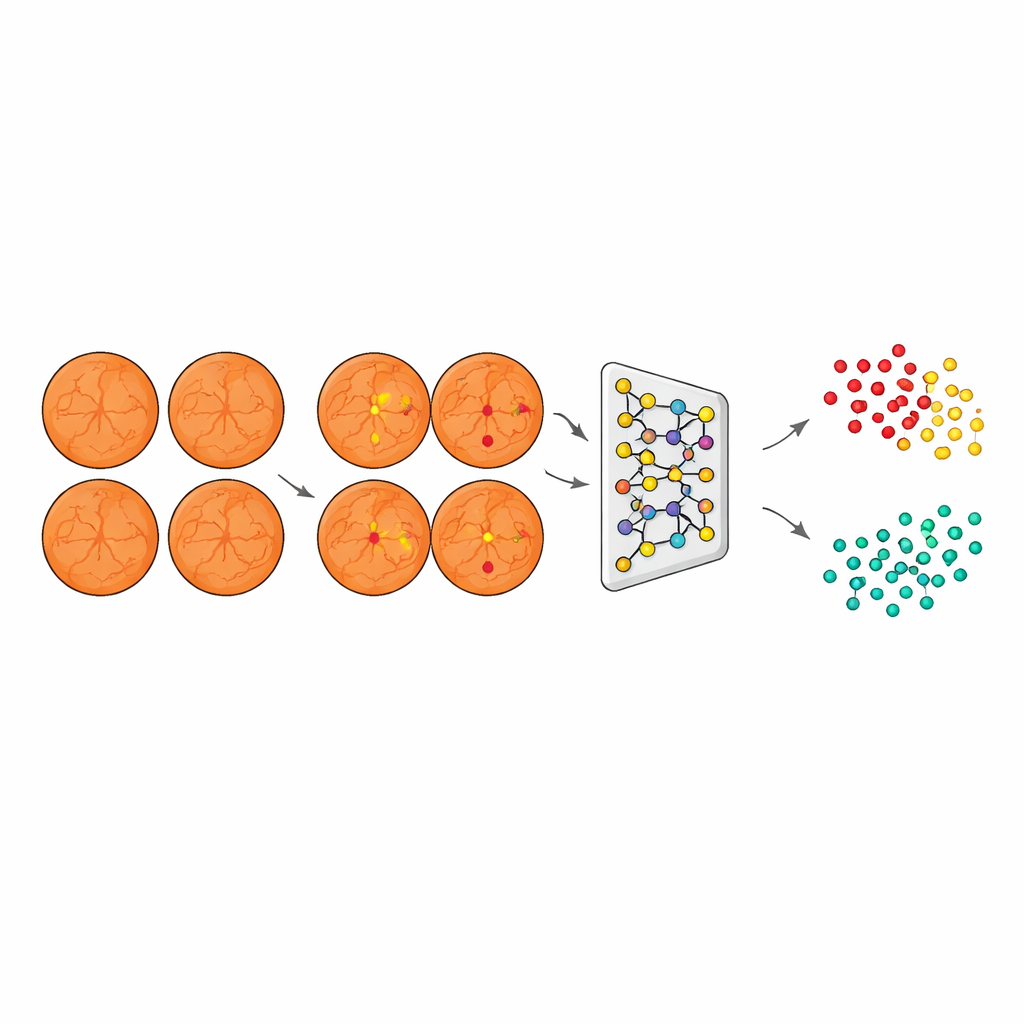
Ongeziene ziekte clusteren in gezond en niet‑gezond
Gewapend met dit laesie‑gerichte beeld, verwerkte het systeem vervolgens afbeeldingen van patiënten met degeneratieve myopie, maar met diabetische‑achtige laesies benadrukt en ziektespecifieke artefacten onderdrukt. Een derde model, gebaseerd op een ResNet‑netwerk gecombineerd met een agglomeratieve clusteringsalgoritme, zette deze gesegmenteerde afbeeldingen om in compacte numerieke beschrijvingen en groepeerde ze in twee natuurlijke clusters. Cruciaal is dat het algoritme dit deed zonder labels die aangaven welke ogen gezond of ziek waren; het organiseerde afbeeldingen gewoon op basis van gedeelde visuele patronen. Toen het team later deze clusters vergeleek met echte klinische labels op een onafhankelijke testset, kwam één cluster overeen met DR1 en de andere met niet‑zieke ogen, wat aantoont dat de AI effectief milde diabetische retinopathie zelf had "ontdekt".
Hoe goed de nieuwe aanpak presteert
Om te beoordelen of dit zero‑shot systeem praktisch nuttig was, vergeleken de onderzoekers het met meer conventionele "few‑shot" deep learning‑modellen die een klein aantal gelabelde voorbeelden mochten zien. Ze testten populaire architecturen zoals ResNet, VGG, MobileNet en AlexNet, allemaal getraind op beperkte hoeveelheden gelabelde data en vervolgens geëvalueerd op een externe dataset genaamd EyePACS. Het zero‑shot model, ondanks dat het tijdens de training nooit gelabelde DR1‑afbeeldingen te zien kreeg, behaalde een nauwkeurigheid van ongeveer 83% en een hoge area‑under‑the‑curve‑score, waarmee het de meeste van deze supervised concurrenten overtrof—vooral in precisie, wat betekent dat de ogen die het als ziek aangaf meestal daadwerkelijk risicovol waren. Ablatie‑experimenten, waarbij individuele componenten werden verwijderd, bevestigden dat zowel de stap voor ziekte‑vergelijkbaarheid als de stap voor laesie‑segmentatie essentieel waren voor deze sterke prestatie.
Wat dit betekent voor toekomstige oogzorg
In praktische termen laat dit werk zien dat een AI kan leren vroege diabetische oogschade te herkennen door "redeneren per analogie" van verwante aandoeningen en door experts gedefinieerde visuele aanwijzingen, in plaats van te vertrouwen op duizenden handmatig gelabelde voorbeelden van precies die aandoening. Dat kan een doorbraak betekenen voor screeningsprogramma’s in delen van de wereld waar deskundige labeling duur of schaars is, of voor recent geïdentificeerde oogaandoeningen die geen grote, gecureerde datasets hebben. Hoewel de methode nog uitdagingen kent—zoals uitbreiding naar andere beeldvormende technieken buiten fundusfoto’s en het transparanter maken van beslissingen voor artsen en patiënten—wijst het op een toekomst waarin machines clinici helpen subtiele oogaandoeningen eerder te herkennen, met veel minder gelabelde data dan moderne systemen nu vereisen.
Bronvermelding: Pan, C., Wang, Y., Jiang, Y. et al. A generalizable eye disease detection method based on Zero-Shot Learning. Commun Med 6, 249 (2026). https://doi.org/10.1038/s43856-026-01439-3
Trefwoorden: diabetische retinopathie, retina‑beeldvorming, zero‑shot learning, medische AI, screening van oogziekten