Clear Sky Science · de
Eine verallgemeinerbare Methode zur Erkennung von Augenerkrankungen basierend auf Zero‑Shot‑Learning
Warum frühe Warnzeichen am Auge wichtig sind
Viele ernsthafte Augenprobleme beginnen mit so feinen Veränderungen, dass selbst geschulte Spezialisten Schwierigkeiten haben können, sie zu erkennen. Eine leichte diabetische Retinopathie, eine frühe Komplikation bei Diabetes, ist ein solches stilles Warnzeichen: Wird sie früh erkannt, lässt sich Sehverlust verhindern, doch das erfordert eine sorgfältige Inspektion von Netzhautfotos und sehr viele fachkundig gelabelte Bilder, um heutige KI‑Systeme zu trainieren. Diese Studie stellt eine neue Art von KI vor, die lernen kann, frühe Erkrankungen zu erkennen, selbst wenn Ärztinnen und Ärzte niemals Beispiele genau dieser Erkrankung gelabelt haben — und öffnet damit möglicherweise den Weg zu schnelleren und kostengünstigeren Augenscreenings weltweit.
Eine neue Art, Maschinen ohne Antworten zu lehren
Die Forschenden bauen auf einem Konzept namens Zero‑Shot‑Learning auf, bei dem ein KI‑System etwas Neues erkennt, ohne zuvor gelabelte Beispiele gesehen zu haben. Anstatt Krankheitslabels auswendig zu lernen, ahmt das System nach, wie Klinikerinnen und Kliniker argumentieren: Es sucht nach verwandten Erkrankungen, die ähnliche visuelle Muster zeigen, und überträgt das Gelernte von ihnen. Hier konzentrierte sich das Team auf die leichte diabetische Retinopathie (DR1), trainierte seine Methode jedoch ohne ein einziges als DR1 gelabeltes Bild. Stattdessen stellten sie eine enorme Sammlung von Netzhautfotos zusammen, das LCFP‑14M‑Dataset, das mehr als eine Million Bilder und elf Augenerkrankungskategorien aus vielen öffentlichen Datenbanken integriert. Diese reichhaltige Bildmischung liefert die visuelle „Erfahrung“, aus der die KI Krankheitsmuster ableiten kann.
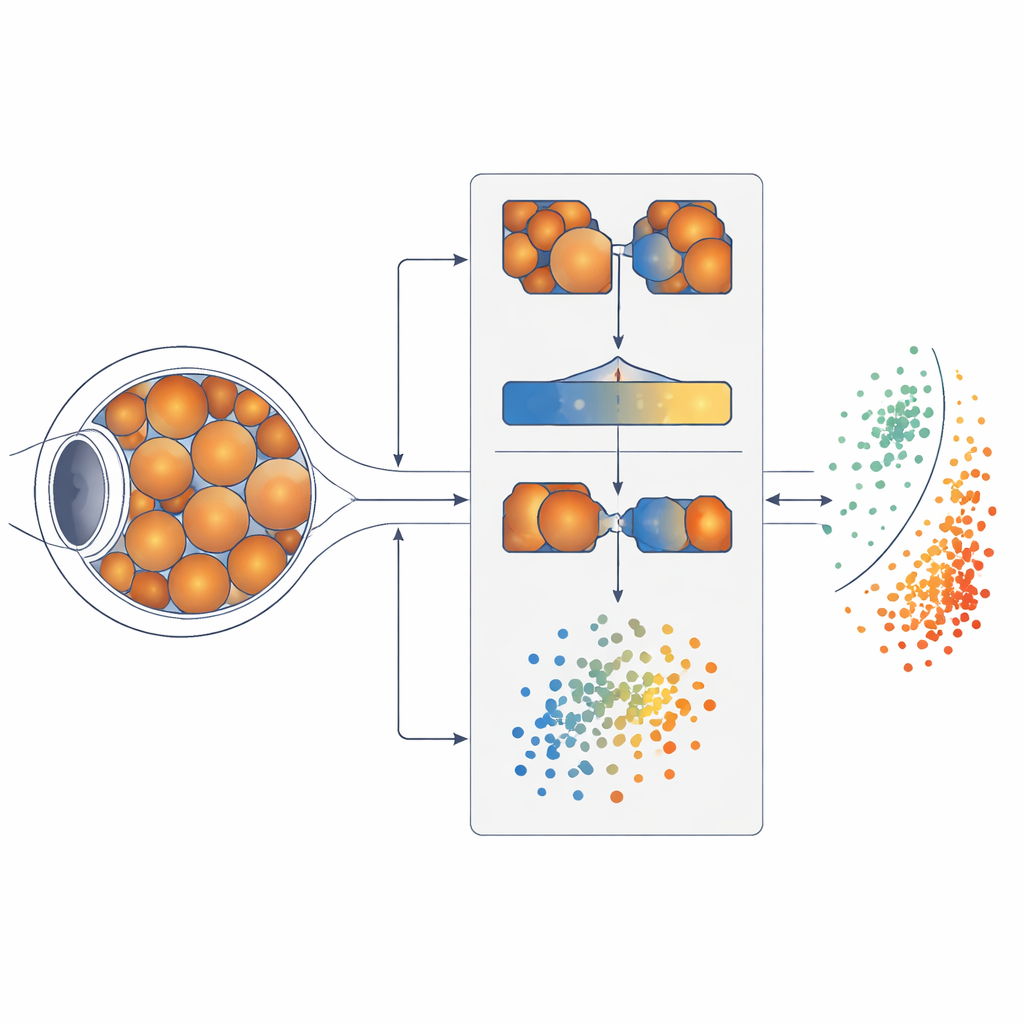
Ein ähnlich aussehende Erkrankung finden
Um herauszufinden, von wo Wissen übertragen werden kann, ist der erste Schritt des Systems, zu messen, wie ähnlich sich verschiedene Augenerkrankungen visuell sind. Das Team verwendete ein Siamese‑Neuronales Netzwerk, ein Paar identischer KI‑Modelle, die jeweils zwei Netzhautbilder gleichzeitig begutachten und lernen zu beurteilen, ob sie wahrscheinlich zur gleichen Erkrankung gehören. Durch den Vergleich tausender Bildpaare baute das Modell eine Karte auf, wie eng elf Erkrankungen mit der leichten diabetischen Retinopathie verwandt sind. Es entdeckte, dass degenerative Myopie — ein Zustand mit Dehnung und Ausdünnung des Augenhintergrunds — retinal am stärksten mit diesen frühen diabetischen Veränderungen korrelierte. In menschlichen Begriffen wurde die degenerative Myopie zum „nächsten Verwandten“, von dem das System lernen konnte, worauf es achten muss.
Dem System beibringen, wie winzige Läsionen aussehen
Nachdem eine geeignete „Lehrer“‑Erkrankung gefunden war, bestand die nächste Aufgabe darin, der KI zu zeigen, welche konkreten Stellen auf der Netzhaut für frühe diabetische Schäden am wichtigsten sind. Mit einem zweiten Modell namens U‑Net trainierten die Forschenden ein Segmentierungssystem an etablierten Datensätzen, in denen Expertinnen und Experten drei Hauptzeichen markiert hatten: winzige Aussackungen in Blutgefäßen, sogenannte Mikroaneurysmen, kleine Einblutungen und blasse Baumwollbüschel (cotton wool spots). Zwar sind nicht alle ausschließlich für das leichte Stadium, doch gemeinsam zeichnen sie eine frühe Spur von Schäden in der Netzhautdurchblutung. U‑Net lernte, genau diese Läsionen in Bildern hervorzuheben und verwandelte Rohfotografien in fokussierte Karten, auf denen wichtige Warnsignale hervortreten, während weniger relevante Details in den Hintergrund treten.
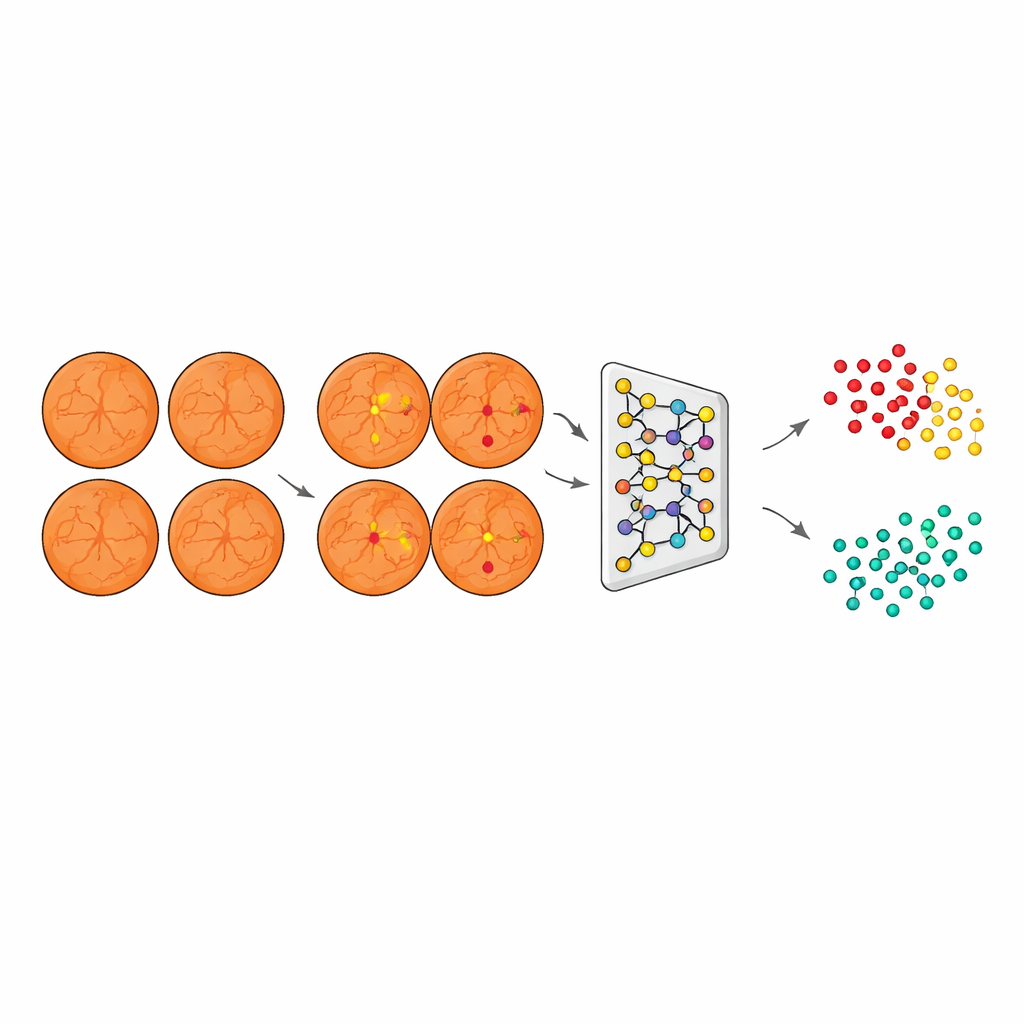
Unbekannte Erkrankungen in gesund und nicht‑gesund clustern
Ausgestattet mit dieser läsionszentrierten Sicht verarbeitete das System dann Bilder von Patientinnen und Patienten mit degenerativer Myopie, wobei diabetisch‑artige Läsionen betont und krankheitsspezifische Artefakte unterdrückt wurden. Ein drittes Modell, basierend auf einem ResNet‑Netzwerk kombiniert mit einem agglomerativen Clustering‑Algorithmus, wandelte diese segmentierten Bilder in kompakte numerische Beschreibungen um und gruppierte sie in zwei natürliche Cluster. Entscheidend ist, dass der Algorithmus dies ohne Labels tat, die angeben, welche Augen gesund oder erkrankt sind; er organisierte die Bilder allein nach gemeinsamen visuellen Mustern. Als das Team diese Cluster später mit echten klinischen Labels auf einem unabhängigen Testdatensatz verglich, entsprach ein Cluster DR1 und der andere nicht erkrankten Augen — ein Beleg dafür, dass die KI die leichte diabetische Retinopathie effektiv „entdeckt“ hatte.
Wie gut sich der neue Ansatz schlägt
Um zu beurteilen, ob dieses Zero‑Shot‑System praktisch nützlich ist, verglichen die Forschenden es mit konventionelleren Few‑Shot‑Deep‑Learning‑Modellen, denen eine kleine Anzahl gelabelter Beispiele gezeigt wurde. Sie testeten gängige Architekturen wie ResNet, VGG, MobileNet und AlexNet, alle auf begrenzte Mengen gelabelter Daten trainiert und anschließend auf einem externen Datensatz namens EyePACS evaluiert. Das Zero‑Shot‑Modell erreichte, obwohl es während des Trainings niemals gelabelte DR1‑Bilder gesehen hatte, eine Genauigkeit von etwa 83 % und einen hohen AUC‑Wert und übertraf die meisten dieser überwachten Konkurrenten — besonders in der Präzision, das heißt: Die Augen, die es als erkrankt einstufte, waren meist tatsächlich gefährdet. Ablations‑Experimente, bei denen einzelne Komponenten entfernt wurden, bestätigten, dass sowohl der Schritt der Krankheitsähnlichkeitsbestimmung als auch der der Läsionssegmentierung für diese starke Leistung essenziell waren.
Was das für die zukünftige Augenversorgung bedeutet
Praktisch betrachtet zeigt diese Arbeit, dass eine KI lernen kann, frühe diabetische Augenschäden zu erkennen, indem sie „durch Analogie“ von verwandten Erkrankungen und von Experten definierten visuellen Hinweisen schließt, anstatt sich auf Tausende hand‑gelabelter Beispiele der exakt gesuchten Erkrankung zu stützen. Das könnte Screening‑Programme in Regionen verändern, in denen fachkundige Label teuer oder selten sind, oder bei neu erkannten Augenerkrankungen ohne große kuratierte Datensätze. Zwar stehen noch Herausforderungen bevor — etwa die Erweiterung über Fundusfotos hinaus auf andere Bildgebungstechnologien und die größere Transparenz der Entscheidungen gegenüber Ärzten und Patientinnen/Patienten — doch die Studie weist in Richtung einer Zukunft, in der Maschinen Klinikerinnen und Kliniker unterstützen, subtile Augenerkrankungen früher zu erkennen und dabei deutlich weniger gelabelte Daten benötigen als heutige Systeme.
Zitation: Pan, C., Wang, Y., Jiang, Y. et al. A generalizable eye disease detection method based on Zero-Shot Learning. Commun Med 6, 249 (2026). https://doi.org/10.1038/s43856-026-01439-3
Schlüsselwörter: diabetische Retinopathie, Retina‑Bildgebung, Zero‑Shot‑Learning, medizinische KI, Augenerkrankungs‑Screening