Clear Sky Science · fr
Une méthode généralisable de détection des maladies oculaires basée sur l’apprentissage zéro‑exemple
Pourquoi les premiers signes oculaires sont essentiels
Beaucoup de problèmes oculaires graves commencent par des modifications si subtiles que même des spécialistes formés peuvent avoir du mal à les percevoir. La rétinopathie diabétique légère, une complication précoce du diabète, est un de ces signes silencieux : la détecter tôt peut prévenir la perte de vision, mais cela exige une inspection méticuleuse des photographies du fond d’œil et un très grand nombre d’images annotées par des experts pour entraîner les systèmes d’intelligence artificielle (IA) actuels. Cette étude présente un nouveau type d’IA capable d’apprendre à repérer une maladie précoce même lorsque les médecins n’ont jamais fourni d’exemples étiquetés de cette condition spécifique, ouvrant potentiellement la voie à un dépistage oculaire plus rapide et moins coûteux à l’échelle mondiale.
Une nouvelle façon d’enseigner aux machines sans réponses préalables
Les chercheurs s’appuient sur un concept appelé apprentissage zéro‑exemple (zero‑shot learning), où un système d’IA apprend à reconnaître quelque chose de nouveau sans avoir vu d’exemples étiquetés auparavant. Plutôt que de mémoriser des étiquettes de maladies, le système imite la façon dont raisonnent les cliniciens : il cherche des maladies apparentées qui partagent des motifs visuels et transfère ce qu’il apprend d’elles. Ici, l’équipe s’est concentrée sur la rétinopathie diabétique légère (DR1) mais a entraîné sa méthode sans une seule image DR1 étiquetée comme telle. À la place, elle a constitué une ressource massive de photographies rétiniennes, appelée jeu de données LCFP‑14M, intégrant plus d’un million d’images et onze catégories de maladies oculaires issues de nombreuses bases publiques. Ce mélange riche d’images fournit « l’expérience » visuelle à partir de laquelle l’IA peut inférer les motifs de la maladie.
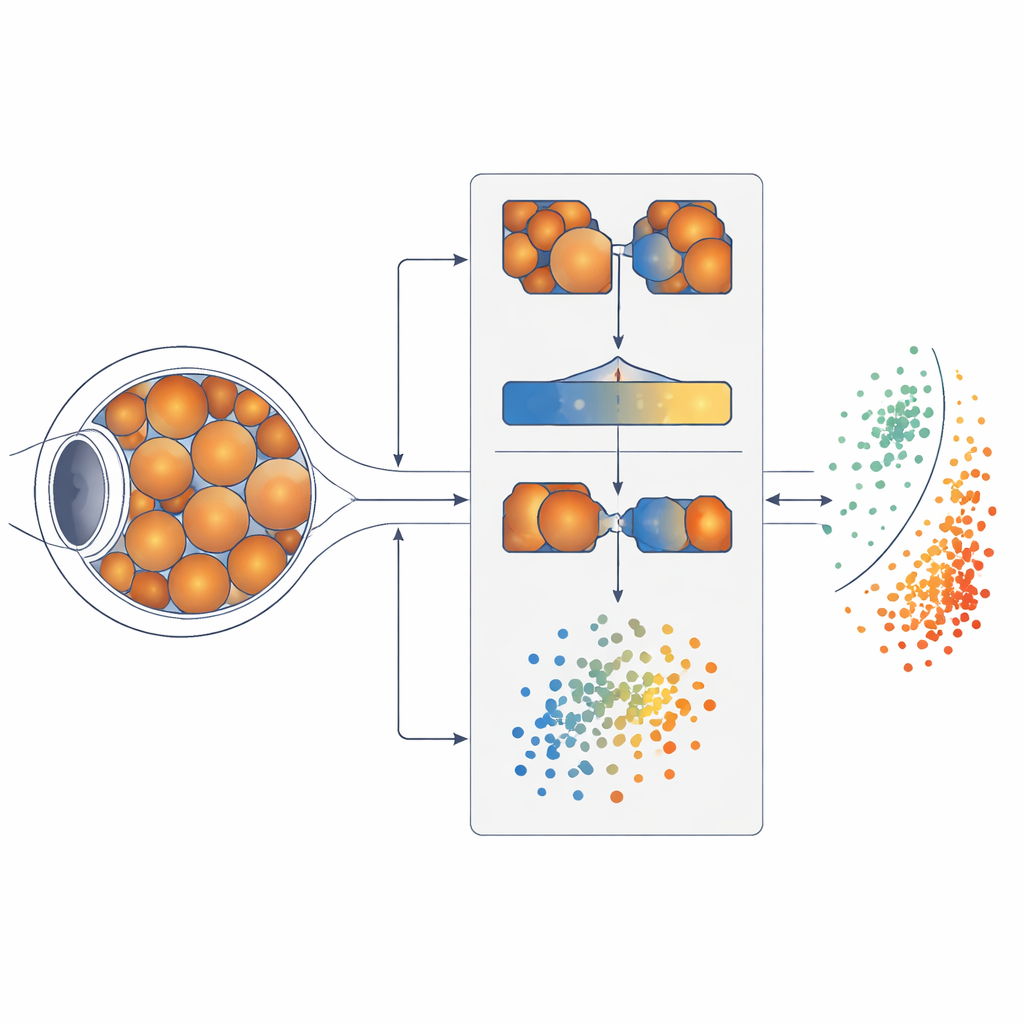
Identifier une maladie ressemblante
Pour déterminer où emprunter des connaissances, la première étape du système consiste à mesurer à quel point différentes maladies oculaires se ressemblent visuellement. L’équipe a utilisé un réseau neuronal siamois, une paire de modèles d’IA identiques qui inspectent deux images rétiniennes à la fois et apprennent à dire si elles appartiennent probablement à la même maladie. En comparant des milliers de paires d’images, le modèle a construit une cartographie de la proximité visuelle entre onze maladies et la rétinopathie diabétique légère. Il a découvert que la myopie dégénérative, une affection impliquant l’étirement et l’amincissement de l’arrière de l’œil, produisait des images rétiniennes les plus fortement corrélées avec ces premiers changements diabétiques. En termes humains, la myopie dégénérative est devenue la « cousine la plus proche » capable d’enseigner au système ce qu’il doit repérer.
Montrer au système à quoi ressemblent les petits lésions
Une fois une maladie « enseignante » appropriée identifiée, la tâche suivante était de montrer à l’IA quelles zones spécifiques de la rétine importent le plus pour les lésions diabétiques précoces. En utilisant un second modèle appelé U‑Net, les chercheurs ont entraîné un système de segmentation sur des jeux de données établis où des experts avaient marqué trois signes clés : de minuscules renflements des vaisseaux sanguins appelés microanévrismes, de petites hémorragies, et des taches cotonneuses pâles. Bien que tous ne soient pas uniques au stade léger, pris ensemble ils tracent une piste précoce de dommages dans la circulation rétinienne. U‑Net a appris à mettre en évidence ces lésions sur les images, transformant les photographies brutes en cartes ciblées où les signes d’alerte importants ressortent tandis que les détails moins pertinents s’estompent en arrière‑plan.
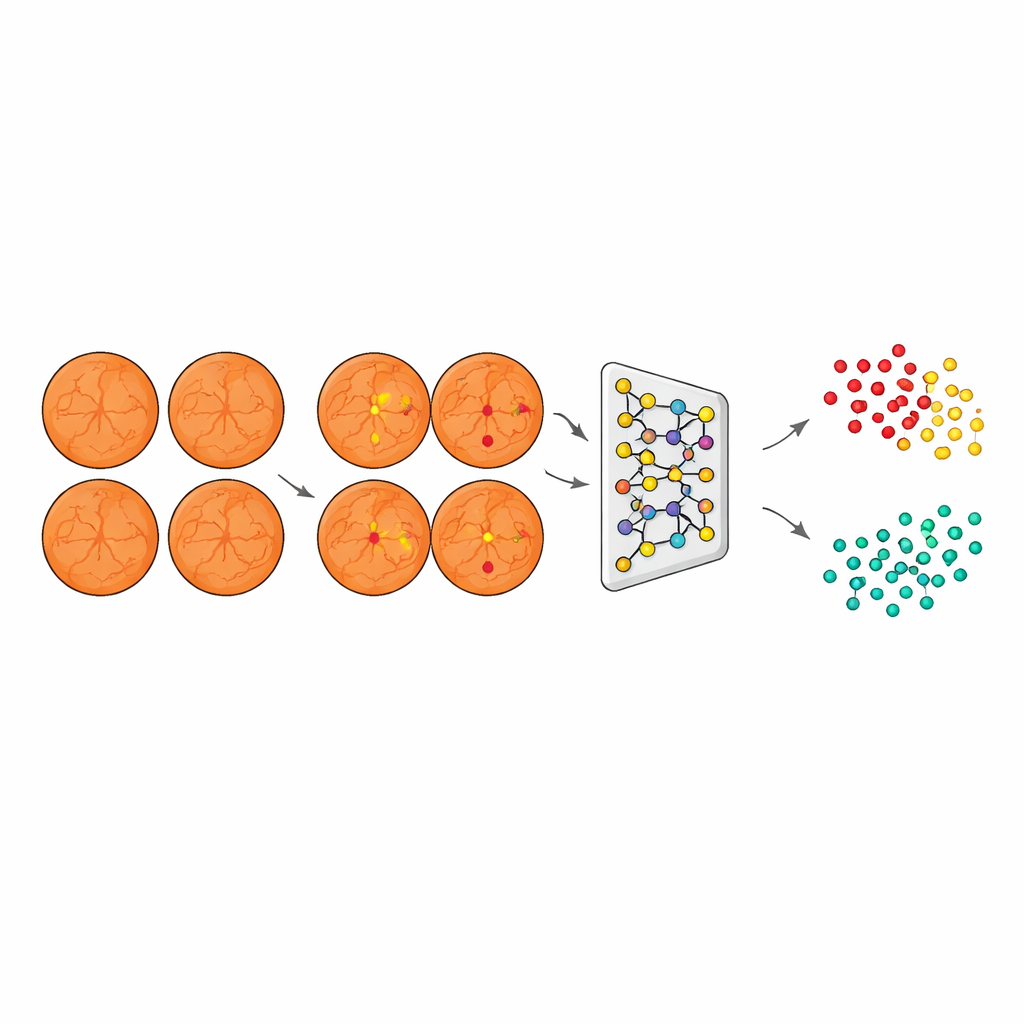
Regrouper une maladie jamais vue en sain et non‑sain
Armé de cette vue axée sur les lésions, le système a ensuite traité des images de patients atteints de myopie dégénérative, mais avec les lésions de type diabétique mises en évidence et les artefacts spécifiques à la maladie atténués. Un troisième modèle, basé sur un réseau ResNet combiné à un algorithme de regroupement agglomératif, a converti ces images segmentées en descriptions numériques compactes et les a regroupées en deux amas naturels. Crucialement, l’algorithme a fait cela sans aucune étiquette indiquant quels yeux étaient sains ou malades ; il a simplement organisé les images en fonction de motifs visuels partagés. Lorsque l’équipe a ensuite comparé ces amas aux étiquettes cliniques réelles sur un jeu de test indépendant, un amas s’est aligné avec la DR1 et l’autre avec des yeux non malades, montrant que l’IA avait effectivement « découvert » la rétinopathie diabétique légère par elle‑même.
Quelle est la performance de la nouvelle approche
Pour juger de l’utilité pratique de ce système zéro‑exemple, les chercheurs l’ont comparé à des modèles d’apprentissage profond « few‑shot » plus conventionnels auxquels on avait montré un petit nombre d’exemples étiquetés. Ils ont testé des architectures populaires telles que ResNet, VGG, MobileNet et AlexNet, toutes entraînées sur des quantités limitées de données étiquetées puis évaluées sur un jeu externe appelé EyePACS. Le modèle zéro‑exemple, malgré l’absence totale d’images DR1 étiquetées pendant l’entraînement, a atteint une précision d’environ 83 % et un score élevé de l’aire sous la courbe, surpassant la plupart de ces compétiteurs supervisés — en particulier en précision, c’est‑à‑dire que les yeux qu’il signalait comme malades étaient généralement réellement à risque. Des expériences d’ablation, où des composants individuels ont été retirés, ont confirmé que l’étape de similarité des maladies et l’étape de segmentation des lésions étaient toutes deux essentielles pour cette forte performance.
Ce que cela signifie pour les soins oculaires à venir
Concrètement, ce travail montre qu’une IA peut apprendre à repérer les premiers dommages diabétiques de l’œil en « raisonnant par analogie » à partir de maladies apparentées et d’indices visuels définis par des experts, plutôt que de dépendre de milliers d’exemples annotés manuellement de la condition précise d’intérêt. Cela pourrait changer la donne pour les programmes de dépistage dans les régions du monde où l’annotation experte est coûteuse ou rare, ou pour des maladies oculaires récemment identifiées qui manquent de grands jeux de données curationnés. Si la méthode doit encore relever des défis — comme s’étendre au‑delà des photos du fond d’œil vers d’autres technologies d’imagerie et rendre ses décisions plus transparentes pour les médecins et les patients — elle ouvre la voie à un avenir où les machines aident les cliniciens à détecter plus tôt des maladies oculaires subtiles, en utilisant beaucoup moins de données étiquetées que les systèmes actuels.
Citation: Pan, C., Wang, Y., Jiang, Y. et al. A generalizable eye disease detection method based on Zero-Shot Learning. Commun Med 6, 249 (2026). https://doi.org/10.1038/s43856-026-01439-3
Mots-clés: rétinopathie diabétique, imagerie rétinienne, apprentissage zéro‑exemple, IA médicale, dépistage des maladies oculaires