Clear Sky Science · nl
Reconstructie in real time van 3D-botmodellen met zeer laag-dosisprotocollen
Precisere chirurgie met zachtere beeldvorming
Elk jaar ondergaan tientallen miljoenen mensen orthopedische ingrepen aan botten en gewrichten. Chirurgen vertrouwen steeds vaker op op maat gemaakte 3D-modellen van het bot van een patiënt om operaties te plannen en nauwkeurige sneden te begeleiden, maar tegenwoordig vereisen die modellen meestal een logge CT-scanner, hoge stralingsdoses en uren werk van specialisten. Deze studie introduceert een snellere, zachtere methode: met slechts twee laagdosisröntgenfoto’s en kunstmatige intelligentie een gedetailleerd 3D-beeld van de knie reconstrueren in ongeveer een halve minuut, wat hoogwaardige planning en begeleiding mogelijk kan maken in meer operatiekamers en voor meer patiënten.
Waarom huidige botscans tekortschieten
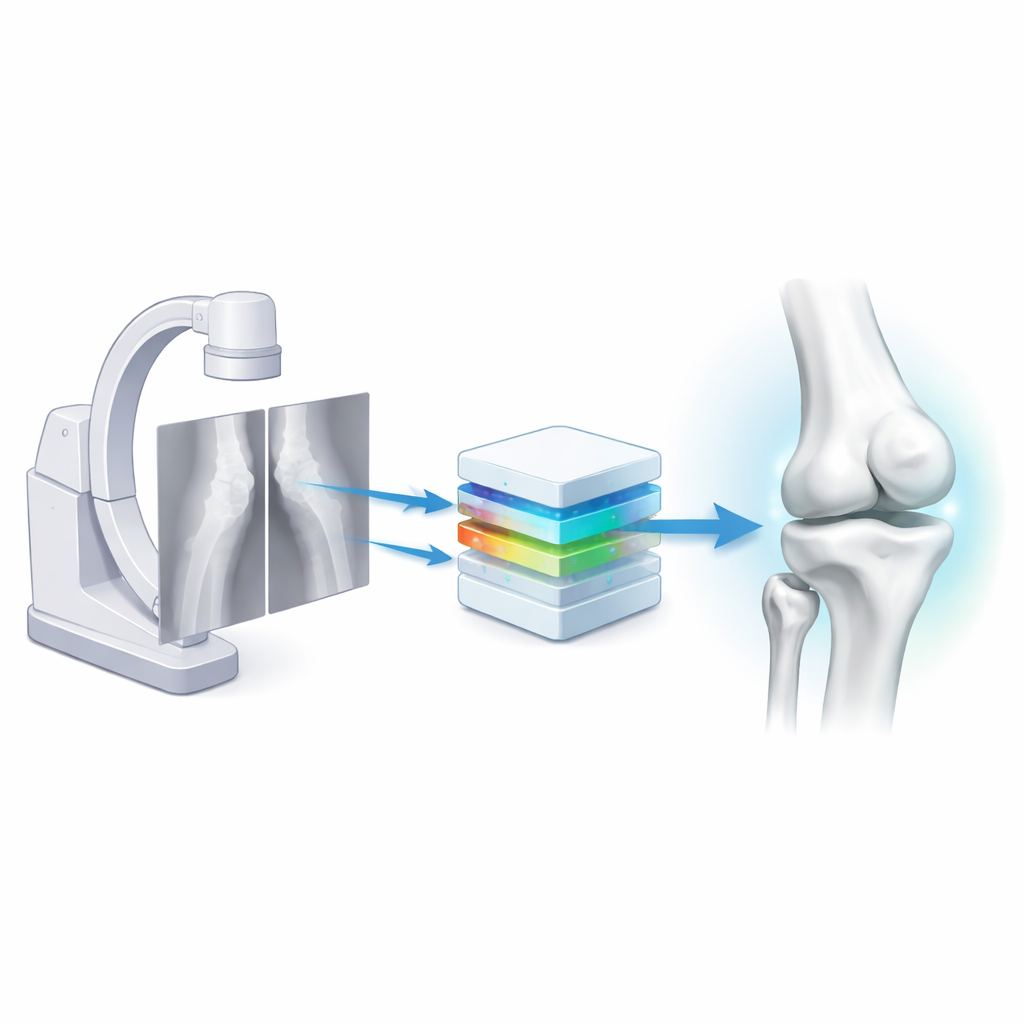
Traditionele 3D-botmodellen beginnen met een CT-scan, die honderden röntgenplakjes maakt die computers samenvoegen tot een volledig volume. Hoewel krachtig, kent deze aanpak drie grote nadelen. Ten eerste zet het patiënten bloot aan relatief veel straling, wat een serieus probleem is voor kinderen, zwangere vrouwen en iedereen die herhaaldelijk gescand moet worden. Ten tweede zijn CT-machines groot, duur en lastig in drukke operatiekamers te plaatsen; het opzetten tijdens een ingreep kan 20–30 minuten duren en het personeel verstoren. Ten derde besteden experts, nadat de scan klaar is, vaak nog uren aan het uitschetsen van de contour van elk bot in gespecialiseerde software om een bruikbaar 3D-model te bouwen. Al met al maakt dat CT-gebaseerde modellen uitstekend voor geselecteerde gevallen, maar onpraktisch voor gebruik in real time midden in een operatie.
Twee simpele röntgenfoto’s omzetten in een volledige 3D-knie
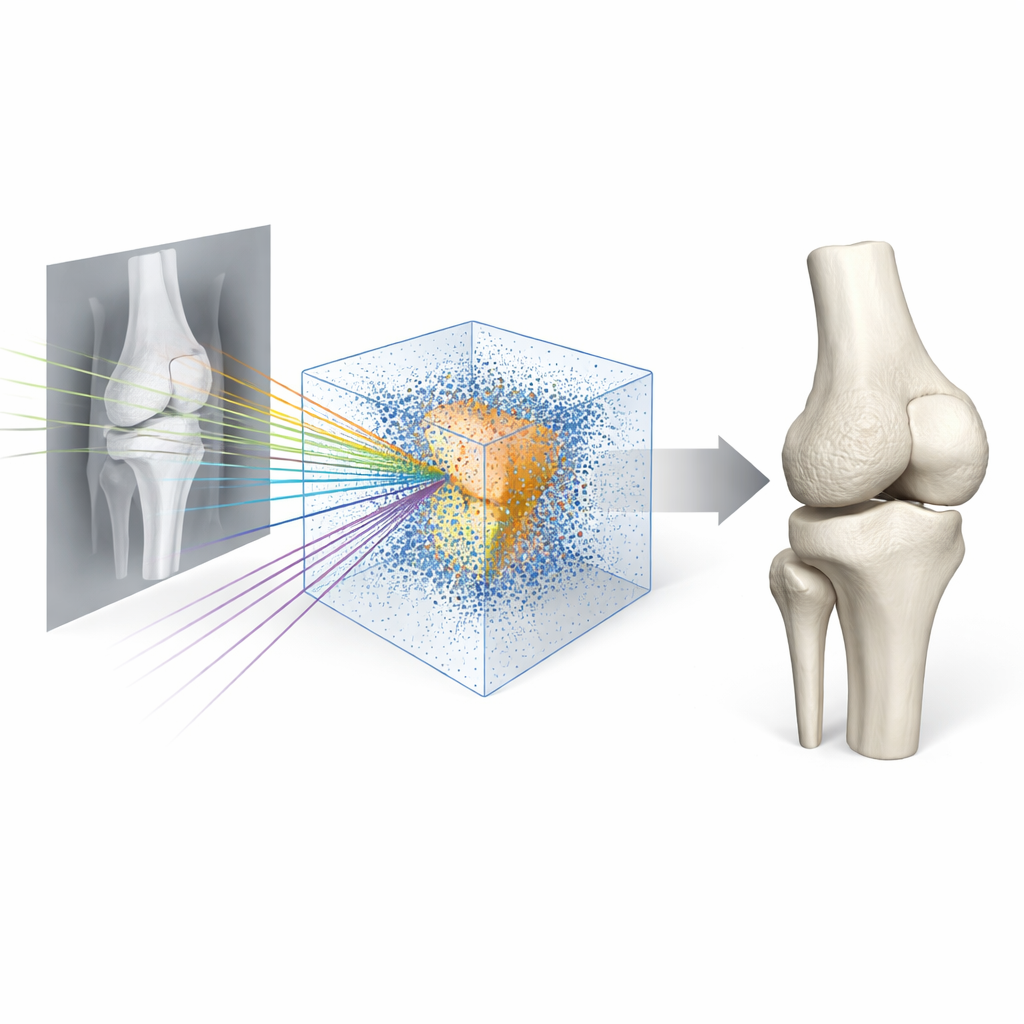
De onderzoekers wilden deze trage keten vervangen door een wendbare opzet gebaseerd op biplanaire röntgenfoto’s — twee standaardaanzichten van de knie onder rechte hoeken, gemaakt met gebruikelijke fluoroscopieapparatuur zoals een C-arm. Ze bouwden een deep-learningsysteem dat Semi-Supervised Reconstruction with Knowledge Distillation (SSR-KD) heet. In plaats van direct een zichtbare oppervlakte te voorspellen, leert het systeem een “occupancy field”: voor elk punt in de 3D-ruimte schat het of dat punt binnen of buiten elk van de vier belangrijkste knieënbotten ligt — het femur, tibia, fibula en de patella. Nadat het netwerk dit onzichtbare 3D-grid heeft gevuld met binnen–buiten-beslissingen, zet een standaardgrafisch algoritme het veld om in vloeiende 3D-botoppervlakken. Op moderne hardware duurt het hele proces — van het binnenkrijgen van de twee röntgenfoto’s tot het produceren van vier gedetailleerde botmodellen — ongeveer 25 seconden.
De AI leren met beperkte experturen
Hoge-kwaliteits trainingsdata vormen doorgaans de bottleneck voor medische AI. Hier kostte het handmatig omlijnen van de botten van één been in CT-experts ongeveer vier uur, dus dat voor honderden gevallen doen was onrealistisch. Het team verzamelde in plaats daarvan 605 knieën met CT-scans, maar labelde zorgvuldig slechts 120 daarvan en gebruikte de rest als ongelabelde ondersteuning. Ze trainden eerst een netwerk om botten direct uit CT-scans te reconstrueren, een taak die gemakkelijker is omdat de 3D-informatie volledig aanwezig is. Dat CT-gebaseerde model diende vervolgens als leraar: voor ongelabelde gevallen produceerde het ‘pseudo’-3D-botinformatie die het X-ray-gebaseerde studentennetwerk begeleidde. Door dit crossmodale onderricht te combineren met een semi-gesuperviseerd trainingsschema leerde de student onzichtbare 3D-structuur uit slechts twee aanzichten af te leiden, en presteerde goed zelfs wanneer slechts enkele tientallen gevallen door experts waren gelabeld.
Hoe goed de nieuwe modellen overeenkomen met de werkelijkheid
Om te beoordelen of deze snelle reconstructies goed genoeg zijn voor echte chirurgie, evalueerde het team ze op meerdere manieren. Ten opzichte van door experts gemaakte CT-modellen was de gemiddelde oppervlaktefout van SSR-KD minder dan één millimeter, waarbij de grote femur en tibia vaak binnen 0,8 millimeter zaten — vergelijkbaar met de inwendige resolutie van de CT-scans zelf. Een panel van tien orthopedische experts en medische ingenieurs beoordeelde 3D-knieën afkomstig van ofwel CT ofwel de twee-röntgenmethode, zonder te weten welke welke was, en beoordeelde vorm, fijne details en klinische bruikbaarheid. De scores waren in wezen niet van elkaar te onderscheiden, en experts vonden over het algemeen dat de AI-gebaseerde modellen geschikt waren voor het plannen van complexe botsneden. In een meer praktische test voerden chirurgen gesimuleerde high tibial osteotomieën uit op 3D-geprinte botten, met behulp van op maat gemaakte zaagmallen die waren ontworpen op basis van ofwel CT-gebaseerde ofwel AI-reconstrueerde botten. Mallen gebaseerd op de nieuwe methode kostten niet meer tijd in gebruik en behaalden vergelijkbare scores voor pasvorm, stabiliteit en nauwkeurigheid.
Beperkingen, uitdagingen en toekomstige toepassingen
De aanpak is niet foutloos. Kleinere botten zoals de knieschijf en de fibula, die in de röntgenaanzichten verborgen kunnen liggen, vertoonden iets grotere fouten. Zeer complexe gevallen, zoals knieën met grote metalen implantaten die de anatomie vervormen, blijven uitdagend, en de huidige studie leunde sterk op gesimuleerde röntgenfoto’s afgeleid van CT in plaats van op grote aantallen echte klinische beelden. Desondanks bleek de methode robuust over verschillende ziekenhuizen en behield ze klinisch nuttige nauwkeurigheid zelfs wanneer de twee röntgenaanzichten minder dan een rechte hoek van elkaar maakten — een realistische beperking in de operatiekamer. hetzelfde raamwerk zou mogelijk kunnen worden aangepast aan andere gewrichten met relatief eenvoudige vormen, zoals de elleboog, hoewel meer complexe gebieden met veel kleine botjes waarschijnlijk verdere vooruitgang vereisen.
Wat dit voor patiënten kan betekenen
Simpel gezegd toont dit werk aan dat een computer kan leren een 3D-knie te ‘zien’ vanuit slechts twee snelle, laagdosis röntgenfoto’s, goed genoeg om precieze chirurgische planning en maatgidsen te ondersteunen die vroeger een volledige CT-scan en uren experts vergden. Als dit gevalideerd wordt op grote sets echte klinische röntgenfoto’s en verder wordt uitgebreid dan de knie, zou dergelijke technologie de stralingsbelasting kunnen verlagen, kosten kunnen besparen en gepersonaliseerde 3D-botmodellen naar meer ziekenhuizen kunnen brengen — ook naar instellingen zonder geavanceerde scanners — waardoor zorgvuldige, beeldgestuurde botchirurgie breder beschikbaar wordt.
Bronvermelding: Lin, Y., Sun, H., Li, Y. et al. Real-time reconstruction of 3D bone models via very-low-dose protocols. npj Digit. Med. 9, 353 (2026). https://doi.org/10.1038/s41746-026-02389-9
Trefwoorden: orthopedische chirurgie, 3D-botmodellen, laagdosis röntgen, medische AI, kniebeeldvorming