Clear Sky Science · nl
Nucleair eiwit 1 is een regelaar van celdood in primaire humane luchtwegepitheelcellen en verminderd bij idiopathische longfibrose
Waarom deze longstudie ertoe doet
Idiopathische longfibrose is een dodelijke longziekte waarbij littekenweefsel de longen geleidelijk verstijft en elke ademhaling zwaarder maakt. Veel patiënten hebben een verleden van roken, maar wetenschappers worstelen nog met het begrijpen hoe rook en kwetsbare luchtwegcellen samenwerken om de long te beschadigen. Deze studie bekijkt nauwkeurig een weinig bekend stress-eiwit binnen luchtwegcellen, met de vraag of het die cellen helpt schade te overleven en of het verlies ervan de longen kwetsbaarder kan maken bij mensen met fibrose.
De voorste verdedigingslinie van de long
De luchtwegen zijn bekleed door een dun, druk bezet blad van cellen dat zowel als schild als schoonmaakploeg fungeert. Sommige cellen dragen trilhaartjes die slijm en stof uit de longen vegen, terwijl andere slijm afscheiden of schade repareren. Omdat sigarettenrook het eerste is wat deze cellen tegenkomen, gebruikten de auteurs volledig gerijpte humane luchtwegcellen gekweekt in het laboratorium om te zien hoe ze reageren op langdurige rookblootstelling. Ze maten duizenden eiwitten in de cellen en gebruikten computertools om te ontdekken welke stressroutes samen veranderden, in de hoop nieuwe spelers in rookgerelateerd letsel te vinden.
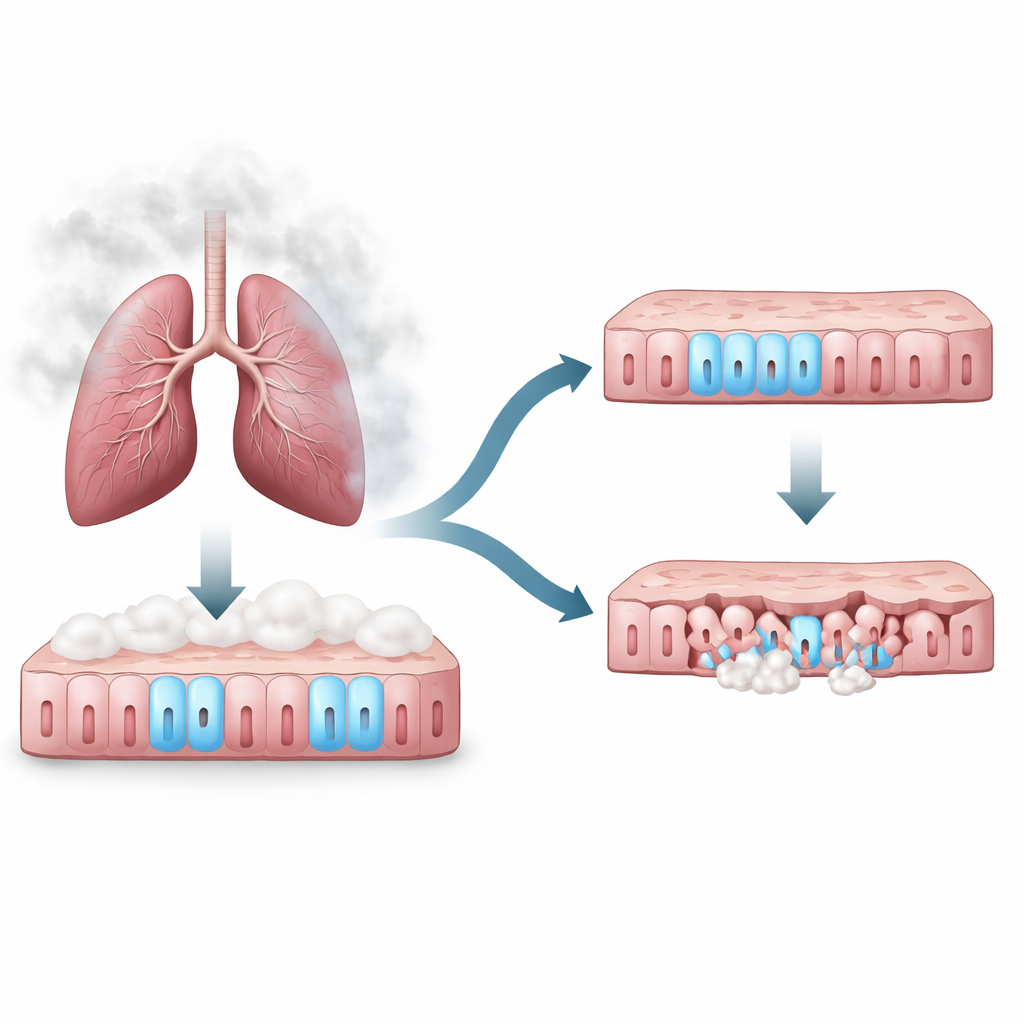
Een stress-eiwit dat stilletjes beschermt
Het eiwit dat eruit sprong was nucleair eiwit 1, of NUPR1, een stressresponsfactor die eerder vooral in verband werd gebracht met kanker en alvleesklierziekten. Analyse met computers suggereerde dat rook NUPR1 zou inschakelen, waarmee luchtwegcellen zouden helpen omgaan met schade. Maar toen het team dit direct controleerde, vonden ze dat sigarettenrook NUPR1-niveaus niet betrouwbaar verhoogde of de locatie binnen de cel niet veranderde. In plaats daarvan toonden experimenten met een medicijn dat voorkomt dat NUPR1 de kern binnengaat aan dat het eiwit zelf sterk beschermend is. Wanneer NUPR1 werd geblokkeerd, stierven meer luchtwegcellen en begon de normaal strakke barrière ertussen te lekken en uiteen te vallen, zelfs zonder rook.
Hoe cellen sterven als de bescherming wegvalt
Celdood kan via verschillende wegen verlopen, en eerder werk had gesuggereerd dat verlies van NUPR1 een speciale vorm van ijzergemedieerde schade, ferroptose genoemd, zou kunnen triggeren. Om dit te testen maten de onderzoekers genen en markers verbonden aan ferroptose, evenals algemene oxidatieve schade, in luchtwegcellen behandeld met de NUPR1-blokker. Hoewel sommige gensignalen versprongen, was er geen overtuigend teken van de kenmerkende lipidedeschade die ferroptose definieert. In plaats daarvan stegen eiwitten geassocieerd met klassieke geprogrammeerde celdood, en daalde het aandeel levende cellen. Deze bevindingen wijzen erop dat NUPR1 voornamelijk fungeert als een schild tegen apoptose in luchtwegcellen, waardoor ze stress doorstaan zonder direct zelfvernietigend te reageren.
Kwetsbare luchtwegen in gefibrotiseerde longen
Het team richtte zich vervolgens op longweefsel en cellen van mensen met idiopathische longfibrose. Single-cell data en fluorescentiekleuring van patiëntlongen toonden dat NUPR1-niveaus in het algemeen lager waren, ook in cellen van het luchtwegepitheel, en leken vooral verminderd bij huidige rokers. Toen de wetenschappers luchtwegcellen van mensen met fibrose kweekten, vormden die kweekjes een epitheel met minder gekiliaerde cellen en meer slijmproducerende cellen dan kweekjes van controledonoren, wat de veranderingen weerspiegelt die in zieke longen worden gezien. Opvallend was dat deze uit fibrose afkomstige cellen gevoeliger waren voor NUPR1-blokkade: ze verloren barrièrefunctie en stierven bij lagere medicijndoses, wat suggereert dat ze sterk afhankelijk zijn van de resterende NUPR1-bescherming.
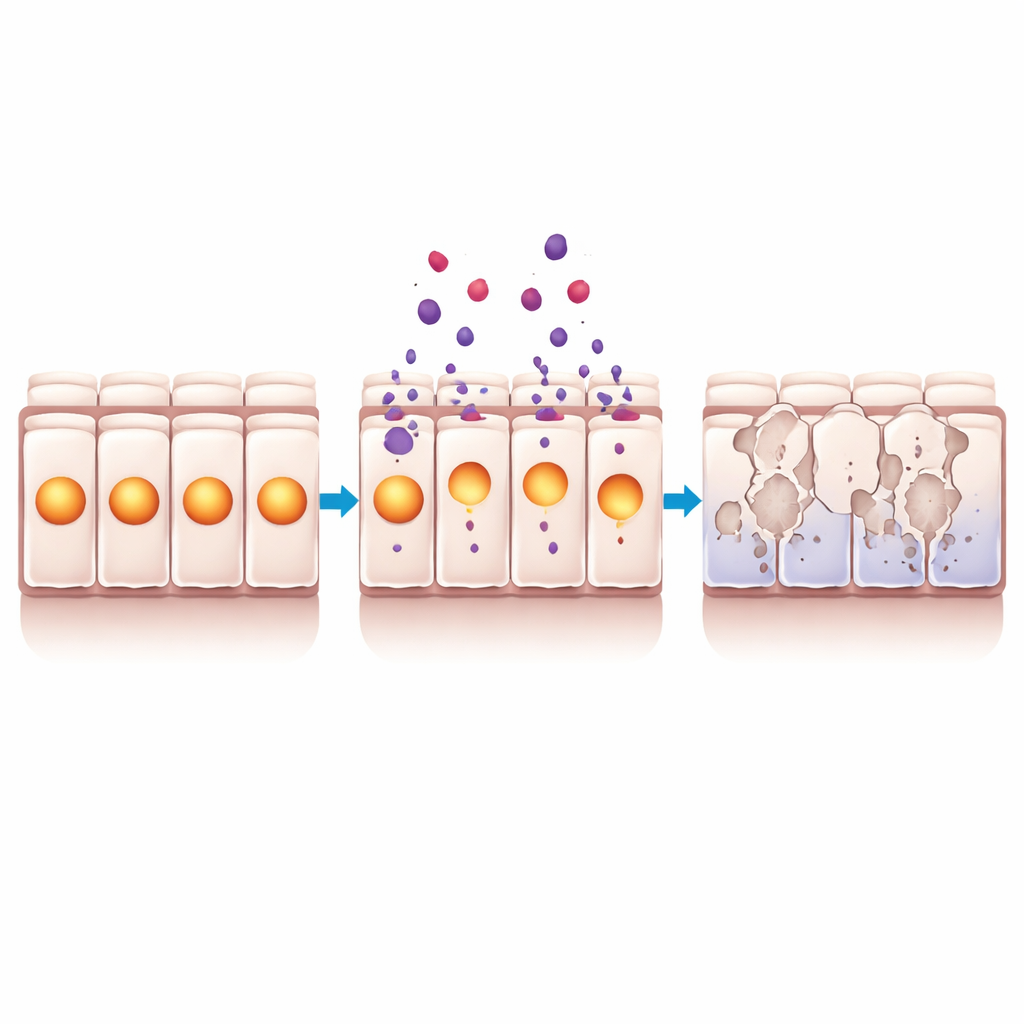
Wat dit betekent voor toekomstige zorg
Kort gezegd suggereert deze studie dat NUPR1 fungeert als een ingebouwd overlevingsfactor die luchtwegcellen helpt in leven te blijven en het longoppervlak afgesloten te houden. Sigarettenrook verhoogde deze beschermingsmechanismen niet duidelijk in in het laboratorium gekweekte cellen, maar patiëntgegevens wezen erop dat langdurig roken en fibrose gekoppeld zijn aan lagere NUPR1-niveaus in de long. Het verlies van die bescherming kan luchtwegcellen in gefibrotiseerde longen kwetsbaarder maken voor schade en sneller laten afsterven, wat de cyclus van littekenvorming kan voeden. De resultaten geven ook een waarschuwingssignaal voor kankermedicijnen die proberen NUPR1 uit te schakelen: hoewel die aanpak tumoren kan verzwakken, zou ze ook reeds gestreste luchtwegcellen kunnen schaden, vooral bij mensen met onderliggende longfibrose.
Bronvermelding: Zöller, M., Mastalerz, M., Dick, E. et al. Nuclear protein 1 is a cell death regulator in primary human airway epithelial cells and reduced in idiopathic pulmonary fibrosis. Sci Rep 16, 14728 (2026). https://doi.org/10.1038/s41598-026-51510-1
Trefwoorden: idiopathische longfibrose, luchtwegepitheel, sigarettenrook, celdood, NUPR1