Clear Sky Science · nl
EneA van Aspergillus fumigatus is een regelaar van secundaire stofwisseling en versterkt nscA‑expressie in aanwezigheid van polyenen en Streptomyces
Waarom deze schimmel en haar trucs ertoe doen
Aspergillus fumigatus is een veelvoorkomende schimmel die in bodem en composthopen voorkomt, maar bij mensen met een verzwakt immuunsysteem kan ze levensbedreigende longinfecties veroorzaken. Artsen vertrouwen op krachtige antischimmelmiddelen, toch is deze microbe opmerkelijk goed in staat te overleven zowel in de natuur als in patiënten. Deze studie onthult hoe een enkele schimmelschakelaar, EneA genoemd, het mos kan helpen antibiotische moleculen in de bodem en geneesmiddelen in de kliniek waar te nemen, en vervolgens te reageren door chemische afweerstoffen te produceren die het beschermen tegen geneesmiddelen, concurrerende bacteriën en zelfs het menselijk immuunsysteem.
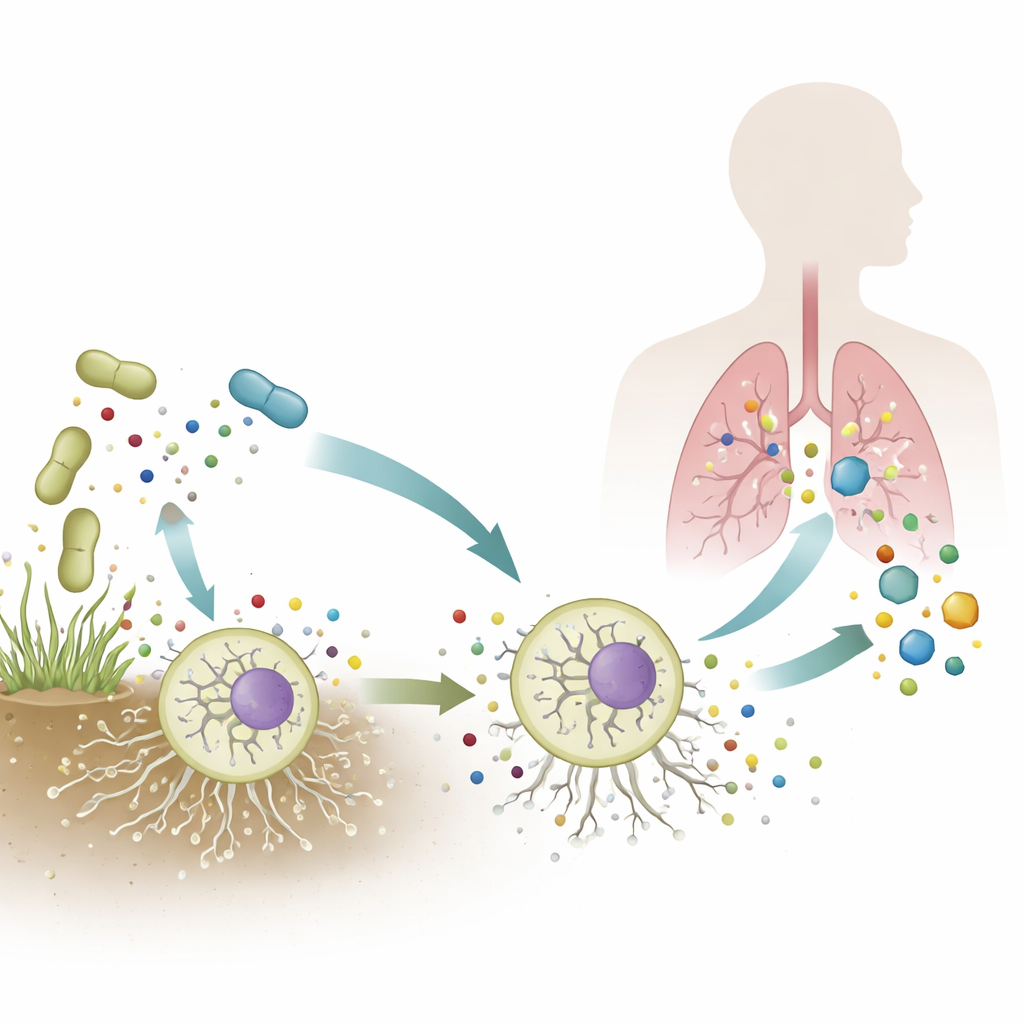
Een verborgen schakelaar in een gevaarlijke schimmel
De onderzoekers richtten zich op EneA, een lid van een grote familie schimmelregulatoren die groepen genen aan- of uitzetten. In A. fumigatus zijn veel van deze genen bestemd voor “secundaire metabolieten” – kleine moleculen die niet essentieel zijn voor basale groei maar fungeren als toxines, signalen of bescherming. Toen EneA kunstmatig werd verhoogd, veranderde de schimmel haar genetische activiteit drastisch: honderden genen werden actiever, waaronder bijna honderd betrokken bij secundaire stofwisseling verspreid over minstens negen verschillende gencluster. Verschillende van deze clusters produceren bekende toxines, en één, het neosartoricin/fumicycline‑cluster, maakt een molecule die menselijke immuunreacties kan dempen.
Hoe geneesmiddelen en buren uit de bodem het systeem wekken
Het team vroeg vervolgens wat EneA natuurlijk activeert. Ze keken naar polyenen, een klasse antischimmelmoleculen waartoe het ziekenhuismedicijn amfotericine B behoort en het bodemantibioticum nystatine dat door Streptomyces‑bacteriën wordt gemaakt. Wanneer de schimmel aan deze polyenen werd blootgesteld, groeide ze slecht als EneA ontbrak, wat aantoont dat EneA nodig is voor aanpassing aan deze geneesmiddelfamilie. Tegelijkertijd verhoogden polyenen de activiteit van een sleutelgen, nscA, dat de productie van neosartoricin start. Deze verhoging was afhankelijk van EneA: zonder EneA reageerde nscA nauwelijks. Intrigerend was dat wanneer de schimmel werd gekweekt met vloeistof uit Streptomyces noursei‑culturen, zowel EneA als nscA opnieuw werden geactiveerd, hoewel nystatine zelf niet langer detecteerbaar was. Dit suggereert dat de schimmel andere bacteriële metabolieten kan waarnemen als vroeg waarschuwingssignaal en zijn chemische verdediging kan inschakelen voordat polyenen verschijnen.
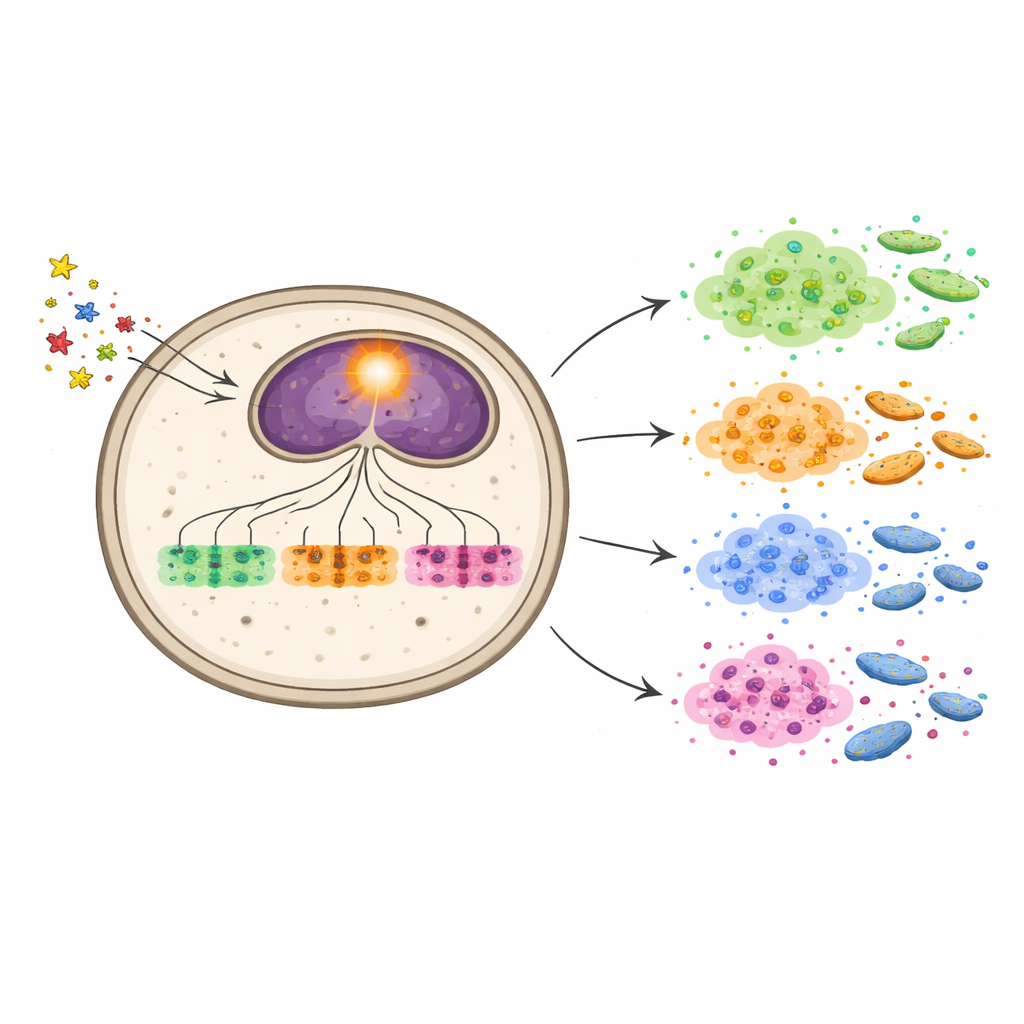
Twee routes naar hetzelfde chemische wapen
In de schimmel wordt nscA gewoonlijk gecontroleerd door een andere regulatorische eiwit, NscR, dat naast nscA in het neosartoricin‑gencluster ligt. De auteurs ontleedden hoe EneA en NscR samenwerken. Onder normale blootstelling aan geneesmiddelen verhoogt amfotericine B de activiteit van EneA, wat op zijn beurt NscR vereist om nscA en de rest van het cluster volledig te activeren. Echter, wanneer EneA op zeer hoge niveaus werd geforceerd, kon de schimmel nscA inschakelen zelfs als NscR was verwijderd. Dit onthult twee verschillende circuits: een polyeen‑responsief pad dat zowel EneA als NscR nodig heeft, en een EneA‑overdrivepad dat NscR omzeilt. De schimmel kan dus haar respons herschakelen afhankelijk van hoe sterk EneA wordt tot expressie gebracht, wat haar flexibiliteit geeft om met verschillende stressfactoren in de bodem of in de gastheer om te gaan.
Schimmelchemie die geneesmiddelen en concurrenten neutraliseert
Zijn deze door EneA gecontroleerde chemicaliën daadwerkelijk van belang voor overleving? Om dit te onderzoeken, extraheerden de wetenschappers metabolieten uit een stam die EneA overproduceerde en uit een normale stam. Metabolieten van de EneA‑verhoogde schimmel vertraagden in laboratoriumtesten sterk de groei van S. noursei, terwijl extracten van de normale stam weinig effect hadden. Dezelfde EneA‑afhankelijke extracten verminderden ook de schade die amfotericine B toebracht aan A. fumigatus, waardoor de schimmel beter kon groeien in aanwezigheid van het geneesmiddel. Verrassend genoeg maakte het verwijderen van nscA de schimmel niet gevoeliger voor amfotericine B, zelfs niet wanneer EneA overgeëxprimeerd was. Dit betekent dat andere metabolieten, die samen met neosartoricin werden geïnduceerd, voornamelijk verantwoordelijk zijn voor het afzwakken van de toxiciteit van het geneesmiddel, terwijl neosartoricin waarschijnlijk een grotere rol speelt bij het ondermijnen van de afweer van de gastheer.
Wat dit betekent voor patiënten en het milieu
Al met al positioneert de studie EneA als een centraal schakelpunt dat omgevingssignalen van bodembacteriën en medische antischimmelbehandelingen koppelt aan een brede chemische respons in A. fumigatus. Door meerdere metabolietclusters tegelijk aan te zetten, helpt EneA de schimmel om bacteriële concurrenten af te weren, polyeen‑geneesmiddelen zoals amfotericine B te neutraliseren en mogelijk de immuunverdediging van geïnfecteerde patiënten te verzwakken. In praktische zin suggereert dit werk dat langdurige polyeentherapie onbedoeld het chemische arsenaal van de schimmel kan versterken. Het gericht aanpakken van EneA zelf, of het netwerk van metabolieten dat het reguleert, kan daarom nieuwe manieren bieden om deze opportunistische pathogeen onder controle te houden.
Bronvermelding: Bunz, O., Gerke, J., Bader, O. et al. EneA of Aspergillus fumigatus is a regulator of secondary metabolism and enhances nscA expression in presence of polyenes and Streptomyces. Sci Rep 16, 12038 (2026). https://doi.org/10.1038/s41598-026-47215-0
Trefwoorden: Aspergillus fumigatus, antischimmelresistentie, secundaire metabolieten, interacties met Streptomyces, amfotericine B