Clear Sky Science · de
EneA von Aspergillus fumigatus ist ein Regulator der Sekundärstoffwechselwege und verstärkt die nscA‑Expression in Anwesenheit von Polyenen und Streptomyces
Warum dieser Pilz und seine Strategien wichtig sind
Aspergillus fumigatus ist ein häufiger Schimmelpilz, der in Boden und Komposthaufen vorkommt; bei Menschen mit geschwächtem Immunsystem kann er jedoch lebensbedrohliche Lungeninfektionen verursachen. Ärztinnen und Ärzte sind auf potente Antimykotika angewiesen, trotzdem ist dieses Mikrobenwesen überraschend widerstandsfähig — sowohl in der Umwelt als auch im Patienten. Diese Studie zeigt, wie ein einziger pilzlicher Schaltregler, EneA genannt, dem Schimmel hilft, antibiotische Moleküle im Boden und Medikamente in der Klinik wahrzunehmen und darauf zu reagieren, indem er chemische Abwehrstoffe produziert, die ihn vor Medikamenten, konkurrierenden Bakterien und sogar dem menschlichen Immunsystem schützen.
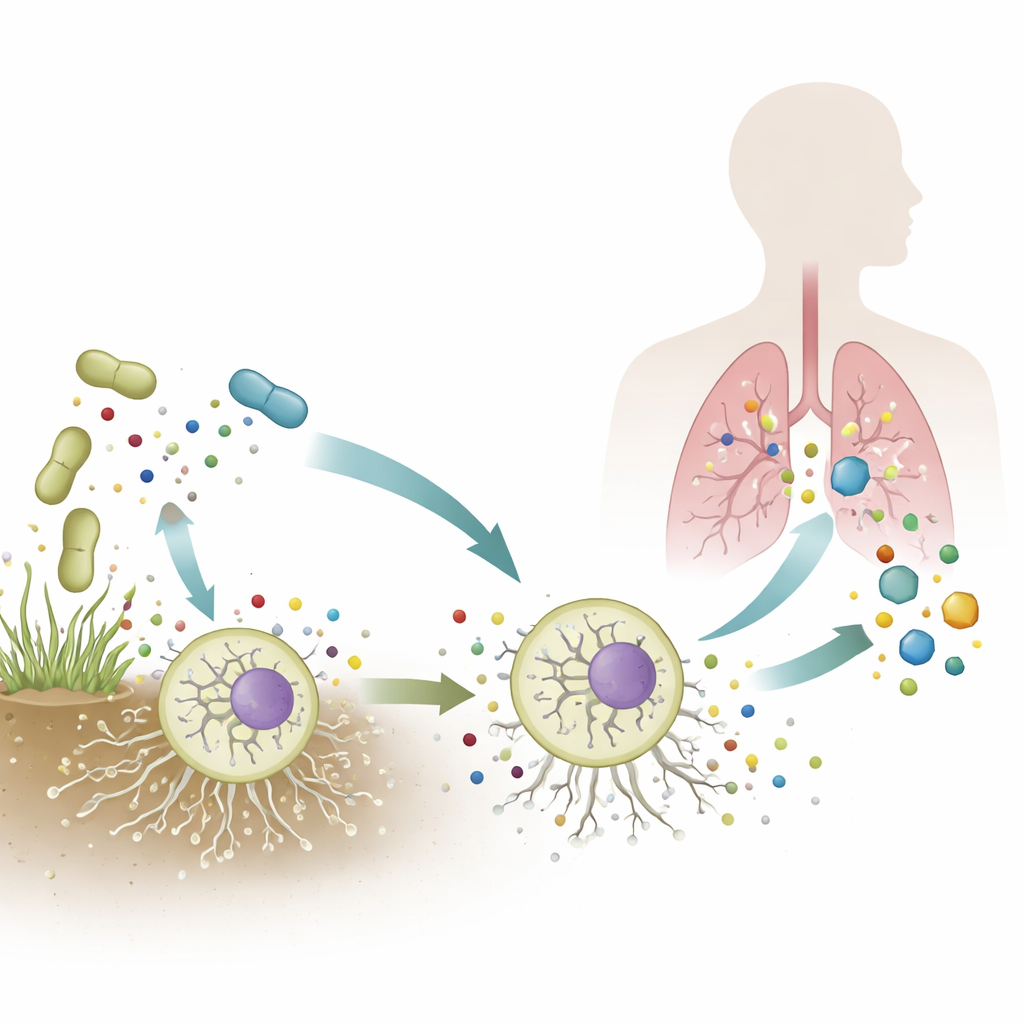
Ein versteckter Schalter in einem gefährlichen Schimmelpilz
Die Forschenden konzentrierten sich auf EneA, ein Mitglied einer großen Familie von pilzlichen Regulatoren, die Gencluster an- oder ausschalten. Bei A. fumigatus sind viele dieser Gene auf „Sekundärmetabolite“ ausgerichtet – kleine Moleküle, die für das Grundwachstum nicht essenziell sind, aber als Toxine, Signalstoffe oder Schutzmechanismen dienen. Als EneA künstlich hochreguliert wurde, veränderte der Pilz seine Genaktivität drastisch: Hunderte Gene wurden aktiver, darunter fast hundert Gene, die am Sekundärstoffwechsel beteiligt sind und sich auf mindestens neun verschiedene Gencluster verteilen. Mehrere dieser Cluster produzieren bekannte Toxine, und eines, das Neosartoricin/Fumicyclin‑Cluster, synthetisiert ein Molekül, das menschliche Immunantworten dämpfen kann.
Wie Medikamente und Boden‑Nachbarn das System wecken
Als Nächstes fragten die Wissenschaftlerinnen und Wissenschaftler, was EneA natürlich aktiviert. Sie untersuchten Polyene, eine Klasse von Antimykotika, zu der das Krankenhausmedikament Amphotericin B sowie das vom Bodenbakterium Streptomyces produzierte Nystatin gehören. Wurde der Pilz diesen Polyenen ausgesetzt, wuchs er schlecht, wenn EneA fehlte, was zeigt, dass EneA für die Anpassung an diese Wirkstofffamilie erforderlich ist. Gleichzeitig steigerten Polyene die Aktivität eines Schlüsselsgens, nscA, das die Neosartoricin‑Produktion startet. Diese Verstärkung hing von EneA ab: ohne EneA reagierte nscA kaum. Interessanterweise wurden EneA und nscA wieder aktiviert, wenn der Pilz mit dem Kulturüberstand von Streptomyces noursei kultiviert wurde, obwohl Nystatin selbst nicht mehr nachweisbar war. Das legt nahe, dass der Schimmel andere bakterielle Metaboliten als Frühwarnsignal wahrnehmen kann und seine chemische Abwehr hochfährt, noch bevor Polyene tatsächlich auftreten.
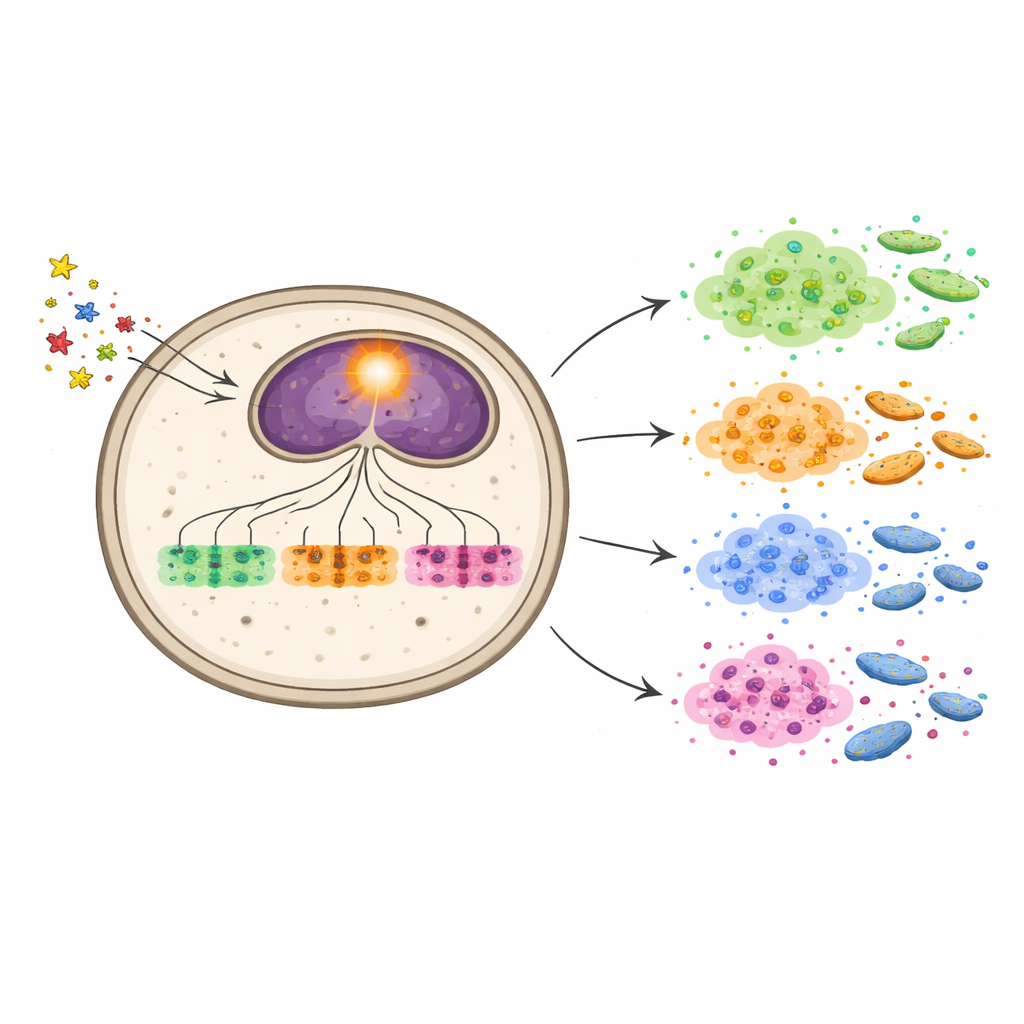
Zwei Wege zu derselben chemischen Waffe
Im Pilz wird nscA normalerweise von einem anderen regulatorischen Protein, NscR, kontrolliert, das neben ihm im Neosartoricin‑Gencluster liegt. Die Autorinnen und Autoren untersuchten, wie EneA und NscR zusammenwirken. Unter normaler Medikamentenexposition erhöht Amphotericin B die EneA‑Aktivität, die wiederum NscR benötigt, um nscA und den Rest des Clusters vollständig zu aktivieren. Wenn EneA jedoch auf sehr hohe Werte gezwungen wurde, konnte der Pilz nscA auch dann einschalten, wenn NscR gelöscht war. Das zeigt zwei unterschiedliche Schaltkreise: einen polyen‑reaktiven Pfad, der sowohl EneA als auch NscR benötigt, und einen EneA‑Übersteuerungs‑Pfad, der NscR umgeht. Der Pilz kann seine Antwort also je nach Stärke der EneA‑Expression umverdrahten und sich so flexibel an verschiedene Stressfaktoren im Boden oder im Wirt anpassen.
Pilzliche Chemie, die Medikamente und Rivalen entschärft
Spielen diese von EneA gesteuerten Chemikalien tatsächlich eine Rolle fürs Überleben? Um das zu klären, extrahierten die Forschenden Metabolite aus einem Stamm mit überproduziertem EneA und aus einem normalen Stamm. Metabolite aus dem EneA‑verstärkten Pilz hemmten in Labortests deutlich das Wachstum von S. noursei, während Extrakte aus dem normalen Stamm kaum Wirkung zeigten. Dieselben EneA‑abhängigen Extrakte verringerten außerdem den Schaden, den Amphotericin B an A. fumigatus anrichtet, sodass der Pilz in Gegenwart des Medikaments besser wachsen konnte. Überraschenderweise machte die Deletion von nscA den Pilz nicht empfindlicher gegenüber Amphotericin B, selbst wenn EneA überexprimiert war. Das bedeutet, dass andere Metabolite, die parallel zu Neosartoricin induziert werden, hauptsächlich dafür verantwortlich sind, die Toxizität des Medikaments abzuschwächen, während Neosartoricin wahrscheinlich eher eine Rolle bei der Schwächung der Immunantwort des Wirts spielt.
Was das für Patienten und die Umwelt bedeutet
Insgesamt stellt die Studie EneA als zentralen Schalter dar, der Umweltsignale von Bodenbakterien und medizinische Antimykotika mit einer breiten chemischen Antwort in A. fumigatus verknüpft. Durch gleichzeitiges Einschalten mehrerer Metabolit‑Cluster hilft EneA dem Schimmel, bakterielle Konkurrenz abzuwehren, Polyen‑Medikamente wie Amphotericin B zu neutralisieren und möglicherweise die Immunabwehr infizierter Patienten zu schwächen. Praktisch gesehen legt diese Arbeit nahe, dass eine längerfristige Polyen‑Therapie unbeabsichtigt das chemische Arsenal des Pilzes stärken könnte. Die gezielte Beeinflussung von EneA selbst oder des Netzwerks von Metaboliten, das es kontrolliert, könnte daher neue Ansätze bieten, um diesen opportunistischen Erreger in Schach zu halten.
Zitation: Bunz, O., Gerke, J., Bader, O. et al. EneA of Aspergillus fumigatus is a regulator of secondary metabolism and enhances nscA expression in presence of polyenes and Streptomyces. Sci Rep 16, 12038 (2026). https://doi.org/10.1038/s41598-026-47215-0
Schlüsselwörter: Aspergillus fumigatus, Antimykotika‑Resistenz, Sekundärmetabolite, Interaktionen mit Streptomyces, Amphotericin B