Clear Sky Science · nl
Lidocaïne remt proliferatie, migratie en invasie van hepatocellulaire carcinoomcellen via downregulatie van SLC6A3
Waarom een verdovingsmiddel ertoe doet bij leverkanker
Lidocaïne is vooral bekend als de verdovingsinjectie die je bij de tandarts krijgt of vóór kleine operaties. Deze studie suggereert echter dat hetzelfde middel stilletjes kan bijdragen aan de bestrijding van een van de dodelijkste kankers wereldwijd: hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker. Door te onderzoeken hoe lidocaïne op moleculair niveau met leverkankercellen interageert, onthullen de onderzoekers een verrassend nieuw doelwit dat mogelijk benut kan worden om tumorgroei en -uitzaaiing te vertragen.
Een nadere blik op de uitdaging van leverkanker
Leverkanker behoort tot de meest voorkomende en dodelijke kankersoorten wereldwijd, en veel patiënten worden pas gediagnosticeerd als de ziekte al vergevorderd is. Zelfs met moderne middelen die het immuunsysteem stimuleren, blijft de lange-termijnoverleving voor de meeste mensen met vergevorderd hepatocellulair carcinoom slecht. Omdat lidocaïne al veel wordt gebruikt en over het algemeen veilig is, kan het begrip of het ook als anticancermiddel werkt de deur openen naar verbeterde behandeling zonder een volledig nieuw geneesmiddel te hoeven ontwikkelen.
Op zoek naar lidocaïne's verborgen doelwitten
Het team combineerde twee sterke benaderingen om in kaart te brengen hoe lidocaïne leverkankercellen beïnvloedt. Eerst gebruikten ze "network pharmacology"-databases om honderden menselijke eiwitten te voorspellen waaraan lidocaïne mogelijk kan binden. Vervolgens behandelden ze leverkankercellen (een lijn genaamd HepG2) met lidocaïne en voerden transcriptomische sequencing uit, waarmee wordt gemeten welke genen op- of neergezet worden. Door deze twee lijsten te overlappen, brachten ze meer dan 400 voorspelde doelwitten en meer dan 400 veranderde genen terug tot slechts negen sleutel-kandidaten die zowel op lidocaïne reageren als waarschijnlijk direct ermee interageren.
Een dopaminetransporter in de schijnwerpers
Onder de negen kandidaten stak er één bovenuit: een gen genaamd SLC6A3, dat codeert voor een transporter die normaal gesproken zenuwcellen helpt het hersenchemische dopamine opnieuw op te nemen. In datasets van leverkankerpatiënten waren hogere niveaus van SLC6A3 en een ander gen, TERT, gekoppeld aan slechtere overleving, waarbij SLC6A3 de sterkste associatie liet zien. De onderzoekers gebruikten vervolgens computerdocking om te modelleren hoe lidocaïne fysiek aan deze eiwitten zou kunnen binden en vonden dat lidocaïne een stabiele, voornamelijk hydrofobe interactie met SLC6A3 vormt. Wanneer ze hun celexperimenten nog eens bekeken, bleek dat behandeling met lidocaïne duidelijk de SLC6A3-niveaus in de kankercellen verminderde.
Wat er gebeurt wanneer de cruciale schakel wordt gedimd
Om te testen of SLC6A3 meer is dan een voorbijganger, manipuleerden de wetenschappers de niveaus ervan rechtstreeks in leverkankercellen. Wanneer ze de cellen dwongen SLC6A3 te verminderen, werden de cellen minder levensvatbaar, vatbaarder voor geprogrammeerde celdood en veel minder in staat tot migratie en invasie—twee gedragingen die ten grondslag liggen aan tumoruitzaaiing. Overexpressie van SLC6A3 had het tegenovergestelde effect: het bevorderde groei en invasiviteit en beschermde cellen tegen dood. De studie koppelde SLC6A3 ook aan patronen van infiltratie van immuuncellen in levertumoren en aan routes gerelateerd aan dopamineregulatie en een type dodelijke celstress genaamd ferroptose, wat suggereert dat deze transporter op het kruispunt van metabolisme, signaalvorming en immuniteit in leverkanker staat.
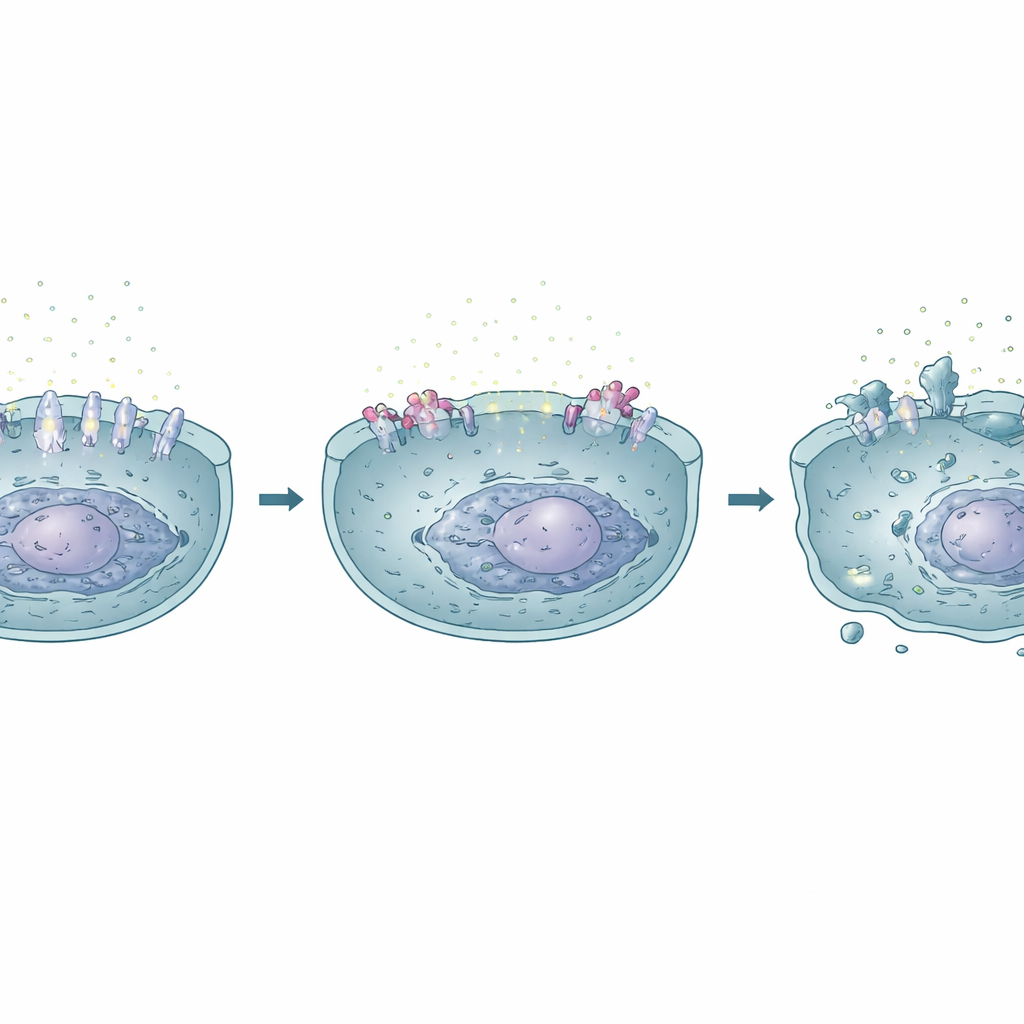
Meer dan één gen: een breder netwerk van veranderingen
Hoewel SLC6A3 naar voren kwam als de centrale speler, gaat de invloed van lidocaïne verder. Het middel wijzigde meerdere andere genen met bekende rollen in kanker en cellulaire lotsbepaling. Het verlaagde de expressie van TERT, een component die kankercellen helpt hun chromosoomuiteinden te onderhouden en zich onbeperkt te delen, en verhoogde de niveaus van ALOX12, een enzym dat gekoppeld is aan ferroptose en tumorsuppressie. Samen ondersteunen deze verschuivingen het beeld dat lidocaïne leverkankercellen zachtjes richting zelfvernietiging duwt en de tumoromgeving minder gastvrij maakt voor agressieve groei en verspreiding.
Wat dit betekent voor patiënten en toekomstige zorg
In eenvoudige bewoordingen suggereert deze studie dat lidocaïne meer kan doen dan pijn verdoven—het kan leverkankercellen direct verzwakken door een dopaminetransporter, SLC6A3, omlaag te schakelen en cellen richting celdood te duwen terwijl hun vermogen om te migreren en te infiltreren wordt beperkt. Omdat lidocaïne al in veel leverkankerprocedures wordt gebruikt, roepen deze bevindingen de mogelijkheid op dat het optimaliseren van timing en toediening de uitkomsten kan verbeteren zonder volledig nieuwe geneesmiddelen toe te voegen. Toch is het werk tot dusver grotendeels uitgevoerd in celmodellen en via computervaardigheden; het bevestigen van deze effecten in diermodellen en klinische proeven zal essentieel zijn voordat lidocaïne doelbewust kan worden hergebruikt als een gerichte bondgenoot tegen leverkanker.
Bronvermelding: Li, P., Tong, W., He, H. et al. Lidocaine inhibits hepatocellular carcinoma cell proliferation, migration, and invasion through the downregulation of SLC6A3. Sci Rep 16, 11678 (2026). https://doi.org/10.1038/s41598-026-46688-3
Trefwoorden: leverkanker, lidocaïne, dopaminetransporter, tumormicro-omgeving, ferroptose