Clear Sky Science · fr
La lidocaïne inhibe la prolifération, la migration et l'invasion des cellules du carcinome hépatocellulaire en réprimant SLC6A3
Pourquoi un anesthésique local importe pour le cancer du foie
La lidocaïne est surtout connue comme l’injection anesthésique que l’on reçoit chez le dentiste ou avant des interventions mineures. Mais cette étude suggère que le même médicament pourrait discrètement contribuer à lutter contre l’un des cancers les plus mortels au monde : le carcinome hépatocellulaire, la forme la plus courante de cancer du foie. En examinant comment la lidocaïne interagit avec les cellules cancéreuses hépatiques au niveau moléculaire, les chercheurs dévoilent une cible inattendue qui pourrait être exploitée pour ralentir la croissance et la dissémination tumorales.
Un regard plus précis sur le défi posé par le cancer du foie
Le cancer du foie figure parmi les cancers les plus fréquents et les plus mortels à l’échelle mondiale, et de nombreux patients ne sont diagnostiqués que lorsque la maladie est déjà avancée. Même avec les médicaments modernes qui stimulent le système immunitaire, la survie à long terme demeure faible pour la plupart des personnes atteintes d’un carcinome hépatocellulaire avancé. Comme la lidocaïne est déjà largement utilisée et généralement sûre, déterminer si elle peut aussi agir comme agent anticancéreux pourrait ouvrir la voie à l’amélioration des traitements sans avoir à inventer un médicament entièrement nouveau.
À la recherche des cibles cachées de la lidocaïne
L’équipe a combiné deux approches puissantes pour cartographier l’effet de la lidocaïne sur les cellules de cancer du foie. D’abord, elle a utilisé des bases de données de « pharmacologie en réseau » pour prédire des centaines de protéines humaines auxquelles la lidocaïne pourrait se lier. Ensuite, les chercheurs ont traité des cellules de carcinome hépatocellulaire (une lignée appelée HepG2) avec de la lidocaïne et réalisé un séquençage transcriptomique, qui mesure quels gènes sont activés ou réprimés. En recoupant ces deux listes, ils ont réduit plus de 400 cibles prédictes et plus de 400 gènes altérés à seulement neuf candidats clés qui répondent à la lidocaïne et sont susceptibles d’interagir directement avec elle.
Mettre en lumière un transporteur de dopamine dans le cancer
Parmi les neuf candidats, un a émergé : un gène nommé SLC6A3, qui code pour un transporteur aidant normalement les neurones à récupérer le neurotransmetteur dopamine. Dans des jeux de données de patients atteints d’un cancer du foie, des niveaux plus élevés de SLC6A3 et d’un autre gène, TERT, étaient associés à une survie plus mauvaise, SLC6A3 affichant l’association la plus forte. Les chercheurs ont ensuite utilisé un docking informatique pour modéliser la liaison potentielle de la lidocaïne à ces protéines et ont constaté que la lidocaïne forme une interaction stable, principalement hydrophobe, avec SLC6A3. Lorsqu’ils ont examiné leurs expériences cellulaires, le traitement par la lidocaïne faisait clairement diminuer les niveaux de SLC6A3 dans les cellules cancéreuses.
Que se passe-t-il lorsque l’interrupteur clé est abaissé
Pour tester si SLC6A3 est plus qu’un simple passager, les scientifiques ont manipulé directement son expression dans des cellules de cancer du foie. Lorsque l’on a forcé la diminution de SLC6A3, les cellules perdaient en viabilité, devenaient plus susceptibles d’entrer en mort cellulaire programmée et étaient beaucoup moins capables de migrer et d’envahir — deux comportements à l’origine de la dissémination tumorale. La surexpression de SLC6A3 avait l’effet inverse, renforçant la croissance et l’invasivité tout en protégeant les cellules de la mort. L’étude a également relié SLC6A3 à des schémas d’infiltration des cellules immunitaires dans les tumeurs hépatiques et à des voies liées à l’équilibre de la dopamine et à un type de stress cellulaire létal appelé ferroptose, laissant entendre que ce transporteur se situe à l’intersection du métabolisme, du signalement et de l’immunité dans le cancer du foie.
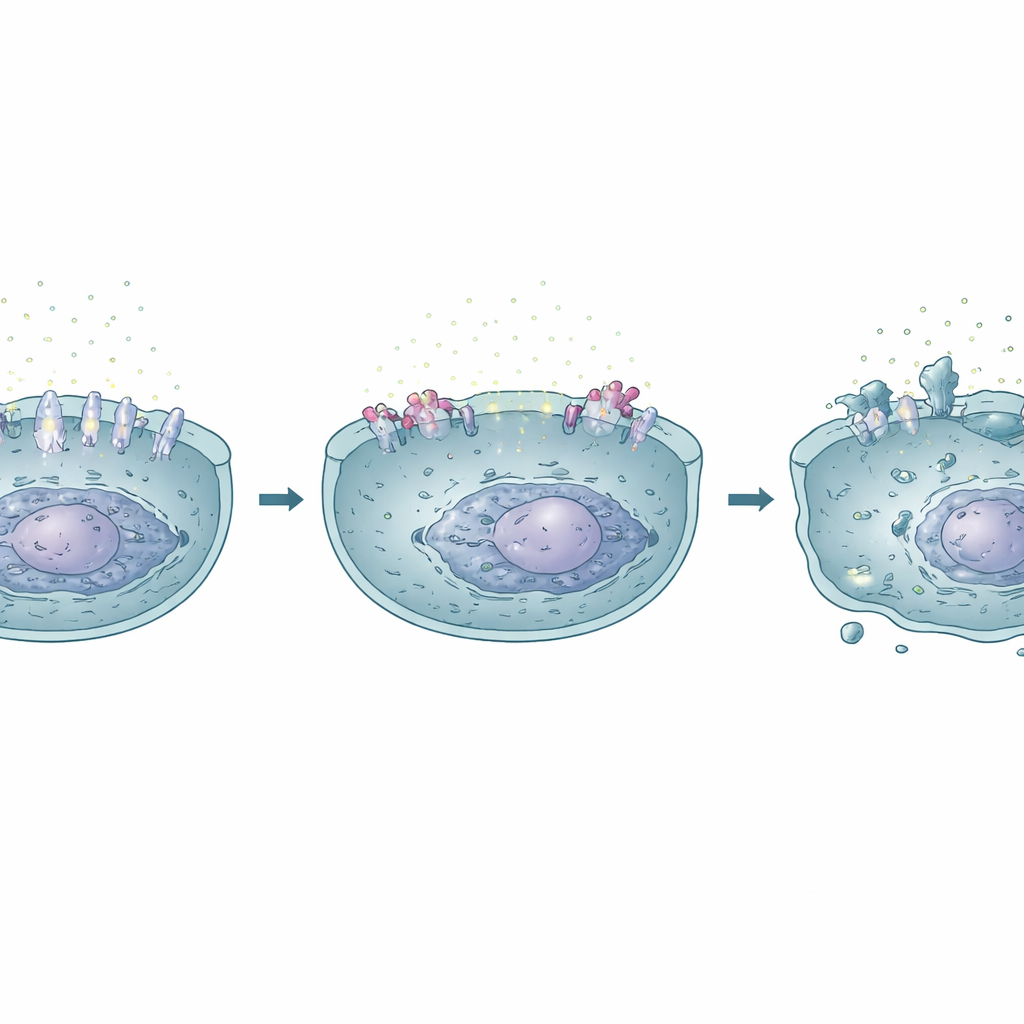
Au-delà d’un gène : un réseau plus large de changements
Si SLC6A3 est apparu comme le protagoniste central, l’impact de la lidocaïne est plus vaste. Le médicament a modifié plusieurs autres gènes connus pour leur rôle dans le cancer et le destin cellulaire. Il a diminué l’expression de TERT, un composant aidant les cellules cancéreuses à maintenir leurs extrémités chromosomiques et à se diviser indéfiniment, et augmenté les niveaux d’ALOX12, une enzyme liée à la ferroptose et à la suppression tumorale. Ensemble, ces changements dessinent un scénario dans lequel la lidocaïne pousse les cellules de cancer du foie vers l’autodestruction tout en rendant le microenvironnement tumoral moins propice à une croissance et une propagation agressives.
Ce que cela signifie pour les patients et les soins futurs
En termes simples, cette étude suggère que la lidocaïne pourrait faire plus que bloquer la douleur — elle pourrait directement affaiblir les cellules du cancer du foie en réprimant un transporteur de dopamine, SLC6A3, et en poussant les cellules vers la mort tout en limitant leur capacité à migrer et à envahir. Parce que la lidocaïne est déjà utilisée dans de nombreuses procédures concernant le cancer du foie, ces résultats ouvrent la possibilité qu’optimiser son mode et son timing d’administration améliore les résultats sans ajouter de médicaments complètement nouveaux. Reste que les travaux actuels reposent principalement sur des modèles cellulaires et des analyses informatiques ; confirmer ces effets chez l’animal et en essais cliniques sera essentiel avant de pouvoir repositionner délibérément la lidocaïne comme alliée ciblée contre le cancer du foie.
Citation: Li, P., Tong, W., He, H. et al. Lidocaine inhibits hepatocellular carcinoma cell proliferation, migration, and invasion through the downregulation of SLC6A3. Sci Rep 16, 11678 (2026). https://doi.org/10.1038/s41598-026-46688-3
Mots-clés: cancer du foie, lidocaïne, transporteur de dopamine, microenvironnement tumoral, ferroptose