Clear Sky Science · ar
الليدوكائين يثبط تكاثر خلايا سرطان الكبد الكبدي، وهجرتها وغزوها عبر خفض تنظيم SLC6A3
لماذا يهم دواء مخدر لسرطان الكبد
يُعرف الليدوكائين أساسًا على أنه الحقنة المخدرة التي تحصل عليها عند طبيب الأسنان أو قبل الجراحة البسيطة. لكن هذه الدراسة تشير إلى أن نفس الدواء قد يساعد بهدوء في مكافحة أحد أخطر السرطانات في العالم: سرطان الكبد الكبدي، وهو الشكل الأكثر شيوعًا لسرطان الكبد. من خلال الخوض في كيفية تفاعل الليدوكائين مع خلايا سرطان الكبد على المستوى الجزيئي، يكشف الباحثون عن هدف جديد مفاجئ يمكن الاستفادة منه لإبطاء نمو الورم وانتشاره.
نظرة أقرب على تحدي سرطان الكبد
يُعد سرطان الكبد من بين أكثر السرطانات شيوعًا وفتكًا على مستوى العالم، وكثير من المرضى يُشخَّصون فقط عندما يكون المرض قد تقدم بالفعل. حتى مع الأدوية الحديثة التي تحفز جهاز المناعة، لا يزال البقاء على المدى الطويل ضعيفًا لمعظم المصابين بسرطان الكبد الكبدي المتقدم. وبما أن الليدوكائين مستخدم على نطاق واسع وآمن عمومًا، فقد يفتح فهم ما إذا كان يمكن أن يعمل أيضًا كعامل مضاد للسرطان الباب لتحسين العلاج دون الحاجة لاختراع دواء جديد بالكامل.
البحث عن أهداف الليدوكائين الخفية
جمع الفريق بين نهجين قويين لرسم خريطة كيفية تأثير الليدوكائين على خلايا سرطان الكبد. أولاً، استخدموا قواعد بيانات «الصيدلة الشبكية» للتنبؤ بمئات البروتينات في الخلايا البشرية التي قد يرتبط بها الليدوكائين. ثم عالجوا خلايا سرطان الكبد (سلالة تسمى HepG2) بالليدوكائين وأجروا تسلسلًا عبر النسخيات، الذي يقيس الجينات التي تُشغل أو تُثبط. من خلال تراكب هذين القائمتين، قلصوا أكثر من 400 هدف متوقع وأكثر من 400 جين متغير إلى تسعة مرشحين رئيسيين فقط يستجيبون لليدوكائين ومن المحتمل أن يتفاعلوا معه مباشرة.
تسليط الضوء على ناقل دوبامين في السرطان
من بين المرشحين التسعة، برز جين واحد: يُسمى SLC6A3، الذي يشفر ناقلًا يساعد عادة الخلايا العصبية على إعادة التقاط مادة الدوبامين الكيميائية في الدماغ. في مجموعات بيانات لمرضى سرطان الكبد، ارتبطت مستويات أعلى من SLC6A3 وجين آخر هو TERT ببقاء أسوأ، مع إظهار SLC6A3 أقوى علاقة. ثم استخدم الباحثون المحاكاة الحاسوبية للتخطيط لكيفية ارتباط الليدوكائين بهذه البروتينات ووجدوا أن الليدوكائين يشكل تفاعلًا ثابتًا أساسه التنافر الهيدروفوبي مع SLC6A3. وعند إعادة النظر في تجارب الخلايا الخاصة بهم، أدى علاج الليدوكائين بوضوح إلى خفض مستويات SLC6A3 في الخلايا السرطانية.
ماذا يحدث عندما يُخفض المفتاح الرئيسي
لاختبار ما إذا كان SLC6A3 أكثر من مجرد مشاهد، تلاعب العلماء مباشرة بمستوياته في خلايا سرطان الكبد. عندما أجبروا الخلايا على خفض SLC6A3، أصبحت الخلايا أقل قابلية للحياة، وأكثر عُرضة للموت المبرمج، وأقل قدرة بكثير على الهجرة والغزو — وهما سلوكانٌ يقومان على انتشار الورم. أما التعبير المفرط عن SLC6A3 فكان له التأثير المعاكس، معززًا النمو والغزو بينما يحمي الخلايا من الموت. ربطت الدراسة أيضًا SLC6A3 بنماذج تسلل الخلايا المناعية في الأورام الكبدية وبمسارات مرتبطة بتوازن الدوبامين ونوع من الإجهاد الخلوي القاتل يسمى الفرروبتوزيس، مما يوحي بأن هذا الناقل يجلس عند مفترق الأيض والإشارة والمناعة في سرطان الكبد.
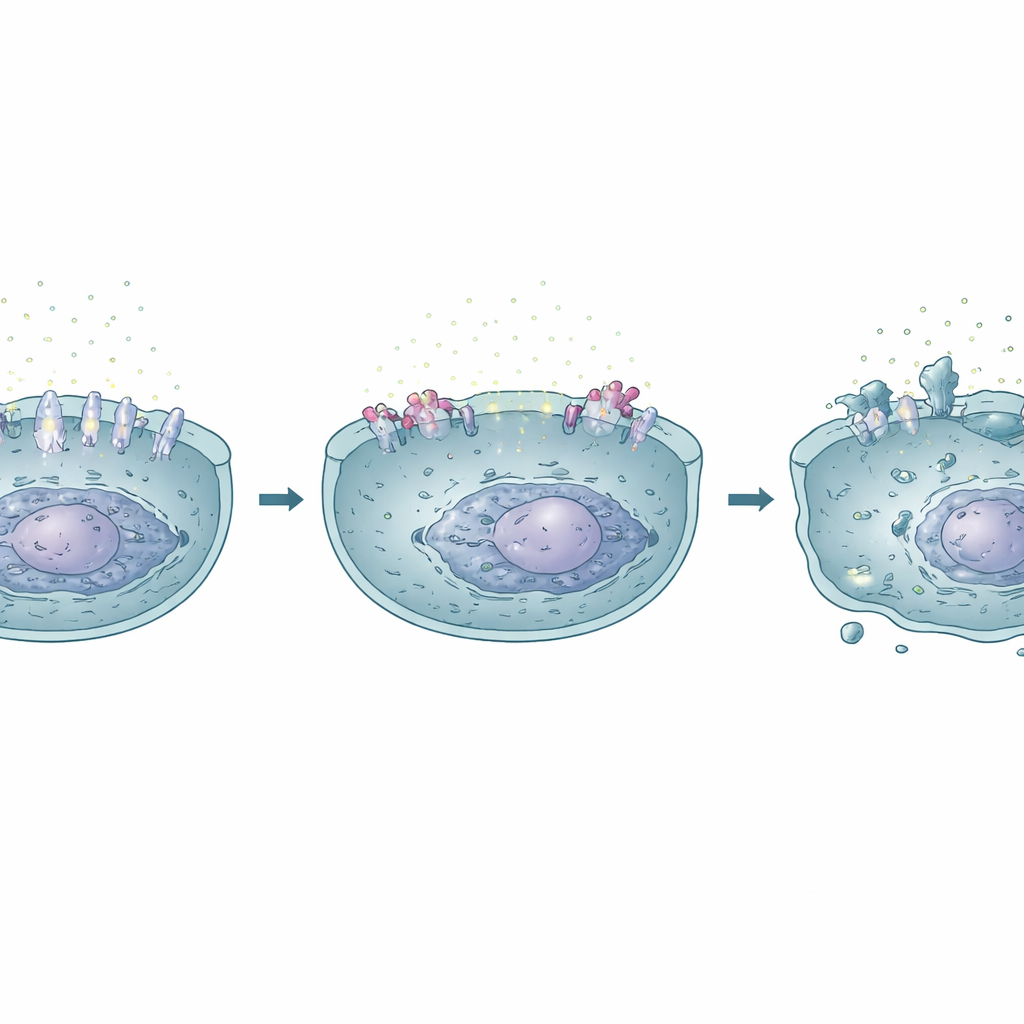
أبعد من جين واحد: شبكة أوسع من التغيرات
بينما برز SLC6A3 كلاعب مركزي، فإن تأثير الليدوكائين أوسع. غيّر الدواء عدة جينات أخرى ذات أدوار معروفة في السرطان ومصير الخلية. خفض تعبير TERT، وهو مكوّن يساعد الخلايا السرطانية على المحافظة على أطراف كروموسوماتها والانقسام بلا حدود، وزاد من مستويات ALOX12، وهو إنزيم مرتبط بالفرروبتوزيس وكبح الأورام. مجتمعة، تدعم هذه التغيرات صورةً حيث يدفع الليدوكائين خلايا سرطان الكبد نحو تدمير ذاتي بينما يجعل بيئة الورم أقل ملاءمة للنمو العدواني والانتشار.
ماذا يعني هذا للمرضى والرعاية المستقبلية
بعبارات بسيطة، تقترح هذه الدراسة أن الليدوكائين قد يفعل أكثر من تخدير الألم — فقد يعيق مباشرة خلايا سرطان الكبد عبر خفض ناقل الدوبامين SLC6A3 ودفع الخلايا نحو الموت مع تقليل قدرتها على الحركة والغزو. وبما أن الليدوكائين مستخدم بالفعل في العديد من إجراءات سرطان الكبد، تثير هذه النتائج احتمال أن تحسين كيفية وموعد إعطائه قد يحسن النتائج دون إضافة أدوية جديدة تمامًا. ومع ذلك، تظل الأعمال المنجزة حتى الآن في المقام الأول على نماذج خلوية وتحليلات حاسوبية؛ سيكون التأكد من هذه التأثيرات في الحيوانات والتجارب السريرية أمرًا أساسيًا قبل أن يمكن إعادة توظيف الليدوكائين عمداً كحليف مستهدف ضد سرطان الكبد.
الاستشهاد: Li, P., Tong, W., He, H. et al. Lidocaine inhibits hepatocellular carcinoma cell proliferation, migration, and invasion through the downregulation of SLC6A3. Sci Rep 16, 11678 (2026). https://doi.org/10.1038/s41598-026-46688-3
الكلمات المفتاحية: سرطان الكبد, ليدوكائين, ناقلة الدوبامين, البيئة الدقيقة للورم, الفرروبتوزيس