Clear Sky Science · nl
Het meten van de toegevoegde waarde van gedeelde trial-elementen (SHASTA): impact op werving, demografie en gegevensvolledigheid via één sponsor
Proeven dichter bij huis brengen
Voor veel mensen betekent deelname aan een medisch onderzoek lange afstanden reizen naar grote ziekenhuizen, werk en gezin combineren en omgaan met ingewikkelde planningen. Dit artikel onderzoekt een nieuwe manier om studies uit te voeren die telefoongesprekken, elektronische formulieren, lokale klinieken en thuiszorg inzet om onderzoek dichter bij de plek te brengen waar mensen daadwerkelijk wonen. Door zes praktijkstudies van één bedrijf te analyseren, stellen de auteurs een praktische vraag: wanneer we sommige trial-activiteiten uit grote onderzoekcentra verplaatsen naar huizen en gemeenschappen, schrijven we dan sneller deelnemers in, bereiken we diversere groepen en verzamelen we nog steeds betrouwbare gegevens?
Waarom traditionele proeven mensen buitensluiten
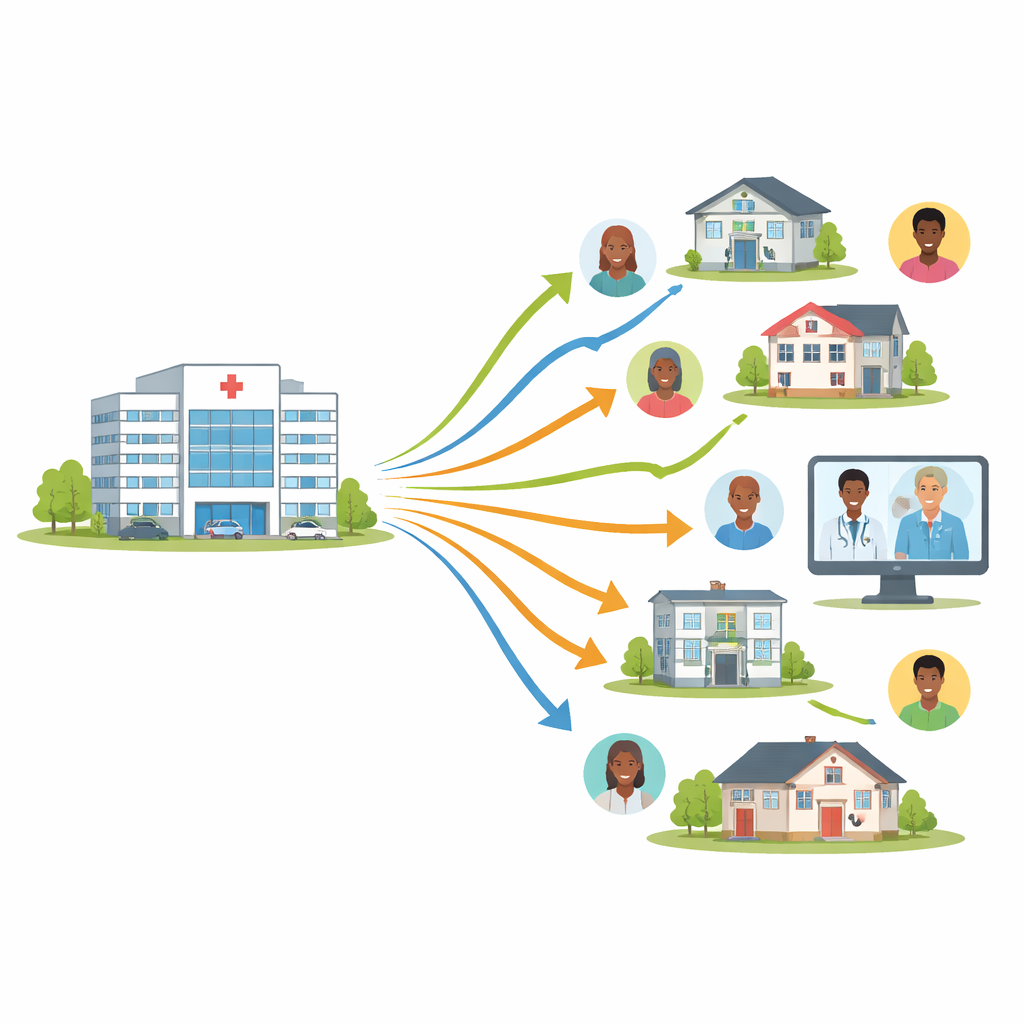
Traditionele klinische proeven draaien om een klein aantal grote ziekenhuizen. Deelnemers moeten deze locaties persoonlijk bezoeken voor toestemming, onderzoeken, laboratoriumtesten en toediening van geneesmiddelen. Deze opzet is duur, tijdrovend en vaak onhandig. Alleen al bij kanker neemt naar schatting slechts 2–8% van de volwassenen deel aan proeven, deels omdat strikte regels en reisvereisten mensen buiten sluiten. Veel patiënten met vergevorderde ziekte wonen een uur of langer van de dichtstbijzijnde triallocatie. In de afgelopen 15 jaar is het aantal triallocaties per studie ook afgenomen, waardoor de toegang nog krapper werd. Als gevolg daarvan kunnen proefresultaten mogelijk niet weerspiegelen hoe geneesmiddelen werken bij mensen in het dagelijks leven, vooral bij personen uit achtergestelde gemeenschappen.
Wat het betekent om een proef te decentraliseren
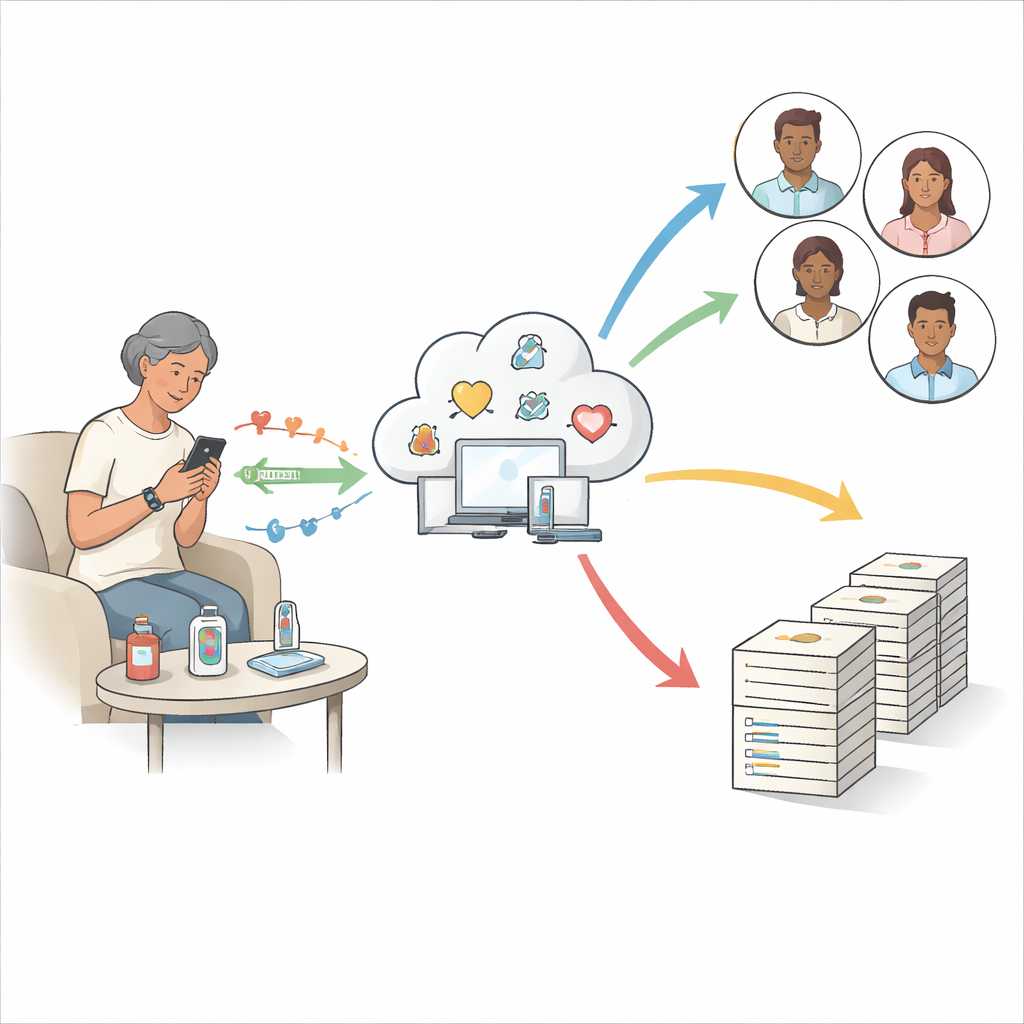
Gedecentraliseerde klinische proeven zijn niet uitsluitend afhankelijk van één ziekenhuis of kliniek. In plaats daarvan kunnen trial-activiteiten op veel plaatsen plaatsvinden: thuis met een verpleegkundige, via videoconsulten, bij lokale laboratoria en klinieken, of via apparaten die op afstand gezondheidsgegevens verzamelen. In de zes bestudeerde onderzoeken kwamen veelvoorkomende elementen voor zoals elektronische toestemming, telezorgafspraken, elektronische vragenlijsten over symptomen of kwaliteit van leven, huisbezoeken door zorgverleners, lokale zorgaanbieders en directe verzending van studiegeneesmiddelen naar deelnemers. Sommige proeven gebruikten zelfs een centraal coördinerend team dat deelnemers in meerdere staten kon werven en volgen, ongeacht waar de hoofdarts fysiek was gevestigd.
Snellere werving en vroege signalen van diversiteit
De auteurs vergeleken hoe snel deelnemers zich inschreven voor deze proeven met historische gemiddelden van vergelijkbare studies. Ze ontdekten dat het toevoegen van gedecentraliseerde elementen samenhing met efficiëntere werving, vooral buiten de oncologie. In kankeronderzoek schreven locaties die deze hulpmiddelen gebruikten iets meer deelnemers per maand in dan oudere, traditionele trials. In niet-kankeronderzoek—met name een grote beroerte-studie—was het verschil veel groter, wat suggereert dat het dichterbij brengen van de proef voor patiënten het proces kan versnellen wanneer tijd en afstand belangrijke barrières zijn. Het team vergeleek ook de raciale en etnische samenstelling van deelnemers met eerdere referentiewaarden. In verschillende studies nam de inschrijving van Aziatische, zwarte en Hispano/Latijns-Amerikaanse deelnemers licht toe, hoewel de auteurs waarschuwen dat dit ook het gevolg kan zijn van gerichte wervingsinspanningen en niet alleen van het gebruik van nieuwe technologieën.
Houden de gegevens stand?
Snellere werving en een bredere reikwijdte zijn alleen van belang als de gegevens betrouwbaar blijven. Om dit te onderzoeken namen de auteurs een nadere blik op één hybride proef die zowel traditionele locaties als virtuele deelname omvatte. Voor kerninformatie die elke deelnemer moet leveren, zoals basale ziektedetails en etniciteit, was de gegevensvolledigheid in beide modellen bijzonder hoog—ongeveer 98–99% in totaal. Maar voor aanvullende metingen die moeilijker te verzamelen zijn, zoals bepaalde functionele of symptoomscores uit medische dossiers, presteerden traditionele locaties beter dan virtuele. Teams ter plaatse hadden vaak gemakkelijker toegang tot volledige testrapporten, terwijl virtuele coördinatoren soms slechts gedeeltelijke of samengevatte informatie zagen. De auteurs merken op dat deze momentopname uit een lopende studie komt, dus deze cijfers kunnen in de loop der tijd verschuiven naarmate systemen verbeteren.
Praktische lessen en waarom het ertoe doet
Het uitvoeren van deels remote proeven is niet zo simpel als het toevoegen van een videoconsult. Het artikel belicht geleerde lessen: het is essentieel om gedecentraliseerde elementen vanaf het begin te plannen; technologieleveranciers moeten aantoonbare ervaring hebben met de specifieke ziekte en medische dossiers; en toezichthouders verwachten duidelijke plannen om toegevoegde risico’s te beheersen, zoals thuisverpleging en complexe gegevensstromen. Aan de positieve kant hielpen centrale coördinerende centra bij het bereiken van patiënten ver buiten het gebruikelijke verzorgingsgebied, en sommige deelnemers gaven duidelijk de voorkeur aan remote opties wanneer ze die keuze kregen. Over het geheel genomen concluderen de auteurs dat gedecentraliseerde benaderingen krachtige instrumenten zijn, maar geen universele oplossing. Doordacht ingezet kunnen ze de werving versnellen, mogelijk verbreden wie deelneemt, en hoge kwaliteit voor kernmetingen behouden. Even belangrijk is dat de vaardigheden en infrastructuur die voor deze proeven zijn opgebouwd een toekomst kunnen ondersteunen waarin alledagzorg—niet alleen onderzoek—flexibeler, digitaler en meer rond het leven van patiënten is ingericht.
Bronvermelding: Yang, A., Mandel, E., Asthana, S. et al. Measuring the added benefits of decentralized trial elements (SHASTA): impact on enrollment, demographics, and data completeness through a single sponsor. Sci Rep 16, 11732 (2026). https://doi.org/10.1038/s41598-026-46193-7
Trefwoorden: gedecentraliseerde klinische proeven, telezorgonderzoek, toegang tot klinische proeven, patiëntgerichte studies, real-world data