Clear Sky Science · nl
Hypoxie of blootstelling aan tabaksrook veroorzaakt regio-specifieke microvasculaire remodelering in de hersenen
Wanneer longziekte de hersenen bereikt
Chronische longaandoeningen zoals COPD worden meestal gezien als problemen met ademhaling en hoesten. Maar de longen zijn de poort van het lichaam voor zuurstof, en als ze falen, kunnen veel andere organen ongemerkt lijden. Deze studie onderzoekt hoe langdurige lage zuurstof of door sigarettenrook veroorzaakte schade in de longen de kleinste bloedvaten van de hersenen in specifieke regio’s kan hervormen, wat mogelijk helpt verklaren waarom mensen met ernstige longziekte vaak geheugenproblemen ontwikkelen en vatbaarder zijn voor hersencomplicaties, waaronder metastasen van longkanker.
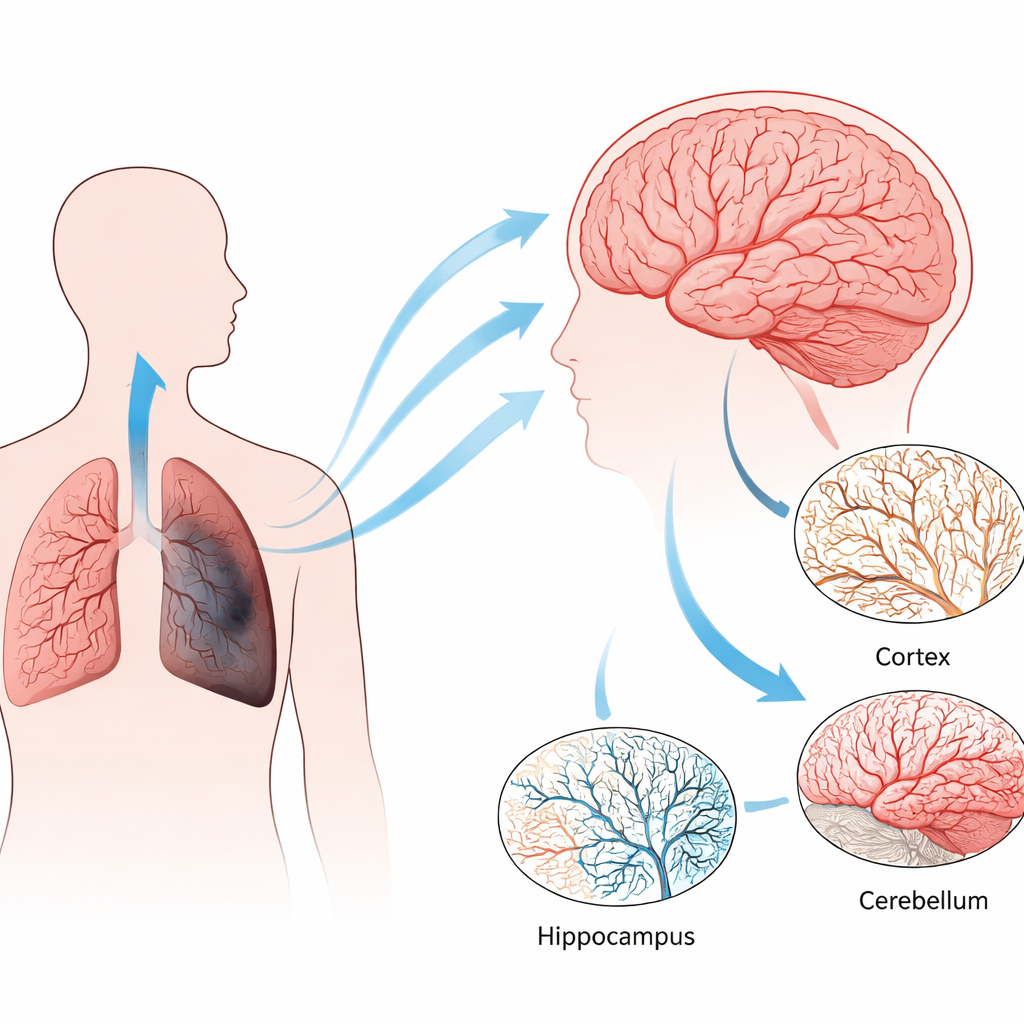
Drie manieren om de longen te belasten
De onderzoekers gebruikten drie muismodellen die verschillende langdurige stressoren nabootsen die bij menselijke longziekten voorkomen. In het ene model werden de dieren in licht verlaagde zuurstof gehouden, wat chronische hypoxie weerspiegelt die ontstaat wanneer beschadigde longen niet genoeg zuurstof meer in het bloed kunnen laden. In de andere twee werden muizen gedurende maanden aan sigarettenrook blootgesteld. Een kortere blootstelling veroorzaakte pulmonale hypertensie, een gevaarlijke stijging van de bloeddruk in de longvaten, terwijl een langere blootstelling zowel pulmonale hypertensie als emfyseem veroorzaakte, het klassieke verlies van luchtzakjes bij COPD. Deze modellen stelden het team in staat de effecten van lage zuurstof te scheiden van die van door rook veroorzaakte ontsteking en schade.
Kleine vaten, grote regionale verschillen
Vervolgens onderzocht het team hoe het capillaire netwerk van de hersenen reageerde in sleutelregio’s: de cortex (betrokken bij denken), de hippocampus (cruciaal voor geheugen), de hersenstam en het cerebellum. Met behulp van fluorescerende markers om de cellen van de bloedvatwand te labelen op dunne weefselsneden, maten ze welk oppervlak door vaten werd ingenomen. Milde chronische hypoxie en het rookmodel met emfyseem leidden beide tot dichtere netwerken van zeer kleine vaten in meerdere regio’s, met name in de hippocampus en het cerebellum. In scherp contrast toonde het rookmodel met alleen pulmonale hypertensie een verlies van microvaten, vooral in de cortex en hippocampus. Drie-dimensionale beeldvorming van geprepareerde, dikkere hersensneden bevestigde deze patronen en benadrukte de hippocampus als het meest gevoelige gebied.
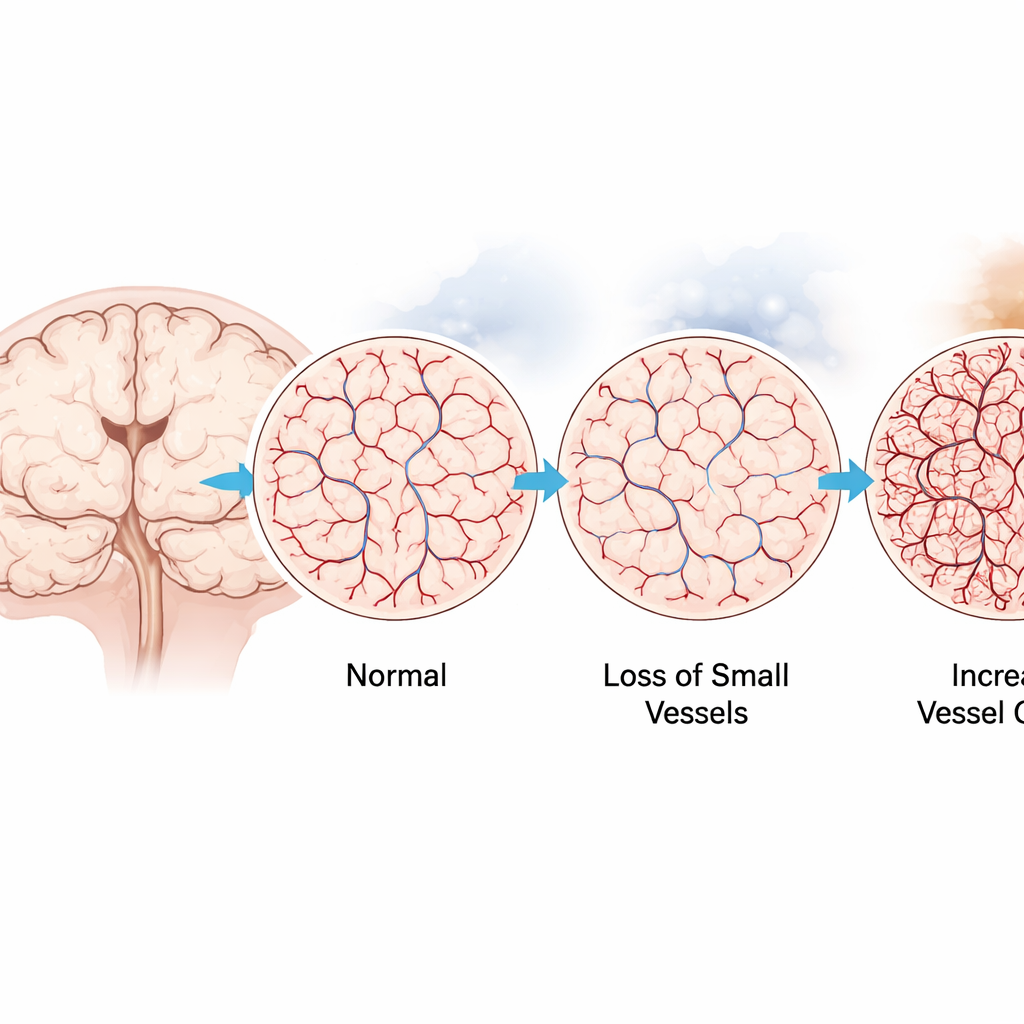
Immuuncellen en lekkage onder de microscoop
Aangezien de residentiële immuuncellen van de hersenen, microglia, bekendstaan om hun rol bij het vormen van bloedvaten, vroegen de onderzoekers zich af of hun aantallen of ruimtelijke verdeling samen met die van de vaten veranderden. Verrassend genoeg vonden ze bij de bestudeerde tijdspunten geen grote verschuivingen in microgliadichtheid of -distributie, wat suggereert dat immuungerichte remodelering ofwel kortstondig is of te subtiel voor standaard telmethoden. Ze keken ook naar aanwijzingen voor lekkage van de bloed–hersenbarrière door fibrinogeen te volgen, een bloedproteïne dat normaal in vaten blijft en stijgt bij systemische ontsteking. In zowel twee- als drie-dimensionale beelden bleef fibrinogeen grotendeels binnen de vaten beperkt, wat wijst op geremodelleerde maar overwegend gesloten capillaire netwerken in plaats van een duidelijke instorting.
Signalen in het bloed en in de hersenen
Om de chemische signalen achter deze structurele veranderingen te onderzoeken, mat het team fibrinogeen en het enzym MMP‑9 in bloedplasma en hersenweefsel. Bij rookblootgestelde muizen was circulerend fibrinogeen hoger, overeenkomend met bevindingen bij mensen met COPD, maar dit vertaalde zich niet in duidelijke ophoping binnen de hersenen. In het lage-zuurstofmodel bleef systemisch fibrinogeen relatief stabiel, terwijl hersenweefsel hogere fibrinogeenniveaus toonde, wat consistent is met lokale depositie binnen groeiende vaten in plaats van lekkage in hersenweefsel. MMP‑9, grotendeels aanwezig in zijn inactieve vorm, was verhoogd in het bloed tijdens chronische hypoxie, terwijl zijn natuurlijke remmer TIMP‑1 niet veranderde, wat erop wijst dat een mogelijke rol van dit enzym bij het hervormen van hersenvaten waarschijnlijk op specifieke locaties wordt gereguleerd in plaats van over de hele circulatie.
Waarom deze veranderingen ertoe doen
Gezamenlijk tonen de experimenten aan dat chronische longproblemen de microcirculatie van de hersenen op regio‑specifieke manieren kunnen hervormen die afhangen van het type en de duur van de stress. Sommige omstandigheden dunnen het capillaire bed uit, terwijl andere extra vaatgroei bevorderen, waarbij de hippocampus naar voren komt als een belangrijk brandpunt. Hoewel dit werk in muizen is uitgevoerd en niet direct tumoren volgt, ondersteunt het het idee dat langdurige longziekte het hersenlandschap stilletjes kan voorbereiden — via veranderde bloedstroom, vaatstructuur en ontstekingssignalen — op manieren die cognitie kunnen beïnvloeden en mogelijk bepalen hoe gemakkelijk kankercellen zich kunnen vestigen. Inzicht in deze verborgen long–hersenverbindingen kan uiteindelijk strategieën begeleiden om kwetsbare hersengebieden te beschermen bij mensen die met chronische longziekte leven.
Bronvermelding: Salik Demirtas, N., Loku, E., Porschen, Y. et al. Hypoxia or tobacco-smoke exposure induce region-specific microvascular remodeling in the brain. Sci Rep 16, 12722 (2026). https://doi.org/10.1038/s41598-026-45975-3
Trefwoorden: COPD, hersenbloedvaten, chronische hypoxie, tabaksrook, long–hersen as