Clear Sky Science · he
היפותוקסיה או חשיפה לעשן טבק מעודדות עיצוב מחדש של המיקרו‑וסקולציה במוח באופן אזורי
כשהמחלה הריאתית מגיעה למוח
מחלות ריאה כרוניות כמו COPD נתפסות בדרך כלל כבעיות נשימה ושיעול. אבל הריאות הן שער הגוף לחמצן, וכשהן נכשלות — גם איברים אחרים עלולים לסבול בשקט. המחקר הזה בוחן כיצד חוסר חמצן ממושך או נזק מעשן סיגריות בריאות יכולים לעצב מחדש את כלי הדם הזעירים ביותר במוח באזורים ספציפיים, והדבר עשוי לעזור להסביר מדוע אנשים עם מחלות ריאה חמורות מפתחים לעתים בעיות זיכרון ונוטים יותר לסיבוכים מוחיים, כולל גרורות של סרטן הריאה.
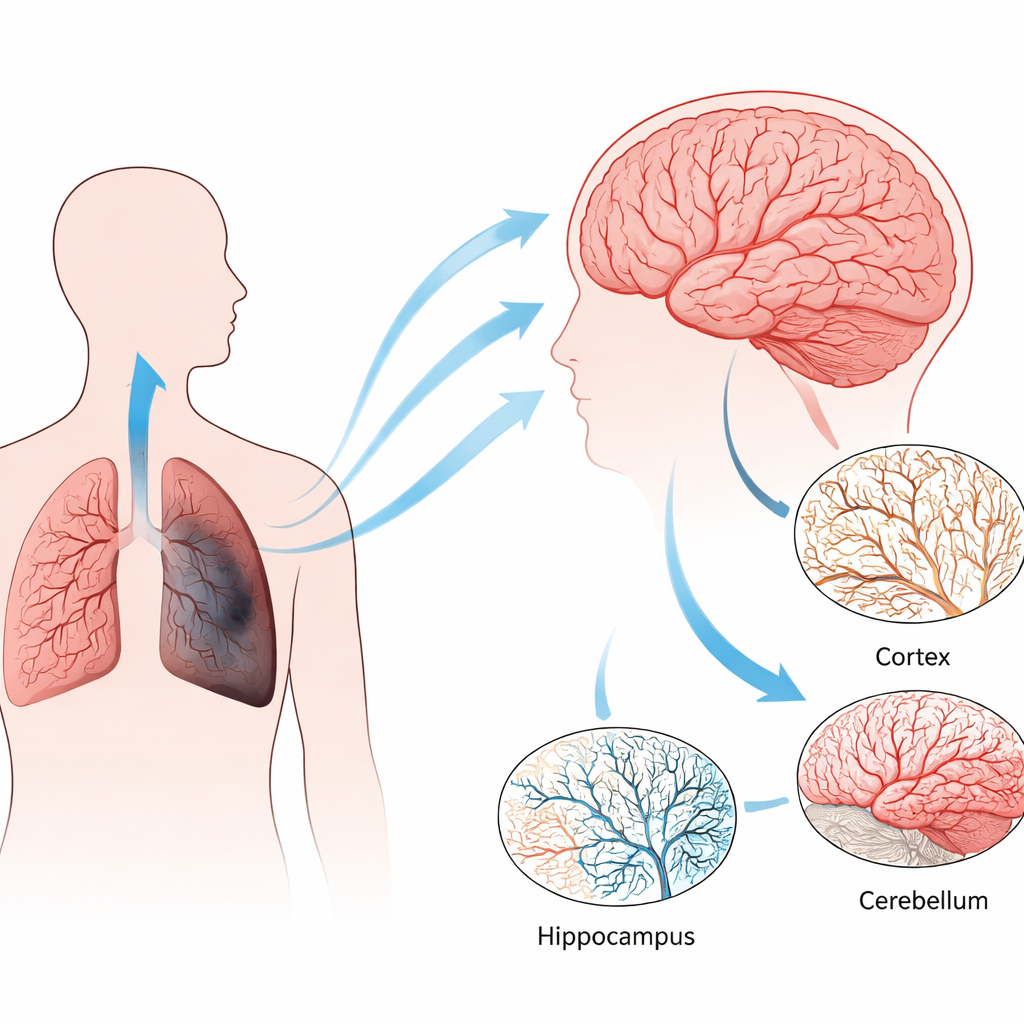
שלוש דרכים להעמיס על הריאות
החוקרים השתמשו בשלוש תבניות עכברים המדמות מתחים כרוניים שונים הנצפים במחלת ריאה אנושית. באחת מהן החזיקו את בעלי החיים בסביבת חמצן מעט נמוכה, המשקפת היפותוקסיה כרונית שמתרחשת כאשר ריאות פגועות אינן מצליחות להעמיס מספיק חמצן לדם. בשתיים האחרות העכברים נשמו עשן סיגריות במשך חודשים. חשיפה קצרה יותר יצרה יתר לחץ דם ריאתי — עלייה מסוכנת בלחץ בכלי הדם של הריאות — בעוד שחשיפה ממושכת יותר גרמה גם ליתר לחץ דם ריאתי וגם לאמפיזמה, אובדן המעטפות האווריריות המוכר ב‑COPD. המודלים הללו איפשרו להפריד בין השפעות חוסר החמצן להשפעות הדלקת והנזק הנגרמות מעשן.
כלי דם זעירים, הבדלים אזוריים גדולים
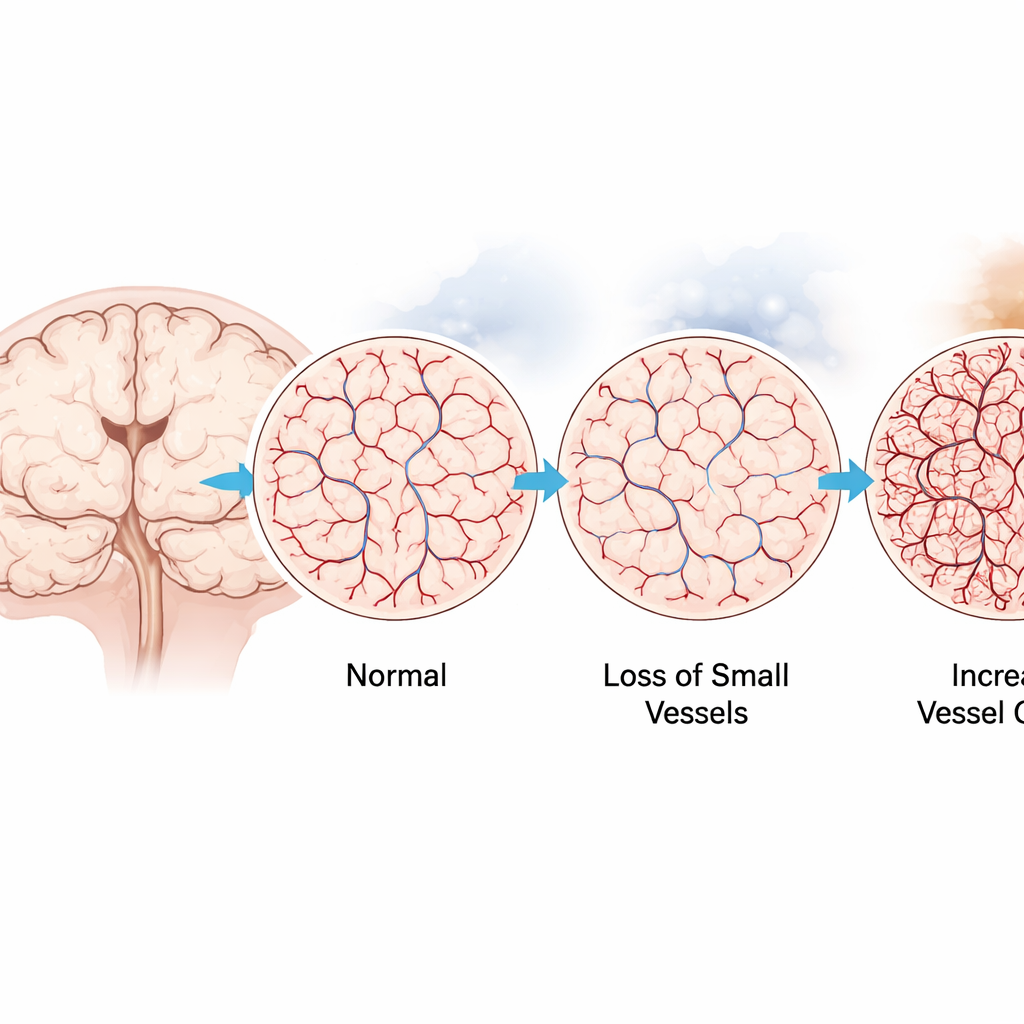
הצוות בדק כיצד רשת הנימים במוח הגיבה באזורים מרכזיים: הקורטקס (מעורב במחשבה), ההיפוקמפוס (חיוני לזיכרון), גזע המוח והצרבלום. באמצעות סימוני פלואורסצנטיות לתאי ציפוי כלי הדם בפרוסות רקמה דקות, מדדו כמה שטח תפסו הכלים. היפותוקסיה כרונית מתונה ומודל העשן שכלל אמפיזמה הובילו לרשתות צפופות יותר של כלי דם זעירים במספר אזורים, במיוחד בהיפוקמפוס ובצרבלום. בניגוד חריף לכך, המודל של העשן שכלל רק יתר לחץ דם ריאתי הראה אובדן מיקרו‑כלי דם, במיוחד בקורטקס ובהיפוקמפוס. הדמיה תלת‑ממדית של פרוסות מוח עבות שהובהרו אישרה תבניות אלה והבליטה את ההיפוקמפוס כאזור הרגיש ביותר.
תאי חיסון ונזקי דליפה תחת המיקרוסקופ
מכיוון שתאי החיסון התושבים במוח, המיקרוגליה, ידועים כמסייעים בעיצוב כלי דם, שאלו החוקרים האם מספרם או מרחקיהם השתנו יחד עם הכלים. באופן מפתיע הם לא מצאו שינויים משמעותיים בצפיפות או בהפצת המיקרוגליה בנקודות הזמן שנבדקו, מה שמרמז שכל עיצוב מחודש מונע על‑ידי מערכת החיסון הוא או קצר־זמני או עדין מדי לשיטות הספירה הסטנדרטיות. הם גם חיפשו סימנים לקרע ב‑blood–brain barrier על‑ידי מעקב אחרי פיברינוגן, חלבון דם שבדרך כלל נשאר בתוך כלי הדם ומעלה בערים דלקתיות מערכתיות. בתמונות דו־ממדיות ותלת‑ממדיות, הפיברינוגן נותר ברובו מוגבל לכלי הדם, מה שמצביע על רשתות נימים שעוצבו מחדש אך נשארו ברובה אטומות ולא על קרע גלוי.
אותות בדם ובמוח
כדי לחקור את האותות הכימיים שמאחורי השינויים המבניים האלה, מדדו החוקרים פיברינוגן ואת האנזים MMP‑9 בפלזמה וברקמת המוח. בעכברים שנחשפו לעשן, פיברינוגן במעגל הדם היה גבוה יותר, מה שמשקף ממצאים אצל בני אדם עם COPD, אך זה לא התבטא בהצטברות ברורה בתוך המוח. במודל חוסר החמצן, פיברינוגן מערכתית נשארה יחסית יציבה, בעוד שרקמת המוח הציגה רמות פיברינוגן גבוהות יותר — תואם להצבעה מקומית בתוך כלי דם גדלים במקום לדליפה לרקמת המוח. MMP‑9, שברובו נמצא בצורתו הבלתי פעילה, עלה בדם במהלך היפותוקסיה כרונית, בעוד חסמו הטבעי TIMP‑1 לא השתנה, מה שמרמז שתפקידו האפשרי של אנזים זה בעיצוב כלי הדם במוח נשלט כנראה באתרים ספציפיים ולא בכל מערכת ההנשלה כולה.
מדוע השינויים האלה חשובים
בהשוואה כוללת, הניסויים מראים שמחלות ריאה כרוניות יכולות לעצב מחדש את המיקרו‑מחזוריות של המוח באופן שנקבע לפי סוג ומשך העומס. תנאים מסוימים מדלילים את מרבד הנימים, בעוד אחרים מקדמים צמיחת כלי דם נוספת, כשההיפוקמפוס בולט כנקודת חום מרכזית. אף על פי שהמחקר בוצע בעכברים ואינו עוקב ישירות אחרי גידולים, הוא תומך ברעיון שמחלת ריאה ממושכת יכולה להכין בשקט את נוף המוח — באמצעות שינויים בזרימת הדם, במבנה הכלי ובאותות דלקתיים — באופן שעשוי להשפיע על קוגניציה ואפילו על הנטייה של תאי סרטן להשתקע. הבנת הקשרים המוסתרים בין ריאות למוח עשויה בסופו של דבר להנחות אסטרטגיות להגנה על אזורים מוחיים פגיעים באנשים החיים עם מחלת ריאה כרונית.
ציטוט: Salik Demirtas, N., Loku, E., Porschen, Y. et al. Hypoxia or tobacco-smoke exposure induce region-specific microvascular remodeling in the brain. Sci Rep 16, 12722 (2026). https://doi.org/10.1038/s41598-026-45975-3
מילות מפתח: COPD, כלי דם במוח, היפותוקסיה כרונית, עשן טבק, ציר ריאות–מוח