Clear Sky Science · de
Hypoxie oder Tabakrauch‑Exposition induzieren regionsspezifisches mikrovasculäres Remodeling im Gehirn
Wenn Lungenerkrankung das Gehirn erreicht
Chronische Lungenerkrankungen wie COPD werden meist als Probleme beim Atmen und Husten verstanden. Die Lunge ist jedoch das Tor des Körpers für Sauerstoff, und wenn sie versagt, können viele andere Organe unbemerkt Schaden nehmen. Diese Studie untersucht, wie anhaltend niedriger Sauerstoff oder durch Zigarettenrauch verursachter Lungenschaden die winzigsten Blutgefäße des Gehirns in bestimmten Regionen umgestalten kann. Das könnte dazu beitragen zu erklären, warum Menschen mit schwerer Lungenerkrankung oft Gedächtnisprobleme entwickeln und anfälliger für Hirnkomplikationen sind, einschließlich Metastasen von Lungenkrebs.
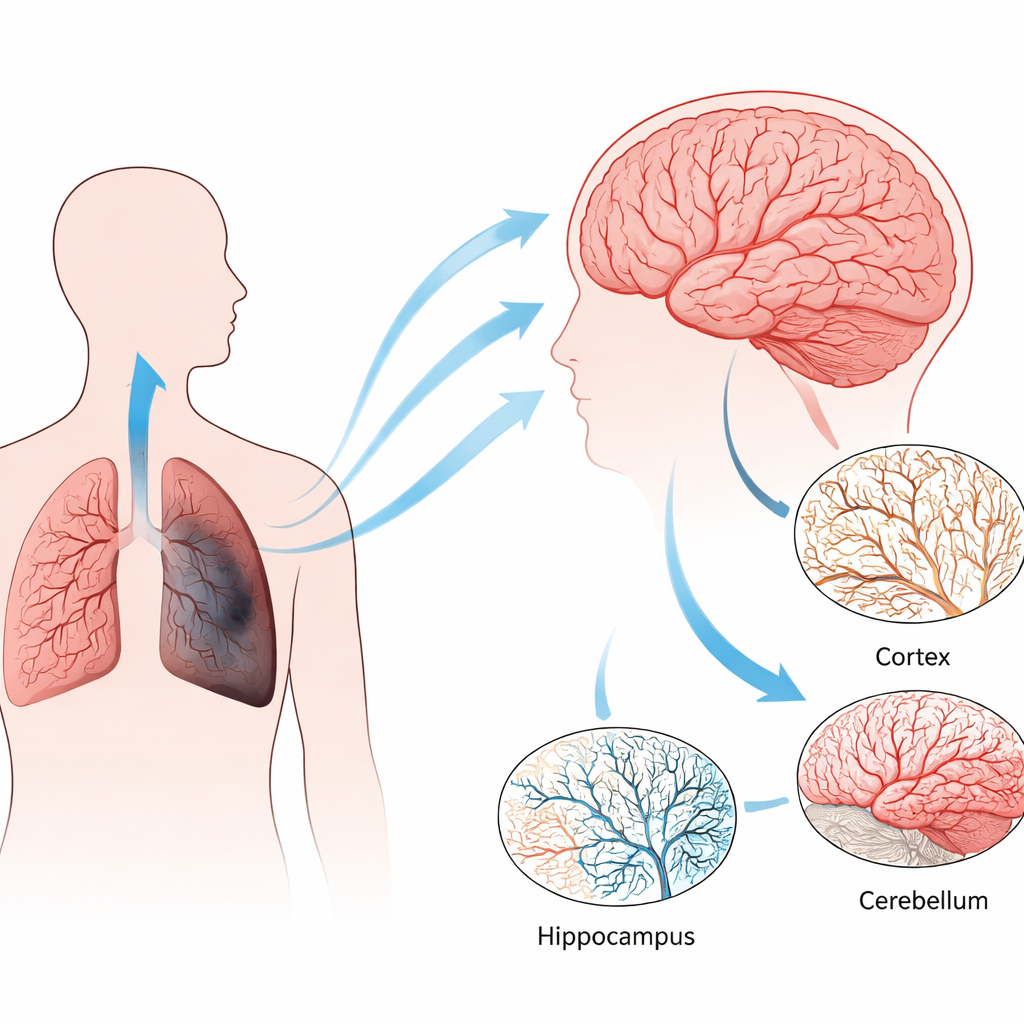
Drei Wege, die Lunge zu belasten
Die Forschenden verwendeten drei Mausmodelle, die unterschiedliche, langanhaltende Belastungen nachahmen, wie sie bei menschlichen Lungenerkrankungen vorkommen. In einem Modell wurden die Tiere in mild niedriger Sauerstoffumgebung gehalten, was die chronische Hypoxie widerspiegelt, die entsteht, wenn geschädigte Lungen nicht mehr genügend Sauerstoff in das Blut bringen. In den beiden anderen inhalierten die Mäuse über Monate Zigarettenrauch. Eine kürzere Exposition erzeugte pulmonale Hypertonie, einen gefährlichen Blutdruckanstieg in den Gefäßen der Lunge, während eine längere Exposition sowohl pulmonale Hypertonie als auch Emphysem — den typischen Verlust von Lungenbläschen bei COPD — auslöste. Diese Modelle erlaubten es dem Team, die Effekte von Sauerstoffmangel von denen durch Rauch‑bedingte Entzündung und Schädigung zu trennen.
Winzige Gefäße, große regionale Unterschiede
Das Team untersuchte anschließend, wie das Kapillarnetz des Gehirns in Schlüsselregionen reagierte: der Großhirnrinde (Beteiligung an Denken), dem Hippocampus (entscheidend für Gedächtnis), dem Hirnstamm und dem Kleinhirn. Mit fluoreszierenden Markern zur Kennzeichnung der Gefäßendothelzellen auf dünnen Gewebeschnitten maßen sie den von Gefäßen eingenommenen Flächenanteil. Milde chronische Hypoxie und das Rauchmodell mit Emphysem führten in mehreren Regionen, besonders im Hippocampus und Kleinhirn, zu dichteren Netzwerken winziger Gefäße. Im scharfen Kontrast dazu zeigte das Rauchmodell mit nur pulmonaler Hypertonie einen Verlust von Mikrogefäßen, vor allem in Rinde und Hippocampus. Dreidimensionale Aufnahmen von geklärten, dickeren Hirnschnitten bestätigten diese Muster und machten den Hippocampus zur am stärksten empfindlichen Region.
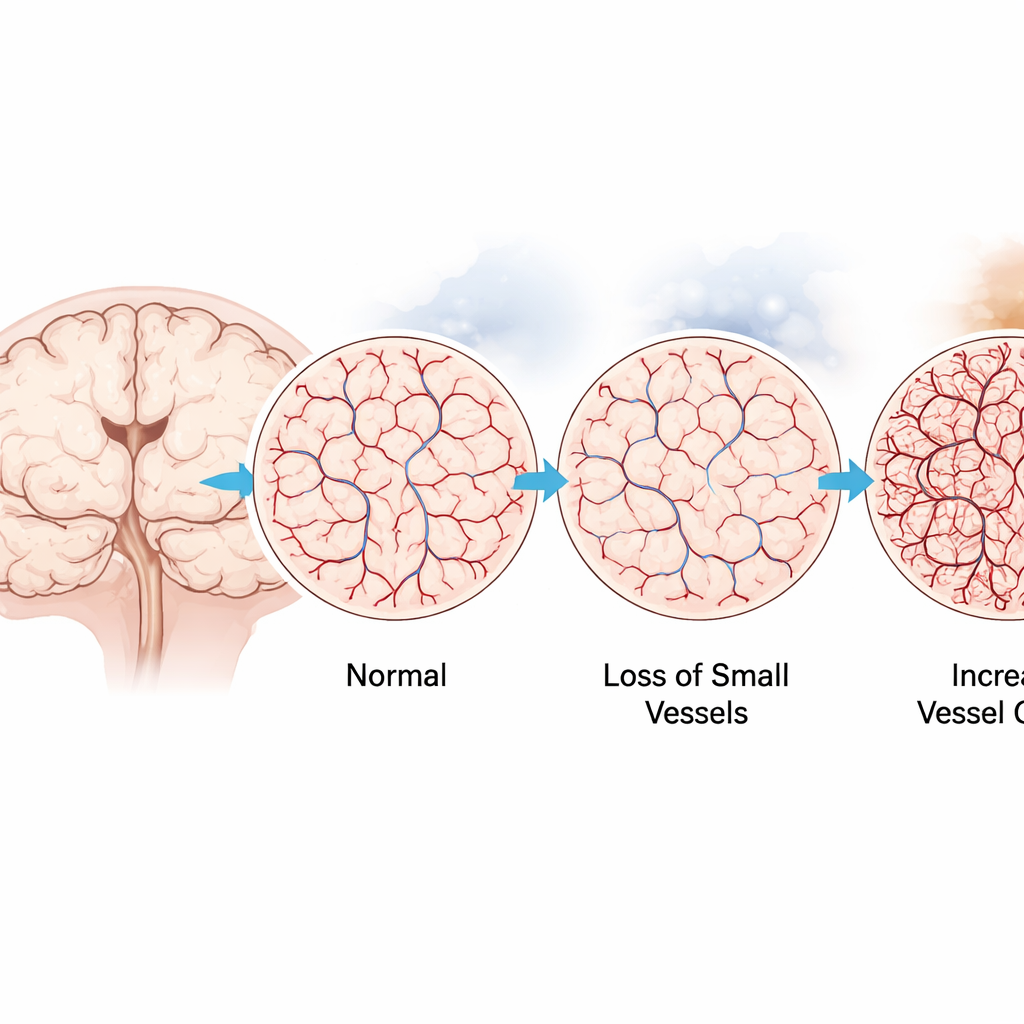
Immunzellen und Undichtigkeiten unter dem Mikroskop
Da die im Gehirn ansässigen Immunzellen, Mikroglia, dafür bekannt sind, an der Formung von Blutgefäßen mitzuwirken, fragten die Forschenden, ob sich deren Zahl oder Verteilung parallel zu den Gefäßen veränderte. Überraschenderweise fanden sie zu den untersuchten Zeitpunkten keine größeren Verschiebungen in Dichte oder Verteilung der Mikroglia, was nahelegt, dass immunvermittelte Umgestaltungen entweder nur kurz andauern oder für Standardzählmethoden zu subtil sind. Sie suchten auch nach Anzeichen einer Schädigung der Blut‑Hirn‑Schranke, indem sie Fibrinogen verfolgten — ein Blutprotein, das normalerweise in Gefäßen verbleibt und bei systemischer Entzündung ansteigt. In zwei‑ und dreidimensionalen Bildern blieb Fibrinogen überwiegend innerhalb der Gefäße, was eher auf umgestaltete, aber weitgehend verschlossene Kapillarnetzwerke als auf einen offensichtlichen Zusammenbruch hinweist.
Signale im Blut und im Gehirn
Um die chemischen Signale hinter diesen strukturellen Veränderungen zu untersuchen, maßen die Forschenden Fibrinogen und das Enzym MMP‑9 im Blutplasma und im Hirngewebe. Bei rauchexponierten Mäusen war das zirkulierende Fibrinogen erhöht, was Befunden bei Menschen mit COPD entspricht, doch dies führte nicht zu einer klaren Akkumulation im Gehirn. Im Niedrig‑Sauerstoff‑Modell blieb das systemische Fibrinogen relativ stabil, während im Hirngewebe höhere Fibrinogenwerte nachweisbar waren — konsistent mit lokaler Ablagerung in wachsenden Gefäßen statt einem generellen Austritt ins Hirngewebe. MMP‑9, überwiegend in inaktiver Form vorhanden, war während chronischer Hypoxie im Blut erhöht, während sein natürlicher Hemmer TIMP‑1 unverändert blieb. Das deutet darauf hin, dass eine mögliche Rolle dieses Enzyms beim Umbau von Hirngefäßen eher an spezifischen Orten als im gesamten Kreislauf kontrolliert wird.
Warum diese Veränderungen wichtig sind
Zusammen zeigen die Experimente, dass chronische Lungenprobleme die Mikro‑Zirkulation des Gehirns regionsspezifisch umgestalten können, abhängig von Art und Dauer der Belastung. Manche Zustände dünnen das Kapillarbett aus, andere fördern zusätzliches Gefäßwachstum, wobei der Hippocampus als Schlüssel‑Hotspot hervorgeht. Obwohl diese Arbeit an Mäusen durchgeführt wurde und Tumoren nicht direkt verfolgt wurden, stützt sie die Idee, dass Langzeit‑Lungenerkrankungen die Landschaft des Gehirns still vorbereiten können — durch veränderten Blutfluss, Gefäßstruktur und entzündliche Signale — in einer Weise, die Kognition und möglicherweise die Ansiedlung von Krebszellen beeinflussen kann. Das Verständnis dieser verborgenen Lungen–Gehirn‑Verbindungen könnte letztlich dazu beitragen, Strategien zu entwickeln, um besonders gefährdete Hirnregionen bei Menschen mit chronischer Lungenerkrankung zu schützen.
Zitation: Salik Demirtas, N., Loku, E., Porschen, Y. et al. Hypoxia or tobacco-smoke exposure induce region-specific microvascular remodeling in the brain. Sci Rep 16, 12722 (2026). https://doi.org/10.1038/s41598-026-45975-3
Schlüsselwörter: COPD, Hirngefäße, chronische Hypoxie, Tabakrauch, Lungen–Gehirn‑Achse