Clear Sky Science · nl
ZIF-8 gefunctionaliseerde PCL/BG composietscaffolds met verbeterde bioactiviteit en osteogene differentiatie
Helpen gebroken botten zichzelf te genezen
Wanneer een bot ernstig beschadigd is door een ongeluk, tumor of ziekte, kan het lichaam de kloof niet altijd zelfstandig herstellen. Chirurgen vertrouwen vaak op bottransplantaten, maar die zijn schaars en brengen risico's met zich mee. Deze studie onderzoekt een nieuw type 3D-geprint "botpleister" dat sterk genoeg is voor dagelijks gebruik in het lichaam en tegelijkertijd actief botcellen aanmoedigt om te groeien, zich te hechten en zich te ontwikkelen tot gezond nieuw weefsel.
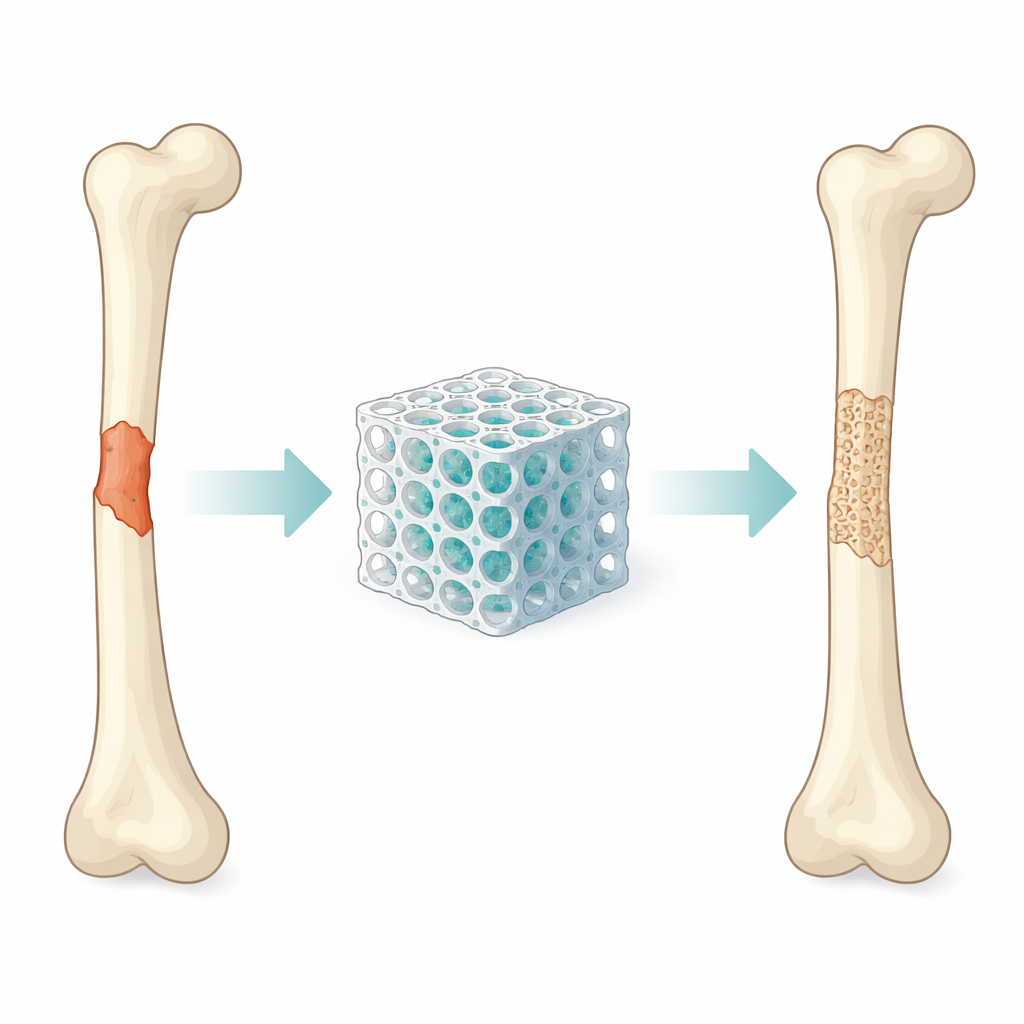
Waarom we slimmere botpleisters nodig hebben
Artsen zoeken al lang naar materialen die een ontbrekend bot kunnen vervangen. Traditionele metalen implantaten zijn sterk maar hechten niet natuurlijk aan levend weefsel. Donorbloed van de patiënt of een ander persoon kan goed integreren maar is beperkt beschikbaar en kan pijn of complicaties veroorzaken. Weefselbouwers maken in plaats daarvan poreuze structuren, scaffolds genaamd, die fungeren als tijdelijke raamwerken: ze ondersteunen het beschadigde gebied, laten bloedvaten en cellen binnendringen en verdwijnen langzaam naarmate nieuw bot ontstaat. Hiervoor moet een scaffold drie eigenschappen tegelijk in balans houden: mechanische stevigheid, celvriendelijkheid en voldoende chemische activiteit om botgroei te stimuleren.
Het bouwen van een beter 3D-geprint raamwerk
De onderzoekers begonnen met een veelgebruikt medisch kunststof, polycaprolacton, dat gemakkelijk 3D te printen is maar van nature te zacht en te inert voor veeleisende botreparaties. Ze mengden dit kunststof met grote hoeveelheden ultrafijne deeltjes van een speciaal bioactief glas bekend als 58S. Dit glas staat bekend om het vormen van een botachtige minerallaag bij contact met lichaamsvloeistoffen en het afgeven van nuttige ionen zoals calcium en silicium. Het team printte poreuze, kubusvormige scaffolds met 40, 45 of 50 procent glas naar gewicht en testte hoeveel compressie elk ontwerp kon weerstaan. De versie met 45 procent glas bleek het beste compromis en bereikte ongeveer 35 megapascal aan sterkte—vergelijkbaar met het sponsachtige (corticale) bot in onze grotere botten—terwijl het voldoende poreus bleef voor weefselingroei.
Een passief frame veranderen in een actieve partner
Om het oppervlak waar cellen eerst landen verder te verbeteren, bedekte het team de gekozen scaffold met 45 procent glas met een dunne laag van een poreus materiaal genaamd ZIF-8, dat zink bevat. Met een zachte, watergebaseerde methode geïnspireerd op mosselhechtingschemie brachten ze eerst een kleverige onderlaag aan en lieten vervolgens kleine ZIF-8 kristallen direct op de buitenoppervlakken van de scaffold groeien. In een vloeistof die bloedplasma nabootst, gaven de scaffolds geleidelijk zinkionen vrij gedurende vier weken zonder een initiële piek, en bleven ze binnen een concentratiebereik dat als veilig voor cellen wordt beschouwd. Tegelijkertijd gaf het glas in de scaffold calcium, fosfor en silicium af, wat hielp bij de vorming van een botachtige mineraallaag op het oppervlak.
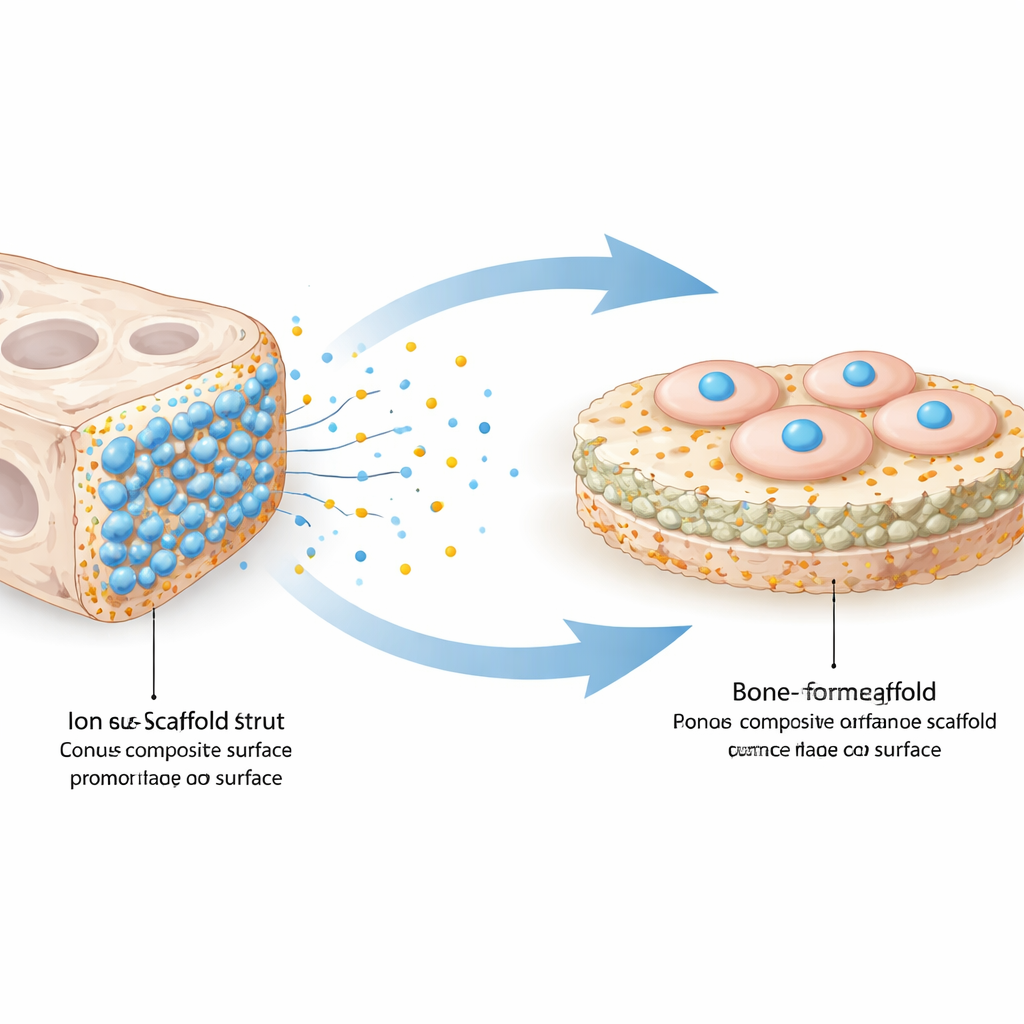
Hoe botcellen reageren op de nieuwe scaffold
Vervolgens testte het team hoe botachtige cellen zich gedroegen op de niet-gecoate en ZIF-8-gecoate scaffolds. Onder de microscoop lieten beide types cellen toe zich te hechten en uit te spreiden, maar de zink-gecoate variant toonde merkbaar dichtere en gelijkmatigere celbedekking na slechts enkele dagen. Een standaard levensvatbaarheidstest toonde aan dat cellen op de gemodificeerde scaffold niet alleen overleefden maar sneller vermenigvuldigden dan op de platte controlovervlakte en de onbewerkte scaffold. Toen de onderzoekers de activiteit maten van verschillende genen die betrokken zijn bij botvorming, inclusief vroege "schakel"genen en late markers van rijpe botcellen, vonden ze dat alle genen significant hoger tot expressie kwamen op de zink-gecoate scaffold—vooral op latere tijdstippen, wanneer normaal gesproken gemineraliseerde botmatrix wordt afgezet.
Wat dit kan betekenen voor toekomstige botreparatie
Samengevat suggereren de resultaten dat het combineren van een hoge dosis bioactief glas binnen het 3D-geprinte kunststof met een zinkrijke buitencoating een multifunctionele scaffold creëert die sterk is, langzaam afbreekt en zeer gastvrij is voor botcellen. Het materiaal is gericht op het opvullen van defecten in sponsachtig bot, waar het belastingen kan dragen terwijl het het lichaam aanmoedigt zichzelf te herbouwen. Hoewel verdere dierstudies nodig zijn om de langetermijnveiligheid en -prestaties te bevestigen, wijst dit dubbelwerkende ontwerp op next-generation botpleisters die veel meer doen dan alleen ruimte innemen—ze sturen en versnellen het genezingsproces actief van binnenuit naar buiten.
Bronvermelding: Soleymani, M., Moslemi, S., Dini, G. et al. ZIF-8 functionalized PCL/BG composite scaffolds with improved bioactivity and osteogenic differentiation. Sci Rep 16, 14335 (2026). https://doi.org/10.1038/s41598-026-44943-1
Trefwoorden: botweefselengineering, 3D-geprinte scaffolds, bioactief glas, polycaprolacton, ZIF-8 coating