Clear Sky Science · fr
Échafaudages composites PCL/GB fonctionnalisés par ZIF-8 avec une bioactivité et une différenciation ostéogénique améliorées
Aider les os cassés à se réparer eux-mêmes
Lorsqu’un os est gravement endommagé par un accident, une tumeur ou une maladie, l’organisme n’est pas toujours capable de combler la perte seul. Les chirurgiens comptent souvent sur des greffes osseuses, mais celles-ci peuvent être rares et comporter des risques. Cette étude explore un nouveau type de « pansement osseux » imprimé en 3D conçu pour être suffisamment solide pour un usage interne tout en encourageant activement les cellules osseuses à croître, à s’attacher et à mûrir pour former un nouveau tissu sain.
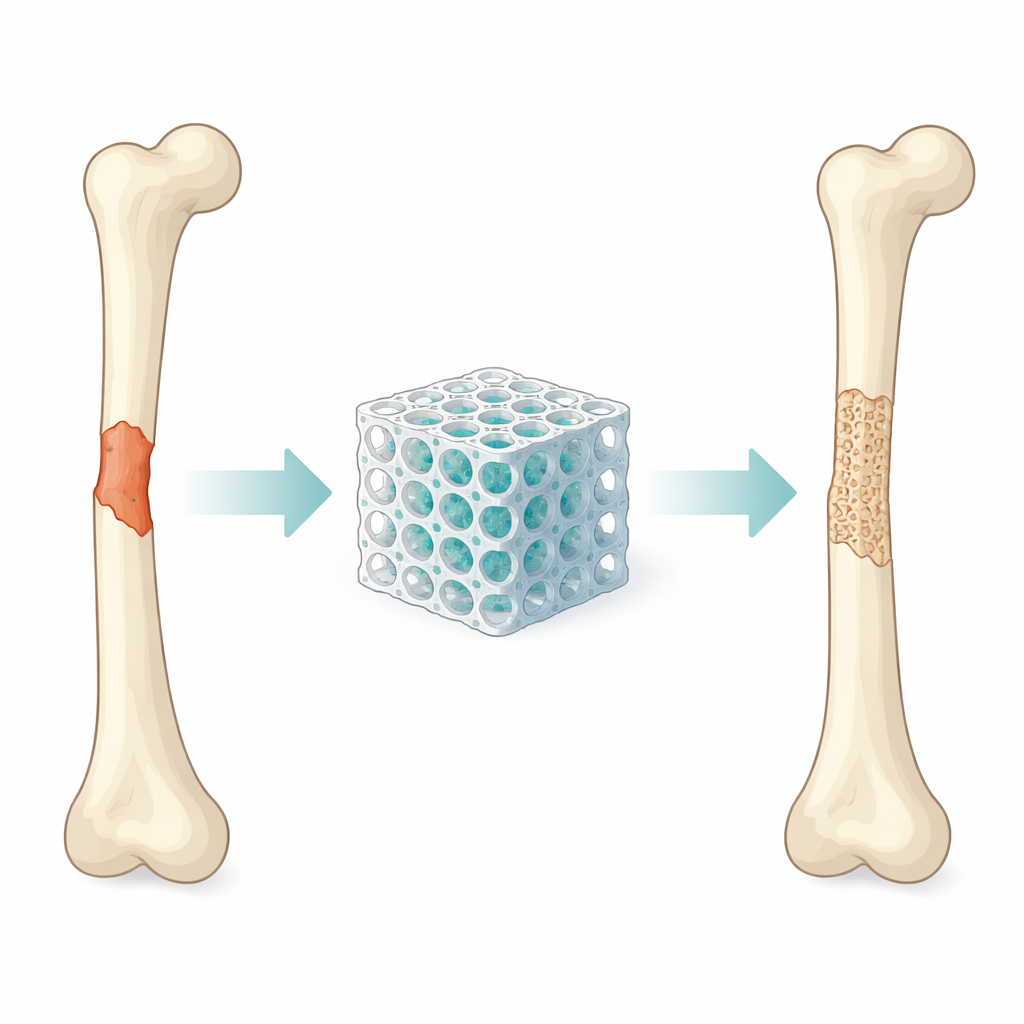
Pourquoi nous avons besoin de pansements osseux plus intelligents
Les médecins recherchent depuis longtemps des matériaux capables de remplacer l’os manquant. Les implants métalliques traditionnels sont solides mais ne se lient pas naturellement au tissu vivant. L’os donneur, issu du patient ou d’un autre individu, peut bien s’intégrer mais son approvisionnement est limité et il peut provoquer douleur ou complications. Les ingénieurs tissulaires fabriquent donc des structures poreuses appelées échafaudages qui servent de cadres temporaires : ils soutiennent la zone endommagée, laissent les vaisseaux sanguins et les cellules pénétrer, et disparaissent progressivement à mesure que le nouvel os se forme. Pour que cela fonctionne, un échafaudage doit concilier trois exigences : être mécaniquement robuste, compatible avec les cellules et suffisamment chimiquement actif pour déclencher la formation osseuse.
Construire un meilleur cadre imprimé en 3D
Les chercheurs ont commencé par un plastique médical couramment utilisé, la polycaprolactone, facile à imprimer en 3D mais naturellement trop souple et trop inerte pour les réparations osseuses exigeantes. Ils ont mélangé ce plastique avec de fortes quantités de particules ultrafines d’un verre bioactif spécial connu sous le nom de 58S. Ce verre est réputé pour former une couche minérale similaire à l’os au contact des fluides corporels et pour libérer des ions bénéfiques tels que le calcium et le silicium. L’équipe a imprimé des échafaudages poreux en forme de cube contenant 40, 45 ou 50 pour cent de verre en poids et a testé la résistance en compression de chaque conception. La version avec 45 pour cent de verre s’est révélée le meilleur compromis, atteignant environ 35 mégapascals de résistance—similaire à l’os spongieux (cancellous) présent à l’intérieur des os longs—tout en restant suffisamment poreuse pour permettre la croissance tissulaire.
Transformer un cadre passif en partenaire actif
Pour améliorer la surface sur laquelle les cellules s’implantent, l’équipe a recouvert l’échafaudage choisi (45 % de verre) d’une fine couche d’un matériau poreux appelé ZIF‑8, contenant du zinc. En utilisant un procédé doux à base d’eau inspiré de la chimie adhésive des moules, ils ont d’abord déposé une sous-couche adhésive puis fait croître de minuscules cristaux de ZIF‑8 directement sur les surfaces externes de l’échafaudage. Dans un fluide mimant le plasma sanguin, les échafaudages ont libéré du zinc de manière régulière pendant quatre semaines sans pic initial, restant dans une plage de concentration considérée comme sûre pour les cellules. Parallèlement, le verre à l’intérieur de l’échafaudage a libéré du calcium, du phosphore et du silicium, favorisant la formation d’un revêtement minéral de type osseux à la surface.
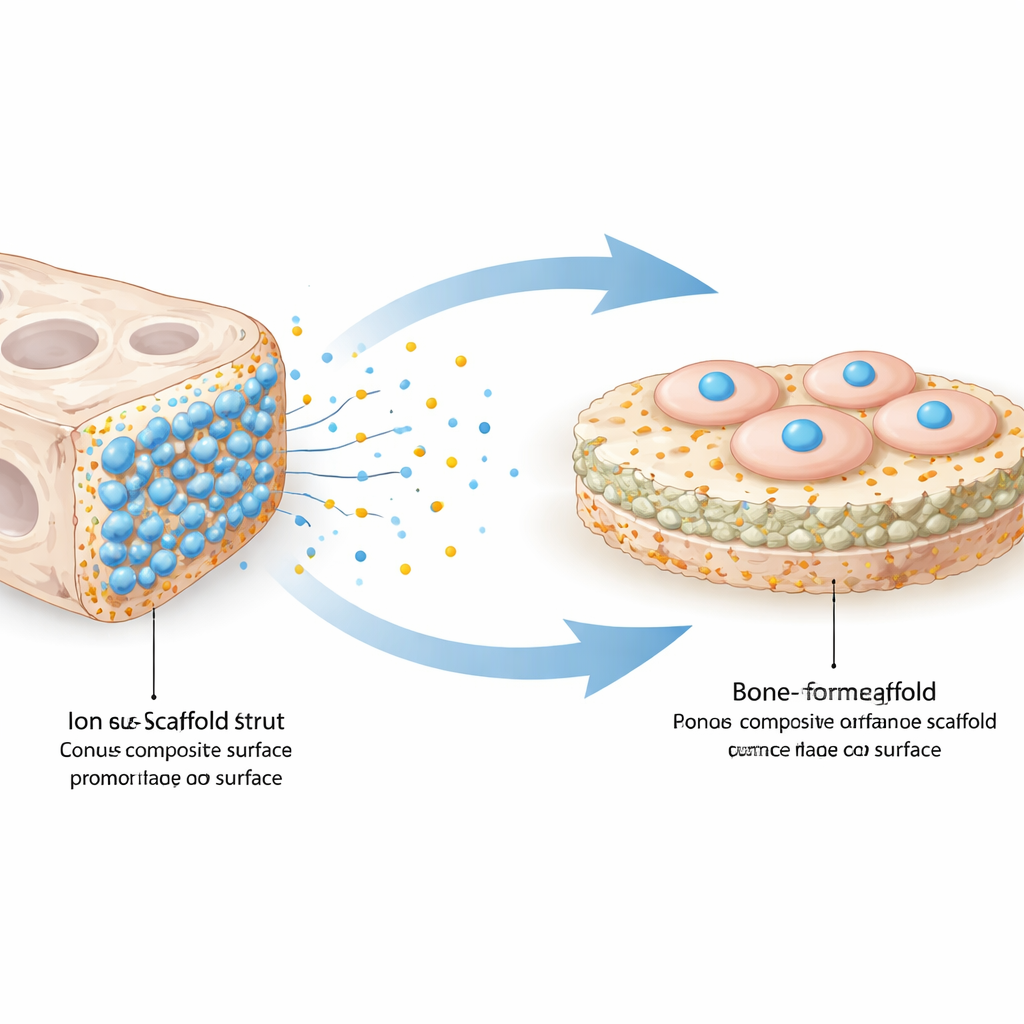
Comment les cellules osseuses réagissent au nouvel échafaudage
L’équipe a ensuite testé le comportement de cellules de type osseux sur les échafaudages non revêtus et revêtus de ZIF‑8. Au microscope, les deux types permettaient aux cellules de s’attacher et de s’étaler, mais la version enrichie en zinc présentait une couverture cellulaire visiblement plus dense et plus uniforme dès les premiers jours. Un test standard de viabilité a montré que les cellules sur l’échafaudage modifié non seulement survivaient mais se multipliaient plus vite que sur l’échafaudage simple et sur une surface témoin plane. Lorsque les chercheurs ont mesuré l’activité de plusieurs gènes liés à la formation osseuse, y compris des gènes « interrupteurs » précoces et des marqueurs tardifs des cellules osseuses matures, ils ont constaté que tous étaient significativement plus élevés sur l’échafaudage enrichi en zinc—en particulier à des temps plus avancés, lorsque la matrice osseuse minéralisée est normalement déposée.
Ce que cela pourrait signifier pour la réparation osseuse future
Dans l’ensemble, les résultats suggèrent que la combinaison d’une forte teneur en verre bioactif dans le plastique imprimé en 3D et d’un revêtement externe riche en zinc crée un échafaudage multifonctionnel, robuste, à dégradation lente et très favorable aux cellules osseuses. Le matériau est conçu pour combler des défauts dans l’os spongieux, où il peut supporter une charge tout en encourageant la reconstruction par l’organisme. Bien que des études animales supplémentaires soient nécessaires pour confirmer la sécurité et les performances à long terme, cette conception à double action ouvre la voie à des pansements osseux de nouvelle génération qui font bien plus que simplement occuper l’espace : ils guident et accélèrent activement le processus de guérison de l’intérieur vers l’extérieur.
Citation: Soleymani, M., Moslemi, S., Dini, G. et al. ZIF-8 functionalized PCL/BG composite scaffolds with improved bioactivity and osteogenic differentiation. Sci Rep 16, 14335 (2026). https://doi.org/10.1038/s41598-026-44943-1
Mots-clés: ingénierie tissulaire osseuse, échafaudages imprimés en 3D, verre bioactif, polycaprolactone, revêtement ZIF-8