Clear Sky Science · it
Scaffolds compositi PCL/BG funzionalizzati con ZIF-8 con bioattività e differenziazione osteogenica migliorate
Aiutare le ossa rotte a guarire da sole
Quando un osso è gravemente danneggiato da un incidente, un tumore o una malattia, il corpo non sempre riesce a riparare il difetto da solo. I chirurghi spesso ricorrono a innesti ossei, ma questi possono scarseggiare e comportare rischi. Questo studio esplora un nuovo tipo di “cerotto osseo” stampato in 3D progettato per essere abbastanza robusto per l’uso quotidiano nell’organismo e per stimolare attivamente la crescita, l’adesione e la maturazione delle cellule ossee in nuovo tessuto sano.
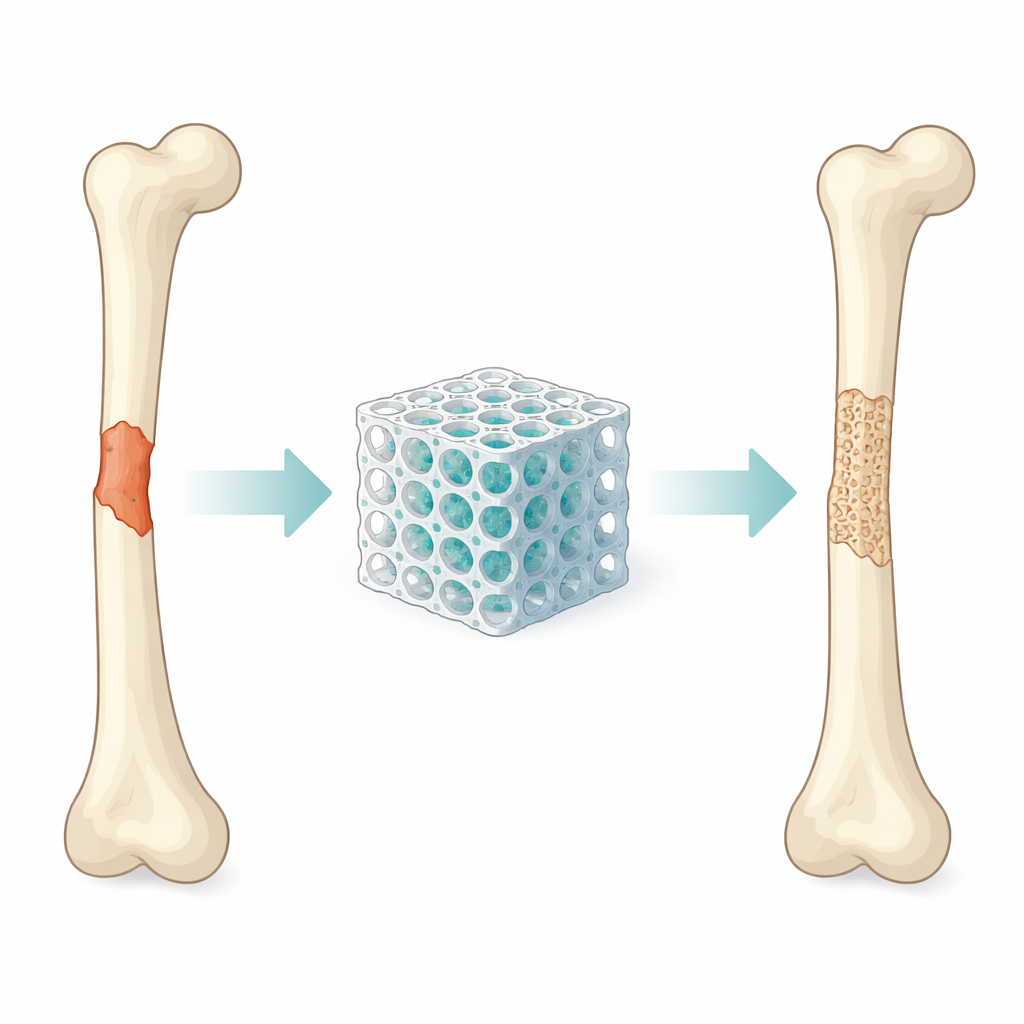
Perché servono cerotti ossei più intelligenti
I medici da tempo cercano materiali che possano sostituire l’osso mancante. Gli impianti tradizionali in metallo sono resistenti ma non si integrano naturalmente con il tessuto vivente. L’osso donato dal paziente o da un altro individuo può integrarsi bene ma è limitato in disponibilità e può causare dolore o complicazioni. Gli ingegneri dei tessuti invece realizzano strutture porose chiamate scaffold che funzionano come telai temporanei: sostengono l’area danneggiata, permettono l’ingresso di vasi sanguigni e cellule e si degradano lentamente mentre si forma nuovo osso. Perché ciò avvenga, uno scaffold deve bilanciare tre esigenze contemporaneamente: essere meccanicamente solido, compatibile con le cellule e chimicamente attivo abbastanza da stimolare la formazione ossea.
Costruire un telaio stampato in 3D migliore
I ricercatori hanno iniziato con una plastica medica di uso comune chiamata policaprolattone, facile da stampare in 3D ma intrinsecamente troppo morbida e troppo inerte per riparazioni ossee impegnative. Hanno miscelato questa plastica con grandi quantità di particelle ultrafini di un particolare vetro biattivo noto come 58S. Questo vetro è famoso per formare uno strato minerale simile all’osso al contatto con i fluidi corporei e per rilasciare ioni utili come calcio e silicio. Il team ha stampato scaffold porosi a forma di cubo contenenti il 40, il 45 o il 50 percento di vetro in peso e ha testato la resistenza alla compressione di ogni design. La versione con il 45 percento di vetro si è rivelata il miglior compromesso, raggiungendo circa 35 megapascal di resistenza—simile all’osso spugnoso (cancelloso) presente all’interno delle ossa più grandi—pur rimanendo sufficientemente porosa per la crescita tissutale.
Trasformare un telaio passivo in un partner attivo
Per migliorare ulteriormente la superficie su cui le cellule si insediano, il team ha rivestito lo scaffold scelto con il 45 percento di vetro con un sottile strato di un materiale poroso chiamato ZIF‑8, che contiene zinco. Usando un processo delicato a base d’acqua ispirato alla chimica adesiva delle cozze, hanno prima depositato un sottostrato adesivo e poi fatto crescere piccole cristallizzazioni di ZIF‑8 direttamente sulle superfici esterne dello scaffold. In un fluido che simula il plasma sanguigno, gli scaffold hanno rilasciato progressivamente ioni zinco per quattro settimane senza picchi iniziali, mantenendosi in un intervallo di concentrazione considerato sicuro per le cellule. Allo stesso tempo, il vetro all’interno dello scaffold ha rilasciato calcio, fosforo e silicio, favorendo la formazione di un rivestimento minerale di tipo osseo sulla superficie.
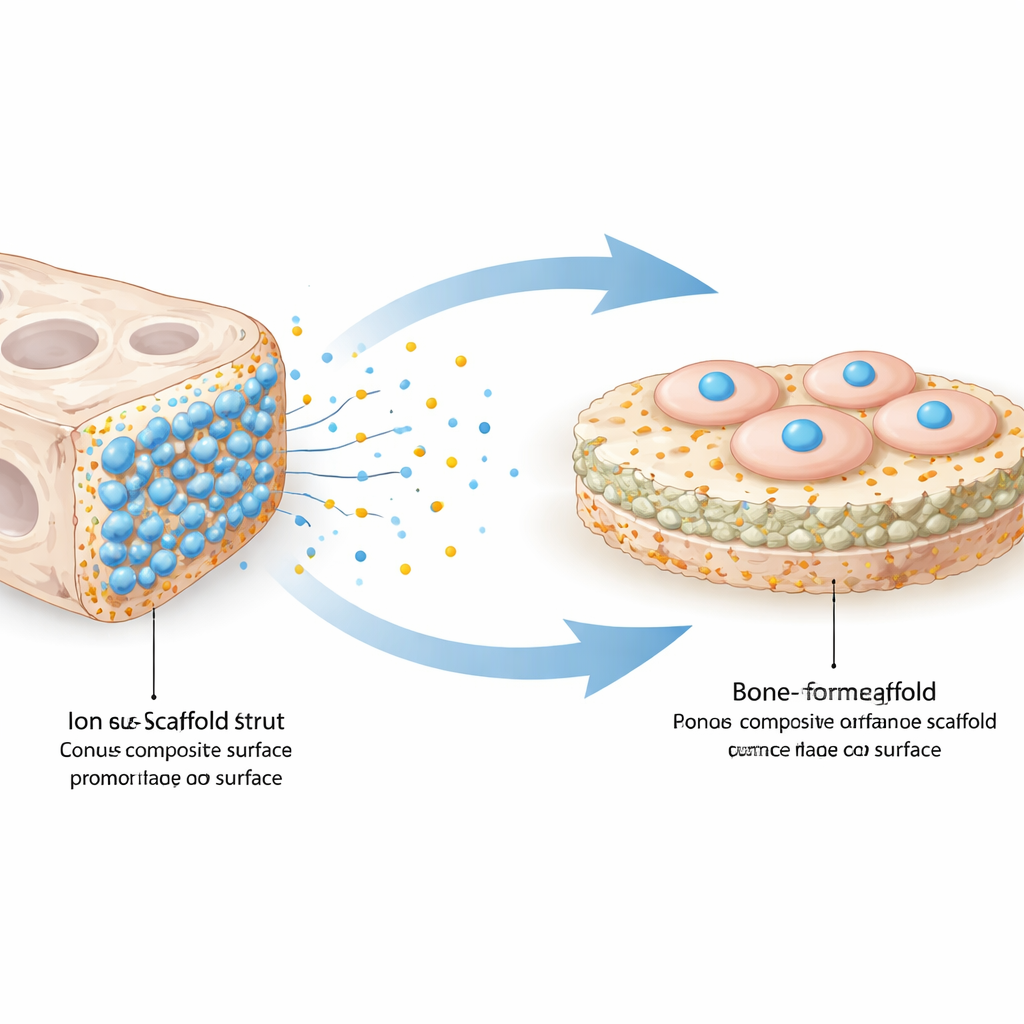
Come rispondono le cellule ossee al nuovo scaffold
Il team ha poi valutato il comportamento di cellule simili a quelle ossee sugli scaffold non rivestiti e su quelli rivestiti con ZIF‑8. Al microscopio, entrambi i tipi permettevano alle cellule di aderire e di dispiegarsi, ma la versione rivestita di zinco mostrava, già dopo pochi giorni, una copertura cellulare visibilmente più densa e uniforme. Un test standard di vitalità ha rivelato che le cellule sullo scaffold modificato non solo sopravvivevano, ma proliferavano più rapidamente rispetto allo scaffold semplice e a una superficie di controllo piana. Quando i ricercatori hanno misurato l’attività di diversi geni legati alla formazione ossea, inclusi geni precoci “interruttori” e marker tardivi di cellule ossee mature, hanno riscontrato che tutti erano significativamente più espressi sullo scaffold ricoperto di zinco—soprattutto a tempi successivi, quando normalmente si deposita la matrice ossea mineralizzata.
Cosa potrebbe significare per la futura riparazione ossea
Complessivamente, i risultati suggeriscono che combinare un’alta percentuale di vetro biattivo all’interno della plastica stampata in 3D con un rivestimento esterno ricco di zinco crea uno scaffold multifunzionale che è resistente, degradabile lentamente e molto favorevole alle cellule ossee. Il materiale è concepito per riempire difetti nell’osso spugnoso, dove può supportare i carichi favorendo al contempo la ricostruzione da parte dell’organismo. Sebbene siano necessari ulteriori studi su animali per confermare la sicurezza e le prestazioni a lungo termine, questo design a doppia azione indica la strada verso cerotti ossei di nuova generazione che fanno molto più che occupare uno spazio: guidano e accelerano attivamente il processo di guarigione dall’interno verso l’esterno.
Citazione: Soleymani, M., Moslemi, S., Dini, G. et al. ZIF-8 functionalized PCL/BG composite scaffolds with improved bioactivity and osteogenic differentiation. Sci Rep 16, 14335 (2026). https://doi.org/10.1038/s41598-026-44943-1
Parole chiave: ingegneria tissutale ossea, scaffold stampati in 3D, vetro biattivo, policaprolattone, rivestimento ZIF-8