Clear Sky Science · nl
Een CAM-bioimagingmodel onthult de verbinding tussen VEGFA-gemedieerde vasculaire remodeling en versnelde sarcoomprogressie via het tumorsecretoom
Waarom dit onderzoek ertoe doet
Sarcomen zijn kankers die ontstaan in botten en zachte weefsels en treffen vaak kinderen en jongvolwassenen. Ze zijn gevaarlijk niet alleen omdat ze snel groeien, maar ook omdat ze zich via het lichaam verspreiden met behulp van nieuw gevormde bloedvaten. Deze studie gebruikt bevruchte kippenembryo’s als een levend testplatform om in real time te volgen hoe sarcoomcellen de nabijgelegen vaten herschikken en hoe het blokkeren van één sleutel‑signaal hun groei en uitzaaiing kan vertragen. Het werk wijst op snellere, goedkopere manieren om geneesmiddelen te testen en verfijnt ons begrip van hoe tumoren nieuw terrein voorbereiden voordat ze daar binnendringen.
Een venster bouwen naar tumorgroei
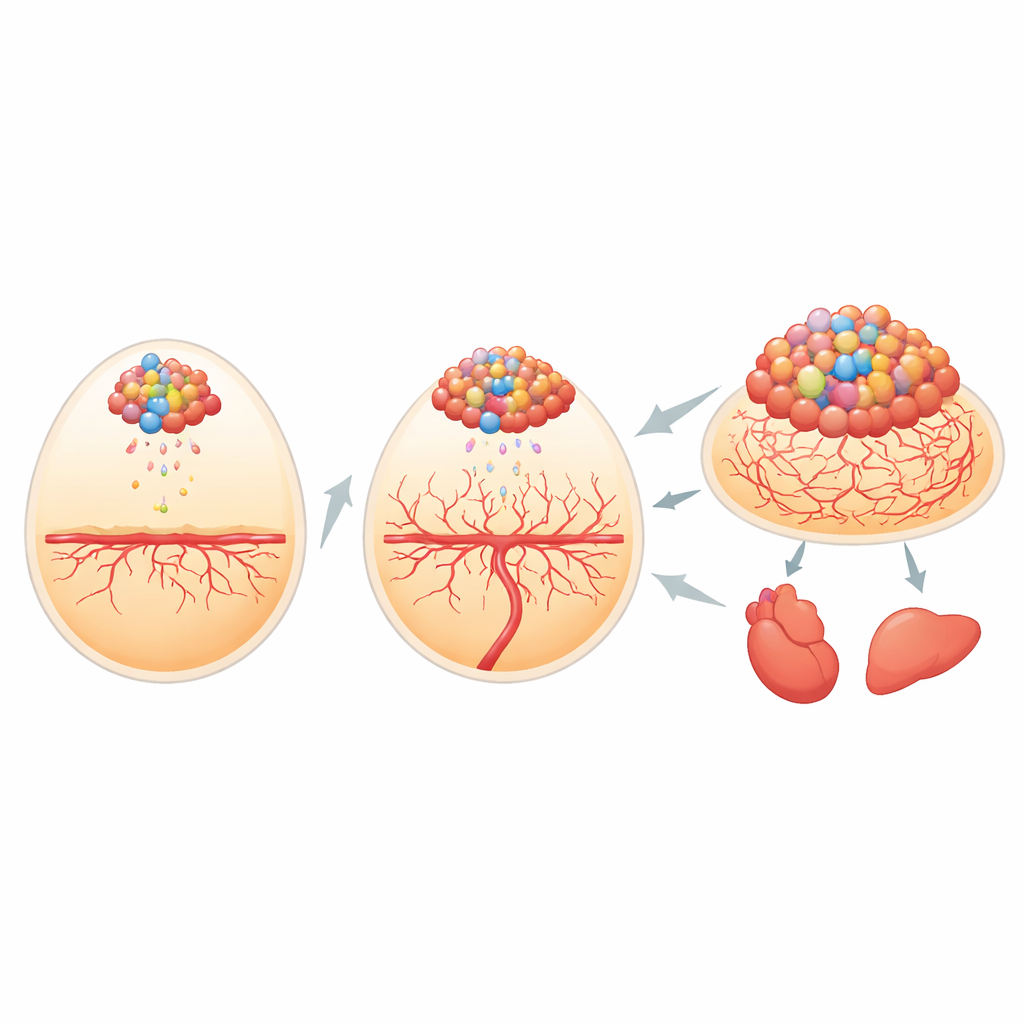
De onderzoekers moesten eerst een methode ontwikkelen om piepkleine cluster(tjes) kankercellen in de zich ontwikkelende kip te volgen. Ze hebben humane botkankercellen en muizen‑zachte‑weefselkankercellen zodanig gemodificeerd dat ze twee lichtproducerende markers dragen: één die oplicht onder bepaald gekleurd licht en één die zelf licht uitzendt wanneer een chemische brandstof wordt toegevoegd. Zodra deze cellen op het rijk gevasculariseerde membraan rond het kippenembryo werden geplaatst, kon het team de helderheid van het signaal meten en die vrijwel perfect koppelen aan de werkelijke tumorgrootte. De zelfoplichtende marker bleek bijzonder krachtig om zeer kleine groepen cellen te detecteren die waren losgeraakt en zich in organen zoals hart en lever hadden genesteld, waardoor de wetenschappers metastase met hoge gevoeligheid konden volgen.
Hoe tumor"boodschappen" nieuw terrein voorbereiden
Voordat kankercellen werden toegevoegd, week het team het membraan in tumorcel‑geconditioneerd medium, in feite de bouillon waarin sarcoomcellen hadden gegroeid. Deze vloeistof bevat het tumorsecretoom—honderden moleculen die door de cellen worden afgestoten. Membranen die vooraf op deze manier waren behandeld, vormden vaker tumoren, en die tumoren waren regelmatiger, groter en volker met delende cellen dan tumoren op membranen die alleen gewoon medium hadden gezien. Het secretoom stimuleerde ook dat kankercellen de oorspronkelijke plaats verlieten en in verre embryo‑organen verschenen, wat nabootst hoe sarcomen zich in het lichaam verspreiden. Deze bevindingen suggereren dat door tumoren vrijgegeven factoren nabijgelegen weefsel kunnen “voorconditioneren”, waardoor het een vriendelijker terrein wordt voor kanker om zich te vestigen en te reizen.
Bloedvaten herbedraden en lekkend maken
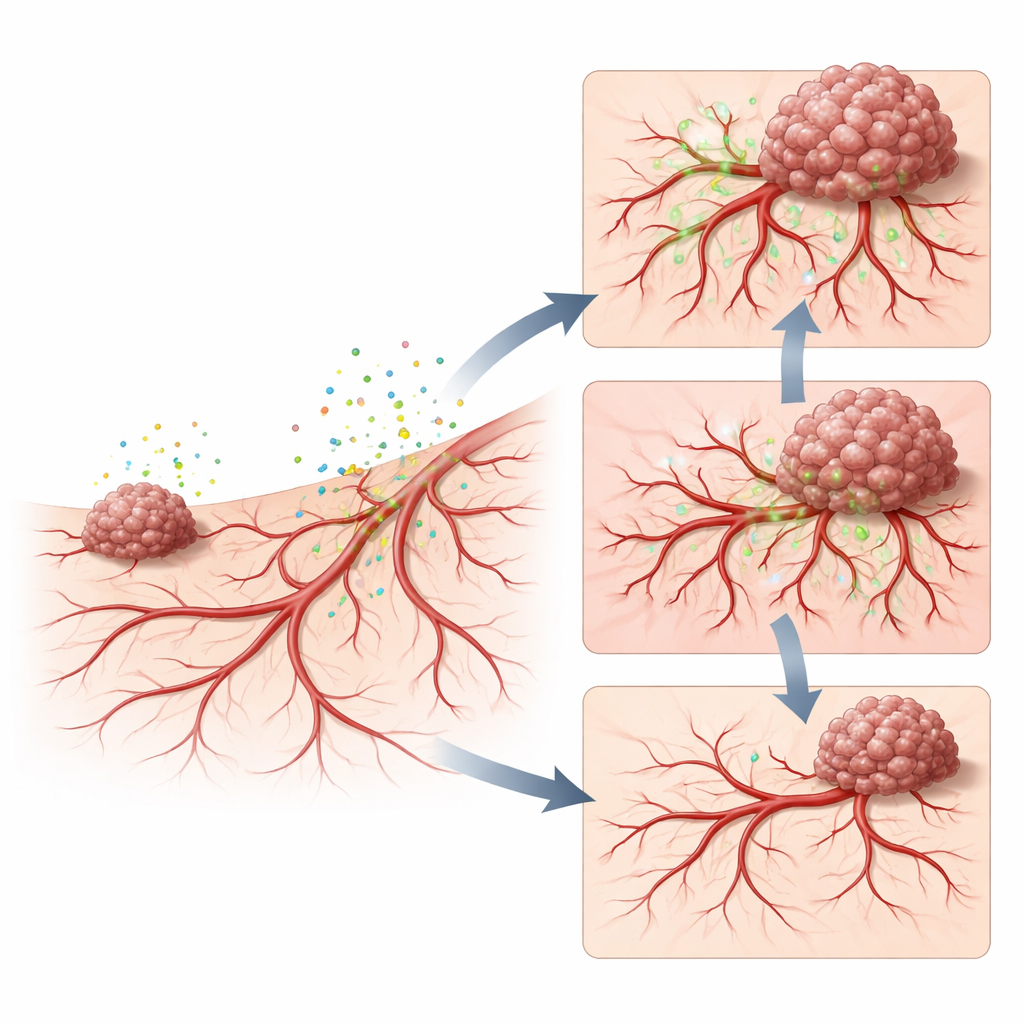
Om te achterhalen wat het secretoom met het gastweefsel deed, onderzochten de wetenschappers de groei en de permeabiliteit van bloedvaten. Tumorgeconditioneerd medium veroorzaakte een piek van fijne nieuwe vaten in het membraan en rond vroege tumoren, waardoor een dicht netwerk ontstond dat snel groeiende kanker kan voeden. Toen een fluorescerende kleurstof gekoppeld aan een groot suikermolecuul in de circulatie werd geïnjecteerd, sijpelde veel meer daarvan na secretoom‑behandeling het tumorgebied in, wat aantoonde dat de nieuwe vaten uitzonderlijk lek waren. Dit lekkende, overgroeide netwerk weerspiegelt wat wordt gezien bij agressieve menselijke kankers, waar abnormale vaten niet alleen nutriënten leveren maar ook kankercellen gemakkelijke uitgangen naar de bloedbaan geven.
VEGFA aanwijzen als sleuteldriver
Het team vroeg vervolgens welke uitgescheiden moleculen hiervoor verantwoordelijk waren. Door tientallen signaalproteïnen in de tumorbouillon te profileren, ontdekten ze dat meerdere vaatgroeifactoren verhoogd waren, waarbij één, VEGFA genaamd, opviel als zowel gemeenschappelijk tussen verschillende saroomlijnen als bijzonder overvloedig in de meer metastatische cellen. Toen ze VEGFA in het secretoom neutraliseerden met een klinisch gebruikt antistofgeneesmiddel, liet het membraan veel minder nieuwe vaten zien, minder lekkage, kleinere tumoren en vrijwel geen detecteerbare metastasen. Het kort opnieuw toevoegen van VEGFA herstelde gedeeltelijk de abnormale vaten, de lekkage en de tumorspreiding. Deze experimenten plaatsen VEGFA in het centrum van een keten die tumorafscheidingen, remodeling van de vasculaire niche en versnelde sarcoomprogressie met elkaar verbindt.
Wat dit betekent voor patiënten en toekomstig onderzoek
Dit werk toont aan dat sarcoomcellen zich niet alleen aan hun omgeving aanpassen; ze herscheppen die omgeving actief vooraf door factoren vrij te geven die nieuwe, fragiele bloedvaten aantrekken. In het hier ontwikkelde kippenembryo‑systeem kan die remodeling binnen dagen worden waargenomen en gemeten, met behulp van lichtgevende tumorcellen als aflezing van groei en verspreiding. Door VEGFA als een belangrijke schakel te onthullen die deze pro‑tumor remodeling aanzet, ondersteunt de studie pogingen om dit signaal en verwante routes bij sarcoom te richten. Tegelijkertijd biedt het onderzoekers een praktisch platform om combinaties van medicijnen te testen die het tumorsecretoom kalmeren, vaten stabiliseren en uiteindelijk de kans verkleinen dat deze kankers groeien en metastaseren.
Bronvermelding: Wang, Y., Xue, W., Sakr, N. et al. A CAM bioimaging model reveals the connection between VEGFA vascular remodeling and enhanced sarcoma progression via tumor secretome. Sci Rep 16, 12525 (2026). https://doi.org/10.1038/s41598-026-42154-2
Trefwoorden: sarcoom, tumormicro-omgeving, angiogenese, VEGFA, CAM-model