Clear Sky Science · de
Ein CAM-Bioimaging-Modell zeigt die Verbindung zwischen VEGFA-vermittelter Gefäßumgestaltung und verstärktem Sarkomwachstum über das Tumorsekretom
Warum diese Forschung wichtig ist
Sarkome sind Krebsarten, die in Knochen und Weichgewebe entstehen und häufig Kinder und junge Erwachsene betreffen. Sie sind gefährlich, nicht nur weil sie schnell wachsen, sondern weil sie sich mithilfe neu gebildeter Blutgefäße im Körper ausbreiten. In dieser Studie werden befruchtete Hühnereier als lebendes Versuchssystem genutzt, um in Echtzeit zu beobachten, wie Sarkomzellen benachbarte Gefäße umgestalten und wie die Blockade eines einzigen Schlüsselsignals ihr Wachstum und ihre Ausbreitung verlangsamen kann. Die Arbeit weist auf schnellere, kostengünstigere Möglichkeiten hin, Medikamente zu testen, und verfeinert unser Verständnis dafür, wie Tumoren neues Territorium vorbereiten, bevor sie eintreffen.
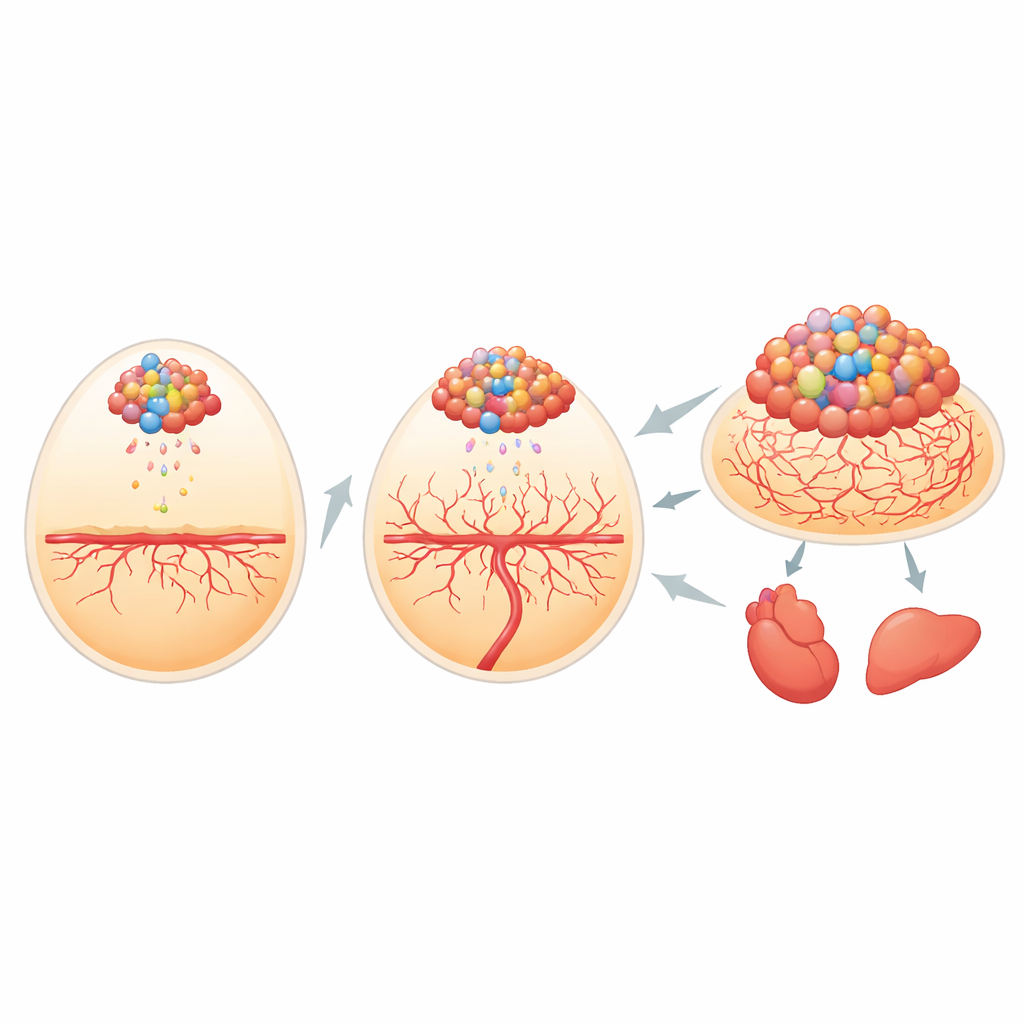
Ein Fenster in das Tumorwachstum bauen
Die Forschenden brauchten zunächst eine Methode, um winzige Zellklumpen im sich entwickelnden Küken zu verfolgen. Sie konstruierten humane Knochenkrebs- und Maus-Weichgewebstumorzellen so, dass sie zwei lichtabgebende Marker tragen: einen, der unter bestimmtem farbigen Licht leuchtet, und einen zweiten, der selbst Licht aussendet, wenn ihm ein chemischer Brennstoff zugeführt wird. Sobald diese Zellen auf die gut durchblutete Membran gelegt wurden, die den Embryo umgibt, konnte das Team die Signalstärke messen und sie nahezu perfekt mit der tatsächlichen Tumorgröße korrelieren. Der selbstleuchtende Marker erwies sich als besonders nützlich, um sehr kleine Zellgruppen zu erkennen, die sich gelöst und in Organen wie Herz und Leber eingenistet hatten, sodass die Wissenschaftler die Metastasierung mit hoher Empfindlichkeit verfolgen konnten.
Wie Tumor-„Botschaften" neues Terrain vorbereiten
Bevor Krebszellen zugegeben wurden, tränkte das Team die Membran mit tumorzellkonditioniertem Medium, im Grunde der Nährlösung, in der Sarkomzellen gewachsen waren. Diese Flüssigkeit enthält das Tumorsekretom – Hunderte von Molekülen, die von den Zellen abgesondert werden. Vorbehandelte Membranen entwickelten häufiger Tumoren, und diese Tumoren waren regelmäßiger, größer und stärker mit teilenden Zellen gefüllt als Tumoren auf Membranen, die nur normales Medium gesehen hatten. Das Sekretom veranlasste außerdem Krebszellen dazu, den Ursprungsort zu verlassen und in entlegenen embryonalen Organen aufzutauchen, was das Ausbreitungsverhalten von Sarkomen im Körper nachahmt. Diese Befunde deuten darauf hin, dass von Tumoren freigesetzte Faktoren umliegendes Gewebe „vorbereiten“ können und es damit zu einem günstigeren Standort für die Ansiedlung und das Fortschreiten von Krebs machen.
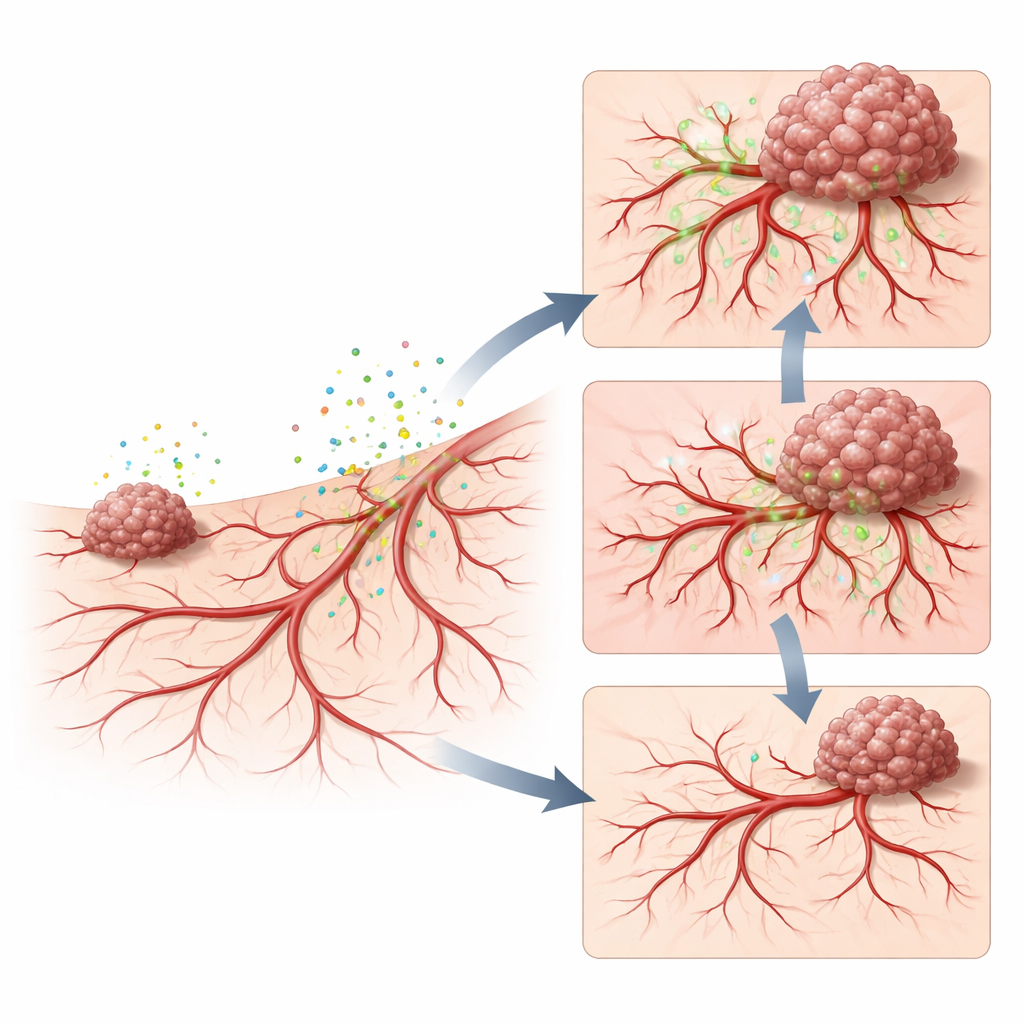
Umbau der Blutgefäße und erhöhte Durchlässigkeit
Um herauszufinden, was das Sekretom im Wirtsgewebe bewirkte, untersuchten die Forschenden das Gefäßwachstum und die Gefäßdurchlässigkeit. Tumorkonditioniertes Medium löste einen Schub feiner neuer Gefäße in der Membran und rund um frühe Tumoren aus und bildete ein dichtes Netz, das schnell wachsenden Tumoren Nahrung liefern kann. Wurde ein fluoreszierender Farbstoff, gekoppelt an ein großes Zuckermolekül, in den Kreislauf injiziert, sickerte deutlich mehr davon nach Sekretombehandlung in das Tumorgewebe, was zeigt, dass die neuen Gefäße ungewöhnlich durchlässig waren. Dieses undichte, überwachsene Gefäßnetz spiegelt wider, was bei aggressiven menschlichen Krebserkrankungen beobachtet wird, wo abnorme Gefäße nicht nur Nährstoffe liefern, sondern Tumorzellen auch erleichterte Ausstiegswege ins Blut bieten.
VEGFA als zentraler Treiber identifizieren
Das Team fragte dann, welche ausgeschiedenen Moleküle verantwortlich sind. Durch die Profilierung Dutzender Signalproteine in der Tumorsuppe stellten sie fest, dass mehrere gefäßanregende Faktoren erhöht waren, wobei ein Faktor namens VEGFA sowohl bei verschiedenen Sarkomlinien häufig vorkam als auch besonders reichlich in den stärker metastatischen Zellen vorhanden war. Als sie VEGFA im Sekretom mit einem klinisch eingesetzten Antikörper neutralisierten, zeigten die Membranen deutlich weniger neue Gefäße, geringere Durchlässigkeit, kleinere Tumoren und nahezu keine nachweisbaren Metastasen. Eine kurze Wiederzugabe von VEGFA stellte teilweise die abnormalen Gefäße, die Leckage und die Tumorausbreitung wieder her. Diese Experimente platzieren VEGFA in der Mitte einer Kette, die Tumorsekrete, Umbau der vaskulären Nische und verstärktes Sarkomprogression verbindet.
Was das für Patientinnen und Patienten und künftige Studien bedeutet
Diese Arbeit zeigt, dass Sarkomzellen sich nicht nur an ihre Umgebung anpassen; sie formen sie aktiv vorab, indem sie Faktoren freisetzen, die neue, fragile Blutgefäße anlocken. In dem hier entwickelten Kükenembryo-System kann dieser Umbau innerhalb weniger Tage beobachtet und quantifiziert werden, wobei lichtemittierende Tumorzellen als Maß für Wachstum und Ausbreitung dienen. Indem VEGFA als wichtiger Schalter identifiziert wird, der dieses pro-tumorale Umbauprogramm einschaltet, unterstützt die Studie Bestrebungen, dieses Signal und verwandte Wege in Sarkomen gezielt anzugehen. Zugleich bietet sie Forschenden eine praktische Plattform, um Wirkstoffkombinationen zu testen, die das Tumorsekretom beruhigen, Gefäße stabilisieren und letztlich die Wahrscheinlichkeit verringern, dass diese Tumoren wachsen und metastasieren.
Zitation: Wang, Y., Xue, W., Sakr, N. et al. A CAM bioimaging model reveals the connection between VEGFA vascular remodeling and enhanced sarcoma progression via tumor secretome. Sci Rep 16, 12525 (2026). https://doi.org/10.1038/s41598-026-42154-2
Schlüsselwörter: Sarkom, Tumormikroumgebung, Angiogenese, VEGFA, CAM-Modell