Clear Sky Science · fr
Un modèle d’imagerie CAM révèle le lien entre le remodelage vasculaire par la VEGFA et l’accélération de la progression des sarcomes via le secretome tumoral
Pourquoi cette recherche est importante
Les cancers appelés sarcomes prennent naissance dans les os et les tissus mous et touchent souvent les enfants et les jeunes adultes. Ils sont dangereux non seulement parce qu’ils croissent rapidement, mais aussi parce qu’ils se propagent dans l’organisme avec l’aide de nouveaux vaisseaux sanguins formés autour d’eux. Cette étude utilise des œufs de poule fécondés comme banc d’essai vivant pour observer, en temps réel, comment les cellules de sarcome réorganisent les vaisseaux voisins et comment le blocage d’un signal clé peut ralentir leur croissance et leur dissémination. Ce travail ouvre la voie à des méthodes de test de médicaments plus rapides et moins coûteuses et affine notre compréhension de la façon dont les tumeurs préparent de nouveaux territoires avant d’y parvenir.
Construire une fenêtre sur la croissance tumorale
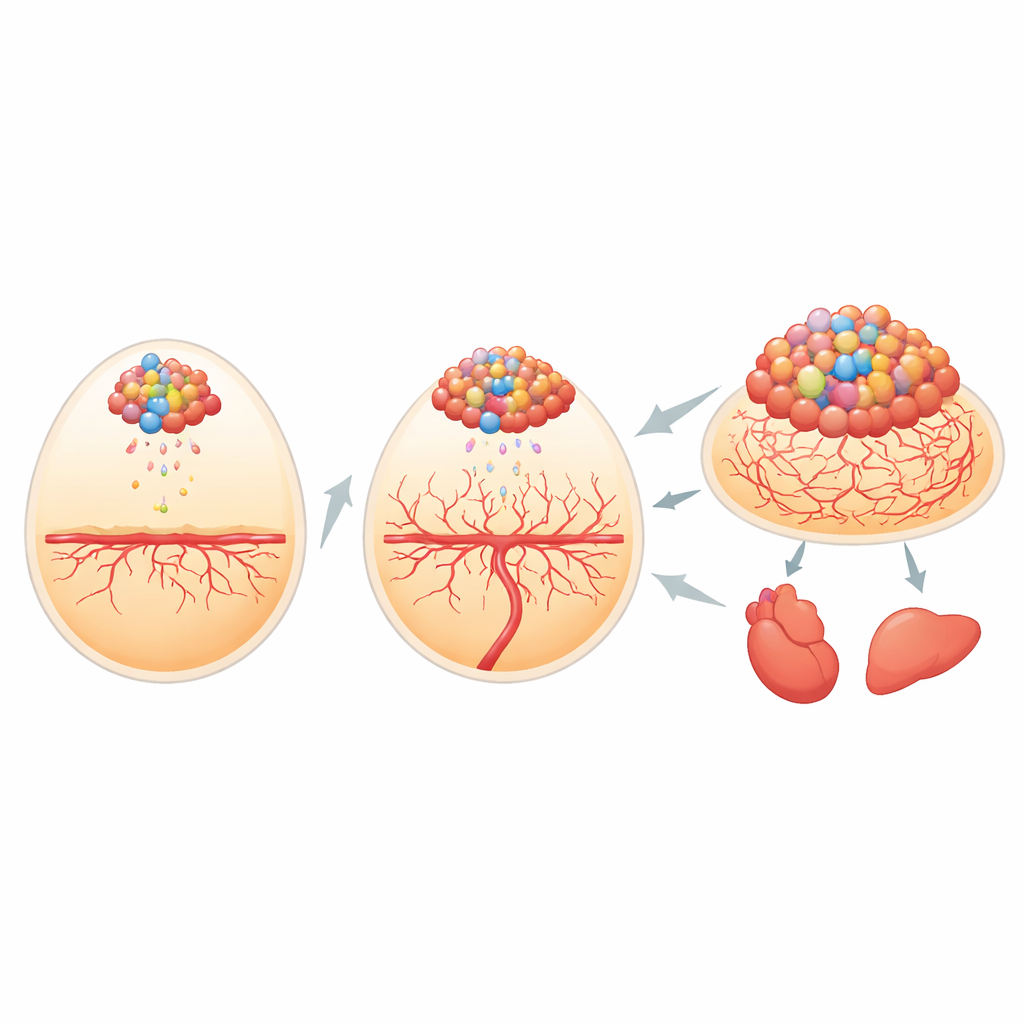
Les chercheurs ont d’abord dû trouver un moyen de suivre de minuscules amas de cellules cancéreuses à l’intérieur de l’embryon de poulet en développement. Ils ont modifié des cellules de cancer osseux humain et de cancer des tissus mous murin pour qu’elles portent deux marqueurs bioluminescents : l’un qui brille sous une lumière colorée spécifique et l’autre qui émet sa propre lumière lorsqu’on lui fournit un carburant chimique. Lorsqu’on a placé ces cellules sur la membrane richement vascularisée qui entoure l’embryon de poulet, l’équipe a pu mesurer l’intensité du signal et la corréler presque parfaitement à la taille réelle des tumeurs. Le marqueur auto‑luminescent s’est révélé particulièrement utile pour repérer de très petits groupes de cellules qui s’étaient détachés et logés dans des organes tels que le cœur et le foie, permettant aux scientifiques de suivre les métastases avec une grande sensibilité.
Comment les « messages » tumoraux préparent le terrain
Avant d’ajouter les cellules cancéreuses, l’équipe a imprégné la membrane d’un milieu conditionné par des cellules tumorales, essentiellement le bouillon dans lequel les cellules de sarcome avaient été cultivées. Ce liquide contient le secretome tumoral — des centaines de molécules libérées par les cellules. Les membranes prétraitées de cette façon ont formé des tumeurs plus fréquemment, et ces tumeurs étaient plus régulières, plus volumineuses et remplies de cellules en division que les tumeurs sur des membranes ayant reçu seulement du milieu simple. Le secretome a aussi poussé les cellules cancéreuses à quitter le site d’origine et à apparaître dans des organes embryonnaires distants, reproduisant la manière dont les sarcomes se propagent dans l’organisme. Ces résultats suggèrent que les facteurs libérés par la tumeur peuvent « préconditionner » les tissus voisins, rendant le terrain plus favorable à l’implantation et à la propagation du cancer.
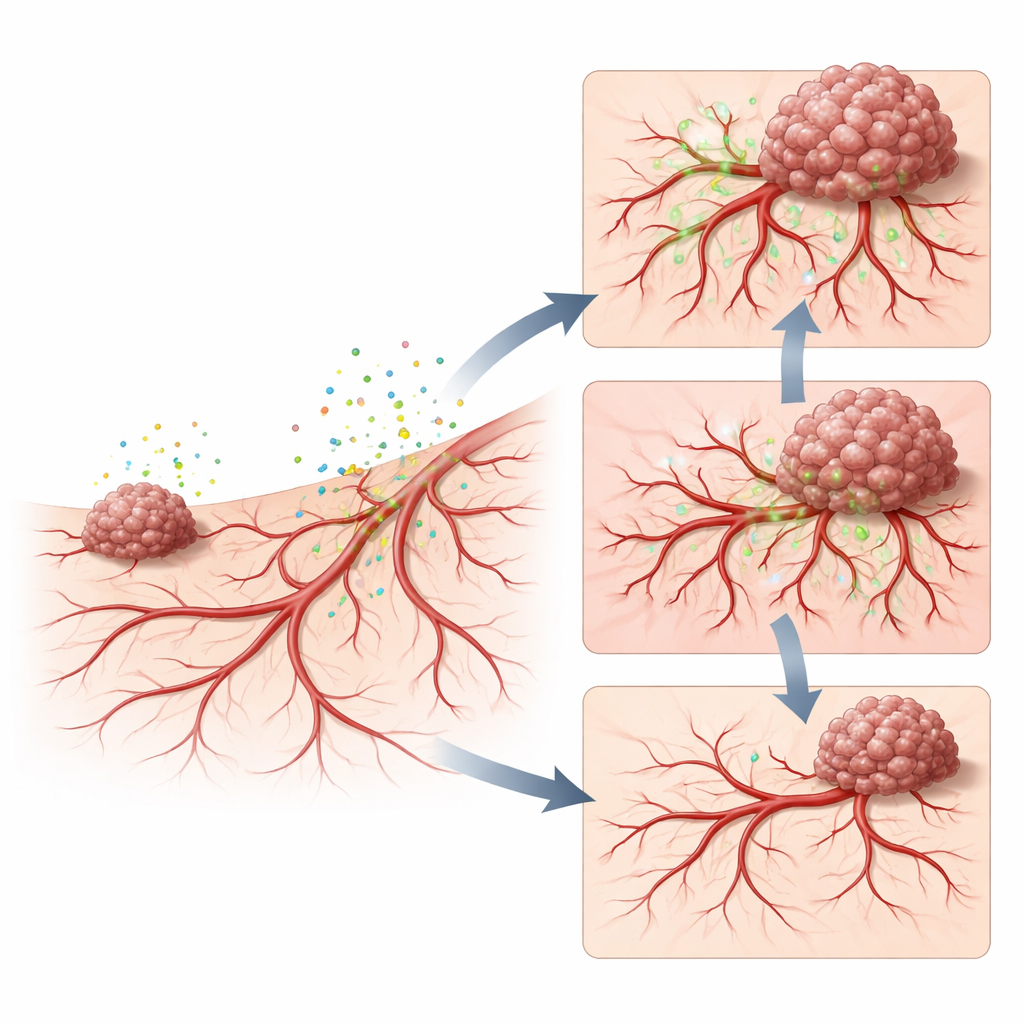
Reconfiguration des vaisseaux sanguins et augmentation de leur perméabilité
Pour comprendre ce que le secretome faisait au tissu hôte, les scientifiques ont examiné la croissance et la perméabilité des vaisseaux sanguins. Le milieu conditionné par la tumeur a provoqué une poussée de fins nouveaux vaisseaux dans la membrane et autour des premières tumeurs, construisant un réseau dense capable d’alimenter un cancer en forte croissance. Lorsqu’un colorant fluorescent lié à une grosse molécule de sucre a été injecté dans la circulation, beaucoup plus de ce colorant a filtré dans le tissu tumoral après le traitement par le secretome, montrant que les nouveaux vaisseaux étaient anormalement perméables. Ce réseau fuyant et surdéveloppé reflète ce qu’on observe dans les cancers humains agressifs, où des vaisseaux anormaux apportent non seulement des nutriments mais offrent aussi aux cellules cancéreuses des sorties faciles vers la circulation sanguine.
Identifier la VEGFA comme moteur clé
L’équipe a ensuite cherché à savoir quelles molécules sécrétées en étaient responsables. En profilant des dizaines de protéines de signalisation dans le bouillon tumoral, ils ont constaté que plusieurs facteurs favorisant la croissance vasculaire étaient élevés, parmi lesquels un nommé VEGFA se distinguait, à la fois commun à différentes lignées de sarcomes et particulièrement abondant dans les cellules les plus métastatiques. Lorsqu’ils neutralisaient la VEGFA dans le secretome à l’aide d’un anticorps thérapeutique utilisé en clinique, la membrane présentait beaucoup moins de nouveaux vaisseaux, moins de fuite, des tumeurs plus petites et presque aucune métastase détectable. La réintroduction brève de la VEGFA a partiellement restauré les vaisseaux anormaux, la fuite et la dissémination tumorale. Ces expériences placent la VEGFA au centre d’une chaîne reliant les sécrétions tumorales, le remodelage du microenvironnement vasculaire et l’aggravation des sarcomes.
Ce que cela signifie pour les patients et les études futures
Ce travail montre que les cellules de sarcome ne se contentent pas de s’adapter à leur environnement ; elles le remodelent activement en amont en libérant des facteurs qui attirent de nouveaux vaisseaux fragiles. Dans le système d’embryon de poulet développé ici, ce remodelage peut être observé et mesuré en quelques jours, en utilisant des cellules tumorales émettrices de lumière comme indicateur de la croissance et de la dissémination. En révélant la VEGFA comme un interrupteur majeur qui déclenche ce remodelage pro‑tumoral, l’étude appuie les efforts visant à cibler ce signal et les voies associées dans les sarcomes. Parallèlement, elle offre aux chercheurs une plateforme pratique pour tester des combinaisons de médicaments visant à calmer le secretome tumoral, stabiliser les vaisseaux et, en fin de compte, réduire la probabilité que ces cancers croissent et métastasent.
Citation: Wang, Y., Xue, W., Sakr, N. et al. A CAM bioimaging model reveals the connection between VEGFA vascular remodeling and enhanced sarcoma progression via tumor secretome. Sci Rep 16, 12525 (2026). https://doi.org/10.1038/s41598-026-42154-2
Mots-clés: sarcome, microenvironnement tumoral, angiogenèse, VEGFA, modèle CAM