Clear Sky Science · nl
Miller–Ross-functiecoëfficiënten en kernel-gebaseerde CT-scan-verbeteringstechniek
Heldere hersenscans voor duidelijkere antwoorden
Computertomografie (CT)-scans zijn essentieel bij het stellen van diagnoses van hersenaandoeningen, maar de ruwe beelden kunnen ruisig, onscherp of laag in contrast zijn—vooral wanneer artsen proberen de stralingsdosis te verlagen. Dit artikel onderzoekt een wiskundig gedreven methode om hersen-CT-beelden te verscherpen voordat ze door radiologen of computersystemen worden geanalyseerd. In plaats van te vertrouwen op grote neurale netwerken gebruiken de auteurs een zorgvuldig ontworpen 3 × 3-beeldfilter dat is opgebouwd uit een speciale familie wiskundige functies, met als doel betere structuur en zichtbaarheid van fijne details in medische scans.
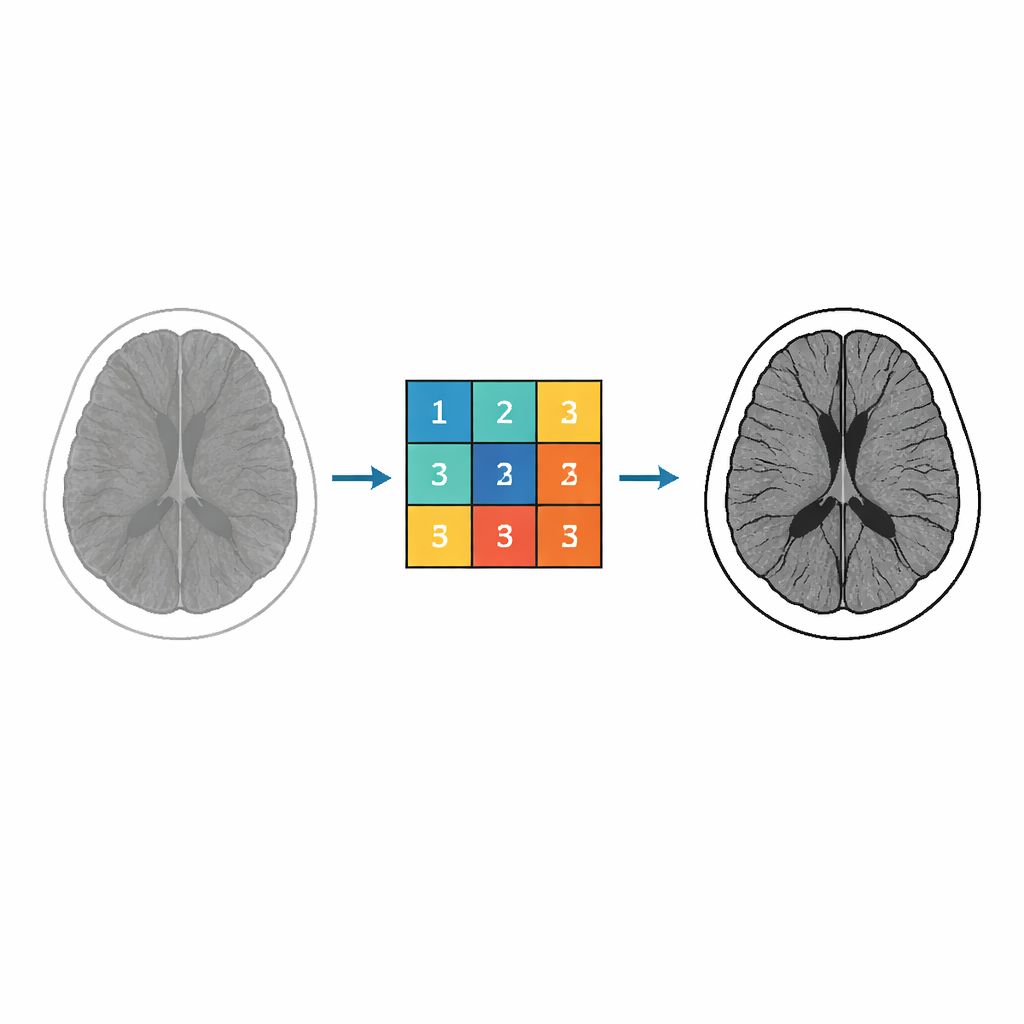
Van abstracte wiskunde naar beeldfilters
Centraal in het werk staat een klasse complexwaardige functies die bekendstaat als Miller–Ross-functies, oorspronkelijk ontwikkeld om fractionele differentiaalvergelijkingen op te lossen. Wiskundigen bestuderen deze functies om hun geometrische eigenschappen, zoals hoe ze een gebied van het complexe vlak naar een ander gebied afbeelden zonder overlappingen. De auteurs benutten deze eigenschappen om te sturen hoe pixelintensiteiten in een beeld worden getransformeerd. Door de coëfficiënten in de reeksexpansie van deze functies te analyseren en te begrenzen, leiden ze expliciete numerieke waarden af die als gewichten in een beeldfilter kunnen worden gebruikt. Deze gewichten worden vervolgens samengevoegd tot een 3 × 3-kernel—een klein rooster dat over het beeld schuift en nabije pixelwaarden combineert om lokale structuur te versterken.
Het bouwen van een verstelbare verbeteringskernel
Het kernidee is om meerdere abstracte parameters uit het Miller–Ross-raamwerk om te zetten in knoppen die het gedrag van het filter bepalen. Verschillende parameters beïnvloeden hoe sterk randen worden benadrukt, hoeveel ruis wordt onderdrukt en hoe fijne details worden behandeld. Met behulp van ongelijkheden die zij bewijzen voor de functiеcoëfficiënten genereren de auteurs negen getallen die de 3 × 3-kernel vullen. Ze richten zich met name op een fractionele parameter die sterk bepaalt hoe subtiele structuren in de hersenen—zoals weefselgrenzen en kleine laesies—naar voren komen. Door deze en andere parameters aan te passen kunnen ze schakelen tussen mildere en agressievere verbetering, terwijl ze binnen wiskundig gecontroleerde grenzen blijven.

De methode testen op echte CT-gegevens
Om hun aanpak te beoordelen passen de onderzoekers deze Miller–Ross-gebaseerde kernels toe op 155 geïnfecteerde hersen-CT-afbeeldingen uit een openbare dataset. Ze ontwerpen drie hoofdexperimentele scenario’s, waarbij in elk scenario de meeste parameters vaststaan en één belangrijke grootheid varieert: in het eerste stemmen ze een contrastachtige parameter af; in het tweede en derde variëren ze een andere fractionele parameter onder twee verschillende instellingen. Voor elke CT-afbeelding zoeken ze de parameterwaarde die de beste verbetering oplevert. De kwaliteit van de verbeterde beelden wordt gemeten met twee gangbare statistieken: Peak Signal-to-Noise Ratio (PSNR), die aangeeft hoeveel het beeld afwijkt van een referentie, en Structural Similarity Index (SSIM), die weergeeft hoe goed belangrijke patronen en structuren behouden blijven. In de beste gevallen levert de methode opmerkelijk hoge PSNR- en SSIM-waarden op, waarbij sommige beelden een SSIM benaderen van 0,99, wat duidt op zeer sterke structurele getrouwheid.
Hoe het zich verhoudt tot moderne AI-methoden
Vervolgens plaatsen de auteurs hun resultaten naast een reeks gevestigde CT-verbeterings- en denoising-technieken, waaronder populaire deep learning-modellen zoals convolutionele neurale netwerken, generatieve adversariële netwerken en residual networks, evenals klassieke benaderingen zoals non-local means en BM3D-filtering. Gemiddeld behalen die diepe modellen nog steeds hogere en stabielere PSNR- en SSIM-scores, wat hun kracht weerspiegelt wanneer ze op grote datasets zijn getraind. De nieuwe Miller–Ross-gebaseerde aanpak laat echter een brede prestatierespons zien: terwijl sommige beelden minder indrukwekkend zijn, overtreffen andere de beste gerapporteerde scores van traditionele filters en naderen ze die van complexere systemen. Deze variabiliteit benadrukt de gevoeligheid van de methode voor parameterkeuzes, maar ook het potentieel wanneer die keuzes goed worden afgestemd.
Belofte en praktische grenzen
De studie concludeert dat de voorgestelde kernel-gebaseerde verbeteringsmethode nog niet overal beter presteert dan eersteklas deep learning-methoden, maar dat zij belangrijke voordelen biedt. Omdat het filter rechtstreeks is opgebouwd uit transparante wiskundige formules, kunnen clinici en ingenieurs begrijpen en beheersen hoe elke parameter het resultaat beïnvloedt—iets wat bij black-box neurale netwerken vaak moeilijk is. De methode blinkt uit in het accentueren van fijne structurele details die bij de diagnose kunnen helpen, zelfs wanneer de globale kwaliteitscores niet altijd stijgen. De auteurs noemen beperkingen, waaronder de afhankelijkheid van een kleine dataset, het vertrouwen op louter numerieke maatstaven en de noodzaak van zorgvuldige parameterafstelling, en pleiten voor toekomstig werk met klinische feedback en grotere studies. Desalniettemin illustreert de aanpak hoe ideeën uit de zuivere wiskunde kunnen worden omgezet in praktische hulpmiddelen om levensreddende beelden duidelijker en informatiever te maken.
Bronvermelding: Murugusundaramoorthy, G., Nalliah, M. Miller–Ross-functions coefficients and kernel-based CT-scan enhancement technique. Sci Rep 16, 13527 (2026). https://doi.org/10.1038/s41598-026-41609-w
Trefwoorden: CT-beeldverbetering, hersenbeeldvorming, beeldfiltering, fractionele calculus, medische beeldverwerking